Tata nama senyawa kimia: Perbedaan antara revisi
k Bot: Perubahan kosmetika |
Menolak 4 perubahan teks terakhir (oleh 182.1.50.156 dan AABot) dan mengembalikan revisi 13793424 oleh HsfBot |
||
| Baris 1: | Baris 1: | ||
'''TATA NAMA SENYAWA''' |
|||
'''Tata nama kimia''' adalah serangkaian aturan [[senyawa kimia|persenyawaan-persenyawaan kimia]] yang disusun secara sistematis. '''Tata nama kimia''' disusun berdasarkan aturan [[IUPAC]] (''International Union of Pure and Applied Chemistry).'' |
'''Tata nama kimia''' adalah serangkaian aturan [[senyawa kimia|persenyawaan-persenyawaan kimia]] yang disusun secara sistematis. '''Tata nama kimia''' disusun berdasarkan aturan [[IUPAC]] (''International Union of Pure and Applied Chemistry).'' |
||
=== |
=== Senyawa Ionik === |
||
Ionik terbentuk dari [[kation]] (ion positif) dan [[anion]] (ion negatif). Banyak senyawa ionik merupakan senyawa biner, yaitu senyawa yang terbentuk dari hanya dua unsur. Untuk senyawa ionik biner, penamaan dimulai dari kation logam kemudian diikuti anion nonlogam dan diberi akhiran "-ida". Untuk kation yang memiliki lebih dari 1 jenis muatan (bilangan oksidasi), diberi keterangan angka romawi di tengahnya sesuai besarnya muatan<ref name=":0">Chang R.2003. ''General Chemistry: The Essential Concept'', ahli bahasa: Indra Noviandri dkk, 2004, Kimia Dasar Jilid 1. Jakarta: Erlangga</ref>. |
Ionik terbentuk dari [[kation]] (ion positif) dan [[anion]] (ion negatif). Banyak senyawa ionik merupakan senyawa biner, yaitu senyawa yang terbentuk dari hanya dua unsur. Untuk senyawa ionik biner, penamaan dimulai dari kation logam kemudian diikuti anion nonlogam dan diberi akhiran "-ida". Untuk kation yang memiliki lebih dari 1 jenis muatan (bilangan oksidasi), diberi keterangan angka romawi di tengahnya sesuai besarnya muatan<ref name=":0">Chang R.2003. ''General Chemistry: The Essential Concept'', ahli bahasa: Indra Noviandri dkk, 2004, Kimia Dasar Jilid 1. Jakarta: Erlangga</ref>. |
||
[[Berkas:wikiyoen.jpg|ka|300px|jmpl|Contoh penamaan senyawa]] |
[[Berkas:wikiyoen.jpg|ka|300px|jmpl|Contoh penamaan senyawa]] |
||
| Baris 182: | Baris 180: | ||
|} |
|} |
||
=== |
=== Senyawa molekular === |
||
banyak senyawa molekular merupakan senyawa biner. senyawa molekular tersusun atas unsur-unsur non-logam. Penamaan dimulai dari unsur no-logam pertama diikuti nama unsur non-logam yang diberi akhiran -ida. Jika dua unsur non-logam dapat membentuk lebih dari dua jenis senyawa maka digunakan awalan Yunani, suatu awalan yang sesuai dengan indeks dalam rumus kimianya<ref name=":0" />. |
banyak senyawa molekular merupakan senyawa biner. senyawa molekular tersusun atas unsur-unsur non-logam. Penamaan dimulai dari unsur no-logam pertama diikuti nama unsur non-logam yang diberi akhiran -ida. Jika dua unsur non-logam dapat membentuk lebih dari dua jenis senyawa maka digunakan awalan Yunani, suatu awalan yang sesuai dengan indeks dalam rumus kimianya<ref name=":0" />. |
||
* 1 = mono |
* 1 = mono |
||
| Baris 199: | Baris 197: | ||
;Contoh: |
;Contoh: |
||
B<sub>2</sub>H<sub>6</sub> |
B<sub>2</sub>H<sub>6</sub> Diboran |
||
CH<sub>4</sub> [[Metana]] |
CH<sub>4</sub> [[Metana]] |
||
| Baris 213: | Baris 211: | ||
H<sub>2</sub>S Hidrogen sulfida |
H<sub>2</sub>S Hidrogen sulfida |
||
=== |
=== Senyawa Ion Poliatomik === |
||
penamaan dimulai dari ion positif (kation) dilanjutkan dengan ion negatif (anion). |
penamaan dimulai dari ion positif (kation) dilanjutkan dengan ion negatif (anion). |
||
| Baris 305: | Baris 303: | ||
'''Contoh:''' |
'''Contoh:''' |
||
NH4Cl |
NH4Cl amonium klorida |
||
NaNO3 |
NaNO3 natrium nitrat |
||
MgSO4 magnesium sulfat |
MgSO4 magnesium sulfat |
||
KCN kalium sianida |
KCN kalium sianida |
||
Zn(OH)2 seng(II) hidroksida (pada senyawa ini, bilangan oksidasi seng = 2) |
Zn(OH)2 seng(II) hidroksida (pada senyawa ini, bilangan oksidasi seng = 2) |
||
FeC2O4 besi(II) oksalat (pada senyawa ini, bilangan oksidasi besi = 2) |
FeC2O4 besi(II) oksalat (pada senyawa ini, bilangan oksidasi besi = 2) |
||
Fe2(SO4)3 besi(III) sulfat (pada senyawa ini, bilangan oksidasi besi = 3) |
Fe2(SO4)3 besi(III) sulfat (pada senyawa ini, bilangan oksidasi besi = 3) |
||
=== Asam dan Basa === |
=== Asam dan Basa === |
||
| Baris 329: | Baris 327: | ||
==== Penamaan basa ==== |
==== Penamaan basa ==== |
||
''[[Basa]]'' adalah zat yang di dalam air dapat menghasilkan ion OH<sup>–</sup>. Larutan basa bersifat kaustik, artinya jika terkena kulit terasa licin seperti bersabun. Pada umumnya basa adalah senyawa ion yang terdiri dari kation logam dan anion OH–.Senyawa basa dibentuk oleh ion logam sebagai kation dan ion OH– |
''[[Basa]]'' adalah zat yang di dalam air dapat menghasilkan ion OH<sup>–</sup>. Larutan basa bersifat kaustik, artinya jika terkena kulit terasa licin seperti bersabun. Pada umumnya basa adalah senyawa ion yang terdiri dari kation logam dan anion OH–.Senyawa basa dibentuk oleh ion logam sebagai kation dan ion OH– atau ion hidroksida sebagai anion. Penamaan senyawa basa yaitu dengan menuliskan nama logam (kation) di depan kata hidroksida.<ref name=":0" /> |
||
;Contoh |
;Contoh |
||
Revisi per 15 Desember 2018 02.37
Tata nama kimia adalah serangkaian aturan persenyawaan-persenyawaan kimia yang disusun secara sistematis. Tata nama kimia disusun berdasarkan aturan IUPAC (International Union of Pure and Applied Chemistry).
Senyawa Ionik
Ionik terbentuk dari kation (ion positif) dan anion (ion negatif). Banyak senyawa ionik merupakan senyawa biner, yaitu senyawa yang terbentuk dari hanya dua unsur. Untuk senyawa ionik biner, penamaan dimulai dari kation logam kemudian diikuti anion nonlogam dan diberi akhiran "-ida". Untuk kation yang memiliki lebih dari 1 jenis muatan (bilangan oksidasi), diberi keterangan angka romawi di tengahnya sesuai besarnya muatan[1].
| Beberapa Kation Monoatom Umum | |||
| Golongan | Unsur | Nama Ion | Simbol Ion |
| IA | Litium | Kation Litium | Li+ |
| Natrium | Kation Natrium | Na+ | |
| Kalium | Kation Kalium | K+ | |
| IIA | Berilium | Kation Berilium | Be2+ |
| Magnesium | Kation Magnesium | Mg2+ | |
| Kalsium | Kation Kalsium | Ca2+ | |
| Stronsium | Kation Stronsium | Sr2+ | |
| Barium | Kation Barium | Ba2+ | |
| IB | Perak | Kation Perak | Ag+ |
| IIB | Seng | Kation Seng | Zn2+ |
| IIIA | Aluminium | Kation Aluminium | Al3+ |
| Beberapa Anion Monoatom Umum | |||
| Golongan | Unsur | Nama Ion | Simbol Ion |
| VA | Nitrogen | Anion Nitrida | N3- |
| Fosfor | Anion Fosfida | P3- | |
| VIA | Oksigen | Anion Oksida | O2- |
| Belerang | Anion Sulfida | S2- | |
| VIIA | Fluorin | Anion Fluorida | F- |
| Klorin | Anion Klorida | Cl- | |
| Bromin | Anion Bromida | Br- | |
| Iodin | Anion Iodida | I-
| |
| Beberapa Logam Umum yang Memiliki Lebih dari Satu Bilangan Oksidasi | |||
| Golongan | Unsur | Nama Ion | Simbol Ion |
| VIB | Kromium | Krom (II) atau Kromo | Cr2+ |
| Krom (III) atau Kromi | Cr3+ | ||
| VIIB | Mangan | Mangan (II) atau Mangano | Mn2+ |
| Mangan (III) atau Mangani | Mn3+ | ||
| VIIIB | Besi | Besi (II) atau Fero | Fe2+ |
| Besi (III) atau Feri | Fe3+ | ||
| Kobalt | Kobalt (II) atau Kobalto | Co2+ | |
| Kobalt (III) atau Kobaltik | Co3+ | ||
| IB | Tembaga | Tembaga (I) atau Cupro | Cu+ |
| Tembaga (II) atau Cupri | Cu2+ | ||
| IIB | Raksa | Merkuri (I) atau Merkuro | Hg22+ |
| Merkuri (II) atau Merkuri | Hg2+ | ||
| IVA | Timah | Timah (II) atau Stano | Sn2+ |
| Timah (IV) atau Stani | Sn4+ | ||
| Timbal | Timbal (II) atau Plumbum | Pb2+ | |
| Timbal (IV) atau Plumbik | Pb4+
| ||
Senyawa molekular
banyak senyawa molekular merupakan senyawa biner. senyawa molekular tersusun atas unsur-unsur non-logam. Penamaan dimulai dari unsur no-logam pertama diikuti nama unsur non-logam yang diberi akhiran -ida. Jika dua unsur non-logam dapat membentuk lebih dari dua jenis senyawa maka digunakan awalan Yunani, suatu awalan yang sesuai dengan indeks dalam rumus kimianya[1].
- 1 = mono
- 2 = di
- 3 = tri
- 4 = tetra
- 5 = penta
- 6 = heksa
- 7 = hepta
- 8 = okta
- 9 = nona
- 10 = deka
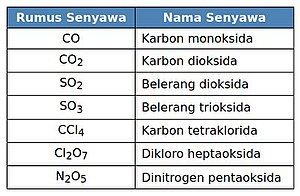
Pengecualian untuk senyawa molekular yang mengandung hidrogen, tidak menggunakan awalan Yunani. di mana senyawa disebut dengan nama umum yang tidak sistematis.[1]
- Contoh
B2H6 Diboran
CH4 Metana
SiH4 Silan
NH3 Amonia
PH3 Fosfin
H2O Air
H2S Hidrogen sulfida
Senyawa Ion Poliatomik
penamaan dimulai dari ion positif (kation) dilanjutkan dengan ion negatif (anion).
untuk ion logam yang memiliki lebih dari satu jenis muatan diberi keterangan angka romawi ditengahnya sesuai besar muatan[2].
| Beberapa Ion Poliatom Penting | |||
| Nama Ion | Simbol Ion | Nama Ion | Simbol Ion |
| Sulfat | SO42- | Hidrogen Fosfat | HPO42- |
| Sulfit | SO32- | Dihidrogen Fosfat | H2PO4- |
| Nitrat | NO3- | Bikarbonat | HCO3- |
| Nitrit | NO2- | Bisulfat | HSO4- |
| Hipoklorit | ClO- | Merkuri (I) | Hg22+ |
| Klorit | ClO2- | Amonia | NH4+ |
| Klorat | ClO3- | Fosfat | PO43- |
| Perklorat | ClO4- | Fosfit | PO33- |
| Asetat | CH3COO- | Permanganat | MnO4- |
| Kromat | CrO42- | Sianida | CN- |
| Dikromat | Cr2O72- | Sianat | OCN- |
| Arsenat | AsO43- | Tiosianat | SCN- |
| Oksalat | C2O42- | Arsenit | AsO33- |
| Tiosulfat | S2O32- | Peroksida | O22- |
| Hidroksida | OH- | Karbonat | CO32-
|
Contoh:
NH4Cl amonium klorida
NaNO3 natrium nitrat
MgSO4 magnesium sulfat
KCN kalium sianida
Zn(OH)2 seng(II) hidroksida (pada senyawa ini, bilangan oksidasi seng = 2)
FeC2O4 besi(II) oksalat (pada senyawa ini, bilangan oksidasi besi = 2)
Fe2(SO4)3 besi(III) sulfat (pada senyawa ini, bilangan oksidasi besi = 3)
Asam dan Basa
Penamaan asam
Untuk asam biner (terdiri dari dua jenis unsur), penamaan dimulai dari kata "asam" diikuti nama sisa asamnya.
Untuk asam yang terdiri dari tiga jenis unsur, penamaan dimulai dari kata "asam" diikuti nama sisa asamnya, yaitu anion poliatom[1]
-
contohnya
Penamaan basa
Basa adalah zat yang di dalam air dapat menghasilkan ion OH–. Larutan basa bersifat kaustik, artinya jika terkena kulit terasa licin seperti bersabun. Pada umumnya basa adalah senyawa ion yang terdiri dari kation logam dan anion OH–.Senyawa basa dibentuk oleh ion logam sebagai kation dan ion OH– atau ion hidroksida sebagai anion. Penamaan senyawa basa yaitu dengan menuliskan nama logam (kation) di depan kata hidroksida.[1]
- Contoh
- NaOH Natrium hidroksida
- Ba(OH)2 Barium hidroksida
- KOH Kalium hidroksida
