Osmosis
Osmosis adalah perpindahan air melalui membran permeabel selektif dari bagian yang lebih encer ke bagian yang lebih pekat. Membran semipermeabel harus dapat ditembus oleh pelarut, tapi tidak oleh zat terlarut, yang mengakibatkan gradien tekanan sepanjang membran. Osmosis merupakan suatu fenomena alami, tapi dapat dihambat secara buatan dengan meningkatkan tekanan pada bagian dengan konsentrasi pekat menjadi melebihi bagian dengan konsentrasi yang lebih encer. Gaya per unit luas yang dibutuhkan untuk mencegah mengalirnya pelarut melalui membran permeabel selektif dan masuk ke larutan dengan konsentrasi yang lebih pekat sebanding dengan tekanan turgor. Tekanan osmotik merupakan sifat koligatif, yang berarti bahwa sifat ini bergantung pada konsentrasi zat terlarut, dan bukan pada sifat zat terlarut itu sendiri.
Osmosis adalah suatu topik yang penting dalam biologi karena fenomena ini dapat menjelaskan mengapa air dapat ditransportasikan ke dalam dan ke luar sel.
Album
- Osmosis
-
Shot of a computer simulation of the process of osmosis
-
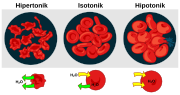
Effect of different solutions on blood cells
-
Plant cell under different environments
Osmosis merupakan difusi air melintasi membran semipermeabel dari daerahdimana air lebih banyak ke daerah dengan air yang lebih sedikit . Osmosis sangatditentukan oleh potensial kimia air atau potensial air , yang menggambarkankemampuan molekul air untuk dapat melakukan difusi. Sejumlah besar volume air akan memiliki kelebihan energi bebas daripada volume yang sedikit, di bawahkondisi yang sama. Energi bebas zuatu zat per unit jumlah, terutama per berat grammolekul (energi bebas mol-1) disebut potensial kimia. Potensial kimia zat terlarutkurang lebih sebanding dengan konsentrasi zat terlarutnya. Zat terlarut yang berdifusicenderung untuk bergerak dari daerah yang berpotensi kimia lebih tinggi menujudaerah yang berpotensial kimia lebih kecil (Ismail, 2006).Osmosis adalah difusi melalui membran semipermeabel. Masuknya larutan kedalam sel-sel endodermis merupakan contoh proses osmosis. Dalam tubuh organismemultiseluler, air bergera dari satu sel ke sel lainnya dengan leluasa. Selain air,molekul-molekul yang berukuran kecil seperti O2 dan CO2 juga mudah melewatimembran sel. Molekul-molekul tersebut akan berdifusi dari daerah dengankonsentrasi tinggi ke konsentrasi rendah. Proses Osmosis akan berhenti jikakonsentrasi zat di kedua sisi membran tersebut telah mencapai keseimbangan(Anonim, 2009).Struktur dinding sel dan membran sel berbeda. Membran memungkinkanmolekul air melintas lebih cepat daripada unsur terlarut; dinding sel primer biasanyasangat permeable terhadap keduanya. Memang membran sel tumbuhanmemungkinkan berlangsungnya osmosis, tapi dinding sel yang tegar itulah yangmenimbulkan tekanan. Sel hewan tidak mempunyai dinding, sehingga bila timbultekanan didalamnya, sel tersebut sering pecah, seperti yang terjadi saat sel darahmerah dimasukkan dalam air. Sel yang turgid banyak berperan dalam menegakkantumbuhan yang tidak berkayu (Salisbury, 1995).Prinsip osmosis: transfer molekul solvent dari lokasi hypotonic (potensirendah) solution menuju hypertonic solution, melewati membran. Jika lokasihypertonic solution kita beri tekanan tertentu, osmosis dapat berhenti, atau malah berbalik arah (reversed osmosis).Besarnya tekanan yang dibutuhkan untuk menghentikan osmosis disebut sebagai osmotic press.Jika dijelaskan sebagai konseptermodinamika, osmosis dapat dianalogikan sebagai proses perubahan entrropi.Komponen solvent murni memiliki entropi rendah, sedangkan komponen berkandunagn solut tinggi memiliki entropi yg tinggi juga. Mengikuti Hukum TermoII: setiap perubahan yang terjadi selalu menuju kondisi entropi maksimum, makasolvent akan mengalir menuju tempat yg mengandung solut lebih banyak, sehinggatotal entropi akhir yang diperoleh akan maksimum.Solvent akan kehilangan entropi,dan solut akan menyerap entropi. "Orang miskin akan semakin miskin, sedang yangkaya akan semakin kaya". Saat kesetimbangan tercapai, entropi akan maksimum, ataugradien (perubahan entropi terhadap waktu) = 0. Ingat: pada titik ekstrim, dS/dt = 0(Wibosono, 2009)