Reaksi penetralan


Reaksi penetralan merupakan reaksi yang terjadi antara asam dan basa. Reaksi asam-basa dalam medium air biasanya menghasilkan garam dan air, yang merupakan senyawa ionik yang terbentuk dari suatu kation selain H+ dan suatu anion selain OH‑ atau O2-.[1]
Asam + basa → garam + air
Semua garam merupakan elektrolit kuat yang berasal dari reaksi antara asam dan basa, karena baik asam maupun basa keduanya merupakan elektrolit kuat, senyawa ini terionisasi sempurna di dalam larutan.
Contoh reaksi antara asam dan basa yang senyawanya terionisasi secara sempurna yaitu:
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O (l)
Jenis-jenis reaksi
Reaksi asam kuat dan basa kuat
Reaksi antara asam kuat dengan basa kuat akan menghasilkan pH larutan yang dihasilkan bersifat netral atau pH = 7.
Contoh reaksi asam basa yang menghasilkan pH netral:
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O (l)
Reaksi asam kuat dan basa lemah
Reaksi antara asam kuat dengan basa lemah akan menghasilkan pH larutan yang dihasilkan bersifat asam atau pH < 7.
Contoh reaksi asam basa yang menghasilkan pH asam:
HCl(aq) + NH3(aq) → NH4Cl(aq)
Reaksi asam lemah dan basa kuat
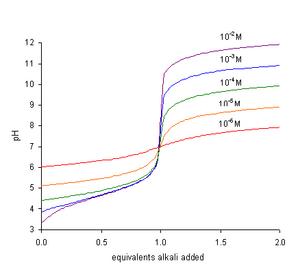
Reaksi antara asam lemah dengan basa kuat akan menghasilkan pH larutan yang di hasilkan bersifat basa atau pH > 7.
Contoh reaksi asam basa yang menghasilkan pH basa:
HC2H3O2(aq) + NaOH(aq) → NaC2H3O2(aq) + H2O (l)
Reaksi asam lemah dan basa lemah
Reaksi antara asam lemah dengan basa lemah akan mengahasilkan pH larutan yang di hasilkan bersifat netral atau pH = 7.[2]
Contoh reaksi asam basa yang menghasilkan pH netral:
HC2H3O2(aq) + NH3(aq) → NH4 C2H3O2(aq)
Reaksi asam dan basa yang sama kekuatannya,akan menghasilkan larutan netral, baik yang reaksi antara asam dan basa yang keduanya kuat maupun keduanya lemah. Reaksi asam dan basa dengan kekuatan yang berlainan akan menghasilkan larutan asam lemah atau basa basa lemah. Jika asam yang dihasilkan itu lebih kuat daripada basa yang dihasilkan, maka diperoleh larutan asam lemah. Sebaliknya jika basa yang dihasilkan lebih kuat dari asam yang dihasilkan, maka di peroleh larutan basa lemah. Terlepas dari kekuatan relative asam dan basa yang terlibatsemua reaksi sam-basa ini merupakan reaksi penetralan.[3]
Aplikasi
Metode titrasi kimia digunakan untuk menganalisis asam atau basa untuk menentukan konsentrasi yang tidak diketahui. Baik pH meter atau indikator pH dapat digunakan untuk menunjukkan titik netralisasi dengan perubahan warna yang berbeda. Perhitungan stoikiometri sederhana dengan volume yang diketahui dari volume yang diketahui dan yang tidak diketahui serta molaritas dari bahan kimia yang ditambahkan memberikan molaritas yang tidak diketahui.
Dalam pengolahan air limbah, metode netralisasi kimia sering diterapkan untuk mengurangi kerusakan yang dapat ditimbulkan oleh limbah setelah dilepaskan ke lingkungan. Untuk kontrol pH, bahan kimia yang populer digunakan termasuk kalsium karbonat, kalsium oksida, magnesium hidroksida, dan natrium bikarbonat. Pemilihan bahan kimia netralisasi yang tepat tergantung pada aplikasi tertentu.
Referensi
- ^ Chang, R. 2004. Kimia Dasar: Konsep-konsep Inti. Jakarta: Erlangga
- ^ Syukri. 1999. Kimia Dasar 2. Bandung: ITB
- ^ Keenan, Kleinfelter dan Wood. 1984. Kimia Untuk Universitas. Jakarta: Erlangga
Bacaan lebih lanjut
Netralisasi tercakup dalam sebagian besar buku teks kimia umum. Ulasan terperinci dapat ditemukan dalam buku teks mengenai kimia analitik seperti
- Skoog, D.A; West, D.M.; Holler, J.F.; Crouch, S.R. (2004). Fundamentals of Analytical Chemistry (edisi ke-8). Thomson Brooks/Cole. ISBN 0-03-035523-0. Bab 14, 15 dan 16
- Aplikasi
- Stumm, W.; Morgan, J.J. (1996). Water Chemistry. New York: Wiley. ISBN 0-471-05196-9.
- Snoeyink, V.L.; Jenkins, D. (1980). Aquatic Chemistry: Chemical Equilibria and Rates in Natural Waters. New York: Wiley. ISBN 0-471-51185-4.
- Millero, F.J. (2006). Chemical Oceanography (edisi ke-3). London: Taylor and Francis. ISBN 0-8493-2280-4.
- Metcalf & Eddy. Wastewater Engineering, Treatment and Reuse. 4th ed. New York: McGraw-Hill, 2003. 526-532.
