Asam sulfonat

Asam benzena sulfonat adalah suatu anggota dari kelas senyawa organosulfur dengan rumus umum R−S(=O)2−OH, di mana R adalah suatu gugus alkil atau aril organik dan gugus S(=O)2−OH merupakan suatu sulfonil hidroksida.[1] Suatu asam sulfonat dapat diibaratkan sebagai asam sulfat dengan satu gugus hidroksil digantikan oleh suatu gugus substituen. Senyawa induk (dengan substituen organik digantikan oleh hidrogen) merupakan senyawa hipotesis asam sulfur. Garam atau ester asam benzena
Preparasi[sunting | sunting sumber]
Asam sulfonat diproduksi melalui proses sulfonasi. Biasanya agen sulfonasi yang digunakan adalah sulfur trioksida. Suatu aplikasi skala sangat besar dari metode ini adalah produksi asam alkilbenzenasulfonat:
- RC6H5 + SO3 → RC6H4SO3H
Dalam reaksi ini, sulfur trioksida merupakan suatu elektrofil dan hidrokarbon aromatik menjalani reaksi substitusi elektrofilik aromatik.[1]
Tiol dapat dioksidasi menjadi asam sulfonat:
- RSH + 3⁄2 O2 → RSO3H
Beberapa asam sulfonat, seperti asam perfluorooktanasulfonat, disiapkan melalui fluorinasi elektrofilik dari asam sulfonat pra-bentuk. Konversi bersih dapat direpresentasikan secara sederhana yaitu:
- C8H17SO3H + 17 F2 → C8F17SO3H + 17 HF
Sifat[sunting | sunting sumber]

Asam sulfonat adalah asam yang jauh lebih kuat dibanding asam karboksilat yang sesuai. Asam p-toluenasulfonat, dengan pKa sebesar −2.8, memiliki keasaman sekitar satu juta kali lebih kuat dari asam benzoat, dengan pKa sebesar 4.2. Serupa dengan itu, asam metanasulfonat, pKa = −1.9, juga memiliki keasaman sekitar satu juta kali lebih kuat dari asam asetat. Karena polaritas mereka, asam sulfonat cenderung berupa padatan kristal. Karena keasaman yang tinggi, asam sulfonat sering larut dalam air atau memperlihatkan sifat seperti-deterjen.
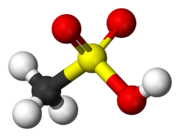
Struktur asam sulfonat diilustrasikan oleh prototipe, asam metanasulfonat. Gugus sulfonat asam, RSO2OH memiliki pusat sulfur tetrahedral, yang berarti bahwa belerang berada di pusat empat atom: tiga atom oksigen dan satu karbon. Geometri keseluruhan pusat sulfur mengingatkan pada bentuk asam sulfat.
Reaksi[sunting | sunting sumber]
Esterifikasi[sunting | sunting sumber]

Asam sulfonat dapat dikonversi ke ester. Kelas senyawa organik ini memiliki rumus umum R−SO2−OR. Ester sulfonat seperti metil triflat dianggap sebagai agen pengalkilasi yang baik dalam sintesis organik. Ester sulfonat semacam ini sering disiapkan melalui alkoholisis pada sulfonil klorida:
- RSO2Cl + R′OH → RSO2OR′ + HCl
Halogenasi[sunting | sunting sumber]
Gugus halida sulfonil terjadi ketika gugus fungsi sulfonil adalah secara tunggal terikat pada atom halogen. Mereka memiliki rumus umum R−SO2−X di mana X adalah halida, hampir selalu klorida. Mereka diproduksi melalui klorinasi asam sulfonat menggunakan tionil klorida dan pereaksi terkait.
Penggantian[sunting | sunting sumber]
Meski ikatan C−SO3H kuat, ikatan (aril)C−SO3 bond dapat dibelah melalui nukleofil tertentu. Signifikansi bersejarah dan berkelanjutan adalah α-sulfonasi dari antrakuinon diikuti oleh pergeseran dari gugus sulfonat melalui nukleofil lainnya, yang tidak bisa dipasang secara langsung.[2] Sebuah metode awal untuk memproduksi fenol melibatkan hidrolisis basa pada natrium benzenasulfonat, yang dapat dihasilkan dengan mudah dari benzena.[3]
- C6H5SO3Na + 2 NaOH → C6H5OH + Na2SO3 + H2O
Aplikasi[sunting | sunting sumber]
Meskipun baik asam alkil dan aril sulfonat diketahui, sebagian besar aplikasi berhubungan dengan derivat aromatik.
Deterjen dan surfaktan[sunting | sunting sumber]

Deterjen dan surfaktan merupakan molekul yang menggabungkan gugus yang sangat nonpolar dan sangat polar. Secara tradisional, sabun adalah surfaktan populer, yang berasal dari asam lemak. Sejak pertengahan abad ke-20, penggunaan asam sulfonat telah melampaui sabun dalam masyarakat maju. Sebagai contoh, diperkirakan 2 miliar kilogram alkilbenzenasulfonat yang dihasilkan setiap tahunnya untuk tujuan yang beragam. Lignin sulfonat, diproduksi oleh sulfonasi dari lignin merupakan komponen cairan pengeboran dan aditif dalam jenis beton tertentu.[4]
Bahan pewarna[sunting | sunting sumber]
Banyak jika sebagian besar pewarna antrakuinon diproduksi atau diproses melalui sulfonasi.[2] Asam sulfonat cenderung mengikat erat protein dan karbohidrat. Kebanyakan pewarna "yang dapat dicuci" adalah asam sulfonat (atau memiliki gugus fungsional sulfonil di dalamnya) karena alasan ini. Asam p-kresidinsulfonat digunakan untuk membuat pewarna makanan.
Katalis asam[sunting | sunting sumber]

Sebagai asam kuat, asam sulfonat juga digunakan sebagai katalis. Contoh yang sederhana adalah asam metanasulfonat, CH3SO2OH dan asam p-toluenasulfonat, yang biasanya digunakan dalam kimia organik dalam bentuk asam yang lipofilik (larut dalam pelarut organik). Asam sulfonat polimerik juga berguna. Resin Dowex adalah turunan asam sulfonat dari polistirena dan digunakan sebagai katalis dan untuk pertukaran ion (pelunakan air). Nafion, asam sulfonat polimerik terfluorinasi adalah komponen dari membran pertukaran proton dalam sel bahan bakar.[5]
Obat-obatan[sunting | sunting sumber]
Obat-obatan antibakteri seperti obat sulfa diproduksi dari asam sulfonat.
Baterai alir[sunting | sunting sumber]
Asam metanasulfonat digunakan sebagai elektrolit pendukung pada baterai alir seng-cerium dan timbal-asam (metanasulfonat).
Referensi[sunting | sunting sumber]
- ^ a b Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (edisi ke-6), New York: Wiley-Interscience, ISBN 0-471-72091-7
- ^ a b Hans-Samuel Bien, Josef Stawitz, Klaus Wunderlich “Anthraquinone Dyes and Intermediates” Ullmann's Encyclopedia of Industrial Chemistry 2002 Wiley-VCH, Weinhem. doi:10.1002/14356007.a02_355
- ^ Manfred Weber, Markus Weber, Michael Kleine-Boymann "Phenol" in Ullmann's Encyclopedia of Industrial Chemistry 2004, Wiley-VCH. doi:10.1002/14356007.a19_299.pub2.
- ^ Kosswig, K. “Surfactants” in Ullmann’s Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a25_747.
- ^ Guido Busca "Acid Catalysts in Industrial Hydrocarbon Chemistry" Chem. Rev. 2007, 107, 5366-5410. doi:10.1021/cr068042e
Bacaan lebih lanjut[sunting | sunting sumber]
- J.A. Titus, R. Haugland, S.O. Sharrow and D.M. Segal, Texas red, a hydrophilic, red-emitting fluorophore for use with fluorescein in dual parameter flow microfluorometric and fluorescence microscopic studies. J. Immunol. Methods 50 (1982), pp. 193–204. doi:10.1016/0022-1759(82)90225-3
- C. Lefevre, H.C. Kang, R.P. Haugland, N. Malekzadeh, S. Arttamangkul, and R. P. Haugland, Texas Red-X and Rhodamine Red-X, New Derivatives of Sulforhodamine 101 and Lissamine Rhodamine B with Improved Labeling and Fluorescence Properties, Bioconj. Chem. 1996, 7(4):482-9 DOI:10.1021/bc960034p
