Valsartan: Perbedaan antara revisi
k Bot: Perubahan kosmetika |
Tidak ada ringkasan suntingan Tag: Suntingan perangkat seluler Suntingan peramban seluler Suntingan seluler lanjutan |
||
| (10 revisi perantara oleh 6 pengguna tidak ditampilkan) | |||
| Baris 1: | Baris 1: | ||
{{Infobox drug |
|||
'''Valsartan''' merupakan obat golongan ''[[Angiotensin Receptor Blocker]]'' (ARB) yang bekerja dengan menghambat reseptor angiotensin II yang menyebabkan terjadinya penurunan tekanan darah pada pasien dengan [[hipertensi]]. Valsartan termasuk obat keras sehingga harus dikonsumsi dengan resep dokter. Valsartan dapat dikonsumsi tunggal maupun kombinasi dengan obat-obatan antihipertensi lain. Namun, penggunaan bersama [[Inhibitor ACE|ACE inhibitor]] dan golongan [[Beta blocker|Beta Blocker]] tidak dianjurkan.<ref>{{Cite journal|last=Huang|first=Qi-Fang|last2=Li|first2=Yan|last3=Wang|first3=Ji-Guang|date=2013-12-30|title=Overview of clinical use and side effect profile of valsartan in Chinese hypertensive patients|url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3883632/|journal=Drug Design, Development and Therapy|volume=8|pages=79–86|doi=10.2147/DDDT.S38617|issn=1177-8881|pmc=3883632|pmid=24403822}}</ref> |
|||
| verifiedrevid = 470628341 |
|||
| image = Valsartan skeletal.svg |
|||
| width = |
|||
| alt = |
|||
| image2 = Valsartan-from-xtal-3D-bs-17.png |
|||
| width2 = |
|||
| alt2 = |
|||
| caption = |
|||
<!-- Clinical data --> |
|||
Valsartan dengan rumus kimia <chem>C24H29N5O3</chem> dikembangkan oleh [[Novartis]] dan dipasarkan di beberapa negara berkembang dengan merek dagang Diovan.<ref>{{Cite web|url=https://www.japsonline.com/admin/php/uploads/54_pdf.pdf|title=|last=|first=|date=|website=|access-date=}}</ref> Nama dagang Valsartan di Indonesia antara lain Co Diovan, Diovan, Exforge, Valesco, dan Valsartan Ni.<ref>{{Cite web|url=http://pionas.pom.go.id/monografi/valsartan|title=VALSARTAN {{!}} PIO Nas|website=pionas.pom.go.id|access-date=2019-11-14}}</ref> Valsartan diserap dengan baik pada pemberian secara oral dan diekskresikan melalui urin dan feses masing-masing sekitar 13% dan 86%.<ref>{{Cite web|url=https://reference.medscape.com/drug/entresto-sacubitril-valsartan-1000010#91|title=Entresto (sacubitril/valsartan) dosing, indications, interactions, adverse effects, and more|website=reference.medscape.com|access-date=2019-11-14}}</ref> |
|||
| pronounce = |
|||
| tradename = Diovan, dll |
|||
| Drugs.com = {{drugs.com|monograph|valsartan}} |
|||
| MedlinePlus = a697015 |
|||
| DailyMedID = Valsartan |
|||
| pregnancy_AU = D |
|||
| pregnancy_AU_comment = <ref name="Drugs.com pregnancy">{{cite web | title=Valsartan Use During Pregnancy | website=Drugs.com | date=28 March 2019 | url=https://www.drugs.com/pregnancy/valsartan.html | access-date=12 February 2020}}</ref> |
|||
| pregnancy_category = |
|||
| routes_of_administration = [[Oral (rute pemberian obat)|Oral]] |
|||
| class = [[Angiotensin II receptor antagonist]] |
|||
| ATCvet = |
|||
| ATC_prefix = C09 |
|||
| ATC_suffix = CA03 |
|||
| ATC_supplemental = {{ATC|C09|DX05}}, {{ATC|C09|DA03}}, {{ATC|C09|DX02}}, {{ATC|C09|DX01}}, {{ATC|C09|DB08}}, {{ATC|C09|DB01}}, {{ATC|C09|DX04}}, {{ATC|C10|BX10}} |
|||
<!-- Legal status --> |
|||
| legal_AU = S4 |
|||
| legal_AU_comment = <ref>{{cite web | title=Diovan valsartan 40mg film-coated tablet blister pack | website=Therapeutic Goods Administration (TGA) | url=https://tga-search.clients.funnelback.com/s/search.html?collection=tga-artg&profile=record&meta_i=93165 | access-date=24 October 2021 | archive-date=25 October 2021 | archive-url=https://web.archive.org/web/20211025160457/https://tga-search.clients.funnelback.com/s/search.html?collection=tga-artg&profile=record&meta_i=93165 | url-status=dead }}</ref><ref>{{cite web | title=Diovan valsartan 80mg film-coated tablet blister pack | website=Therapeutic Goods Administration (TGA) | url=https://tga-search.clients.funnelback.com/s/search.html?collection=tga-artg&profile=record&meta_i=80868 | access-date=24 October 2021 | archive-date=25 October 2021 | archive-url=https://web.archive.org/web/20211025160419/https://tga-search.clients.funnelback.com/s/search.html?collection=tga-artg&profile=record&meta_i=80868 | url-status=dead }}</ref><ref>{{cite web | title=Diovan valsartan 160mg film-coated tablet blister pack | website=Therapeutic Goods Administration (TGA) | url=https://tga-search.clients.funnelback.com/s/search.html?collection=tga-artg&profile=record&meta_i=80871 | access-date=24 October 2021 | archive-date=25 October 2021 | archive-url=https://web.archive.org/web/20211025160608/https://tga-search.clients.funnelback.com/s/search.html?collection=tga-artg&profile=record&meta_i=80871 | url-status=dead }}</ref> |
|||
| legal_BR = <!-- OTC, A1, A2, A3, B1, B2, C1, C2, C3, C4, C5, D1, D2, E, F--> |
|||
| legal_BR_comment = |
|||
| legal_CA = <!-- OTC, Rx-only, Schedule I, II, III, IV, V, VI, VII, VIII --> |
|||
| legal_CA_comment = |
|||
| legal_DE = <!-- Anlage I, II, III or Unscheduled--> |
|||
| legal_DE_comment = |
|||
| legal_NZ = <!-- Class A, B, C --> |
|||
| legal_NZ_comment = |
|||
| legal_UK = POM |
|||
| legal_UK_comment = <ref>{{cite web | title=Valsartan 160 mg capsules - Summary of Product Characteristics (SmPC) | website=(emc) | date=19 February 2019 | url=https://www.medicines.org.uk/emc/medicine/30901 | access-date=12 February 2020 | archive-date=13 February 2020 | archive-url=https://web.archive.org/web/20200213034657/https://www.medicines.org.uk/emc/medicine/30901 | url-status=dead }}</ref> |
|||
| legal_US = Rx-only |
|||
| legal_US_comment = <ref name="Diovan FDA label" /> |
|||
| legal_UN = <!-- N I, II, III, IV / P I, II, III, IV--> |
|||
| legal_UN_comment = |
|||
| legal_status = <!--For countries not listed above--> |
|||
<!-- Pharmacokinetic data --> |
|||
| bioavailability = 25% |
|||
| protein_bound = 95% |
|||
| metabolism = |
|||
| metabolites = |
|||
| onset = |
|||
| elimination_half-life = 6 jam |
|||
| duration_of_action = |
|||
| excretion = [[Ginjal]] 30%, [[saluran empedu]] 70% |
|||
<!-- Identifiers --> |
|||
| index_label = <!-- parent --> |
|||
| index2_label = tritiated |
|||
| CAS_number_Ref = {{cascite|correct|??}} |
|||
| CAS_number = 137862-53-4 |
|||
| CAS_supplemental = |
|||
| PubChem = 60846 |
|||
| IUPHAR_ligand = 3937 |
|||
| IUPHAR_ligand2 = 593 |
|||
| DrugBank_Ref = {{drugbankcite|correct|drugbank}} |
|||
| DrugBank = DB00177 |
|||
| ChemSpiderID_Ref = {{chemspidercite|correct|chemspider}} |
|||
| ChemSpiderID = 54833 |
|||
| UNII_Ref = {{fdacite|correct|FDA}} |
|||
| UNII = 80M03YXJ7I |
|||
| KEGG_Ref = {{keggcite|correct|kegg}} |
|||
| KEGG = D00400 |
|||
| ChEBI_Ref = {{ebicite|correct|EBI}} |
|||
| ChEBI = 9927 |
|||
| ChEMBL_Ref = {{ebicite|correct|EBI}} |
|||
| ChEMBL = 1069 |
|||
| NIAID_ChemDB = |
|||
| PDB_ligand = |
|||
| synonyms = |
|||
<!-- Chemical and physical data --> |
|||
| IUPAC_name = (''S'')-3-metil-2-(''N''-<nowiki/>{[2'-(2''H''-1,2,3,4-tetrazol-5-il)bifenil-4-il]metil}pentanamido)asam butanoat |
|||
| C=24 | H=29 | N=5 | O=3 |
|||
| SMILES = CCCCC(=O)N(Cc1ccc(-c2ccccc2-c2nn[nH]n2)cc1)C(C(=O)O)C(C)C |
|||
| StdInChI_Ref = {{stdinchicite|correct|chemspider}} |
|||
| StdInChI = 1S/C24H29N5O3/c1-4-5-10-21(30)29(22(16(2)3)24(31)32)15-17-11-13-18(14-12-17)19-8-6-7-9-20(19)23-25-27-28-26-23/h6-9,11-14,16,22H,4-5,10,15H2,1-3H3,(H,31,32)(H,25,26,27,28)/t22-/m0/s1 |
|||
| StdInChIKey_Ref = {{stdinchicite|correct|chemspider}} |
|||
| StdInChI_comment = |
|||
| StdInChIKey = ACWBQPMHZXGDFX-QFIPXVFZSA-N |
|||
| density = |
|||
| density_notes = |
|||
| melting_point = |
|||
| melting_high = |
|||
| melting_notes = |
|||
| boiling_point = |
|||
| boiling_notes = |
|||
| solubility = |
|||
| sol_units = |
|||
| specific_rotation = |
|||
}} |
|||
'''Valsartan''' merupakan obat golongan [[Antagonis reseptor angiotensin II|ARB]] yang bekerja dengan menghambat reseptor angiotensin II yang menyebabkan terjadinya penurunan tekanan darah pada pasien dengan [[hipertensi]]. Valsartan termasuk obat keras sehingga harus dikonsumsi dengan resep dokter. Valsartan dapat dikonsumsi tunggal maupun kombinasi dengan obat-obatan antihipertensi lain. Namun, penggunaan bersama [[Inhibitor ACE|ACE inhibitor]] dan golongan [[Beta blocker|Beta Blocker]] tidak dianjurkan.<ref>{{Cite journal|last=Huang|first=Qi-Fang|last2=Li|first2=Yan|last3=Wang|first3=Ji-Guang|date=2013-12-30|title=Overview of clinical use and side effect profile of valsartan in Chinese hypertensive patients|url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3883632/|journal=Drug Design, Development and Therapy|volume=8|pages=79–86|doi=10.2147/DDDT.S38617|issn=1177-8881|pmc=3883632|pmid=24403822}}</ref> |
|||
Valsartan dengan rumus kimia <chem>C24H29N5O3</chem> dikembangkan oleh [[Novartis]] dan dipasarkan di beberapa negara berkembang dengan merek dagang Diovan.<ref>{{Cite web|url=https://www.japsonline.com/admin/php/uploads/54_pdf.pdf|title=|last=|first=|date=|website=|access-date=}}</ref> Nama dagang Valsartan di Indonesia antara lain Co Diovan, Diovan, Exforge, Valesco, dan Valsartan Ni.<ref>{{Cite web|url=http://pionas.pom.go.id/monografi/valsartan|title=VALSARTAN {{!}} PIO Nas|website=pionas.pom.go.id|access-date=2019-11-14|archive-date=2020-01-07|archive-url=https://web.archive.org/web/20200107055044/http://pionas.pom.go.id/monografi/valsartan|dead-url=yes}}</ref> Valsartan diserap dengan baik pada pemberian secara oral dan diekskresikan melalui urin dan feses masing-masing sekitar 13% dan 86%.<ref>{{Cite web|url=https://reference.medscape.com/drug/entresto-sacubitril-valsartan-1000010#91|title=Entresto (sacubitril/valsartan) dosing, indications, interactions, adverse effects, and more|website=reference.medscape.com|access-date=2019-11-14}}</ref> |
|||
Menurut Badan Pengawasan Obat dan Makanan Amerika ([[Badan Pengawas Obat dan Makanan Amerika Serikat|FDA]]), Valsartan termasuk obat-obatan kategori D artinya terbukti berisiko terhadap janin. Namun dapat diberikan jika manfaat yang diperoleh lebih besar daripada risiko. Penggunaan pada ibu hamil tidak direkomendasikan karena dapat menyebabkan [[oligohidramnion]] yang dapat mengakibatkan kematian janin. |
Menurut Badan Pengawasan Obat dan Makanan Amerika ([[Badan Pengawas Obat dan Makanan Amerika Serikat|FDA]]), Valsartan termasuk obat-obatan kategori D artinya terbukti berisiko terhadap janin. Namun dapat diberikan jika manfaat yang diperoleh lebih besar daripada risiko. Penggunaan pada ibu hamil tidak direkomendasikan karena dapat menyebabkan [[oligohidramnion]] yang dapat mengakibatkan kematian janin. |
||
Efek samping |
Efek samping yang timbul akibat penggunaan Valsartan antara lain hipotensi ortostatik, ruam, hiperkalemia, gangguan saluran pernapasan, dispneu, diare, mual, muntah, dispepsia, dan impotensi. Valsartan tidak diberikan pada pasien dengan kegagalan fungsi hati berat, sirosis hati, dan obstruksi empedu.<ref>{{Cite web|url=http://www.fda.gov/news-events/press-announcements/fda-approves-new-generic-valsartan|title=FDA approves a new generic valsartan|last=Commissioner|first=Office of the|date=2019-09-11|website=FDA|language=en|access-date=2019-11-14}}</ref> |
||
Pada tahun 2018, telah dilakukan penarikan obat antihipertensi berbahan aktif Valsartan karena ditemukan adanya cemaran ''[[Nitrosodimethylamine]]'' (NDMA) yang bersifat karsinogenik pada penggunaan jangka panjang.<ref>{{Cite web|url=https://www.pom.go.id/new/view/more/klarifikasi/88/PENJELASAN-BPOM-RI--TENTANG--PENARIKAN-OBAT-ANTIHIPERTENSI-YANG-MENGANDUNG-ZAT-AKTIF-VALSARTAN.html|title=PENJELASAN BPOM RI TENTANG PENARIKAN OBAT ANTIHIPERTENSI YANG MENGANDUNG ZAT AKTIF VALSARTAN|last=|first=|date=|website=|access-date=}}</ref> |
Pada tahun 2018, telah dilakukan penarikan obat antihipertensi berbahan aktif Valsartan karena ditemukan adanya cemaran ''[[Nitrosodimethylamine]]'' (NDMA) yang bersifat karsinogenik pada penggunaan jangka panjang.<ref>{{Cite web|url=https://www.pom.go.id/new/view/more/klarifikasi/88/PENJELASAN-BPOM-RI--TENTANG--PENARIKAN-OBAT-ANTIHIPERTENSI-YANG-MENGANDUNG-ZAT-AKTIF-VALSARTAN.html|title=PENJELASAN BPOM RI TENTANG PENARIKAN OBAT ANTIHIPERTENSI YANG MENGANDUNG ZAT AKTIF VALSARTAN|last=|first=|date=|website=|access-date=}}</ref> |
||
== Referensi == |
== Referensi == |
||
{{reflist}} |
{{reflist}} |
||
[[Kategori: |
[[Kategori:Bifenil]] |
||
[[Kategori:Antihipertensi]] |
|||
[[Kategori:Obat Esensial Nasional Indonesia]] |
|||
[[Kategori:Antagonis reseptor angiotensin II]] |
|||
[[Kategori:Karboksamida]] |
|||
[[Kategori:Asam karboksilat]] |
|||
[[Kategori:Tetrazola]] |
|||
[[Kategori:Obat yang dikembangkan oleh Novartis]] |
|||
Revisi terkini sejak 22 September 2024 08.44
| |
|---|---|

| |
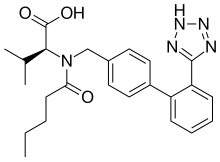
| Nama sistematis (IUPAC) | |
| (S)-3-metil-2-(N-{[2'-(2H-1,2,3,4-tetrazol-5-il)bifenil-4-il]metil}pentanamido)asam butanoat | |
| Data klinis | |
| Nama dagang | Diovan, dll |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a697015 |
| Data lisensi | US Daily Med:pranala |
| Kat. kehamilan | D(AU) |
| Status hukum | Harus dengan resep dokter (S4) (AU) POM (UK) ℞-only (US) |
| Rute | Oral |
| Data farmakokinetik | |
| Bioavailabilitas | 25% |
| Ikatan protein | 95% |
| Waktu paruh | 6 jam |
| Ekskresi | Ginjal 30%, saluran empedu 70% |
| Pengenal | |
| Nomor CAS | 137862-53-4 |
| Kode ATC | C09CA03 C09DX05, C09DA03, C09DX02, C09DX01, C09DB08, C09DB01, C09DX04, C10BX10 |
| PubChem | CID 60846 |
| Ligan IUPHAR | 3937 |
| DrugBank | DB00177 |
| ChemSpider | 54833 |
| UNII | 80M03YXJ7I |
| KEGG | D00400 |
| ChEBI | CHEBI:9927 |
| ChEMBL | CHEMBL1069 |
| Data kimia | |
| Rumus | C24H29N5O3 |
| |
Valsartan merupakan obat golongan ARB yang bekerja dengan menghambat reseptor angiotensin II yang menyebabkan terjadinya penurunan tekanan darah pada pasien dengan hipertensi. Valsartan termasuk obat keras sehingga harus dikonsumsi dengan resep dokter. Valsartan dapat dikonsumsi tunggal maupun kombinasi dengan obat-obatan antihipertensi lain. Namun, penggunaan bersama ACE inhibitor dan golongan Beta Blocker tidak dianjurkan.[1]
Valsartan dengan rumus kimia dikembangkan oleh Novartis dan dipasarkan di beberapa negara berkembang dengan merek dagang Diovan.[2] Nama dagang Valsartan di Indonesia antara lain Co Diovan, Diovan, Exforge, Valesco, dan Valsartan Ni.[3] Valsartan diserap dengan baik pada pemberian secara oral dan diekskresikan melalui urin dan feses masing-masing sekitar 13% dan 86%.[4]
Menurut Badan Pengawasan Obat dan Makanan Amerika (FDA), Valsartan termasuk obat-obatan kategori D artinya terbukti berisiko terhadap janin. Namun dapat diberikan jika manfaat yang diperoleh lebih besar daripada risiko. Penggunaan pada ibu hamil tidak direkomendasikan karena dapat menyebabkan oligohidramnion yang dapat mengakibatkan kematian janin.
Efek samping yang timbul akibat penggunaan Valsartan antara lain hipotensi ortostatik, ruam, hiperkalemia, gangguan saluran pernapasan, dispneu, diare, mual, muntah, dispepsia, dan impotensi. Valsartan tidak diberikan pada pasien dengan kegagalan fungsi hati berat, sirosis hati, dan obstruksi empedu.[5]
Pada tahun 2018, telah dilakukan penarikan obat antihipertensi berbahan aktif Valsartan karena ditemukan adanya cemaran Nitrosodimethylamine (NDMA) yang bersifat karsinogenik pada penggunaan jangka panjang.[6]
Referensi
[sunting | sunting sumber]- ^ Huang, Qi-Fang; Li, Yan; Wang, Ji-Guang (2013-12-30). "Overview of clinical use and side effect profile of valsartan in Chinese hypertensive patients". Drug Design, Development and Therapy. 8: 79–86. doi:10.2147/DDDT.S38617. ISSN 1177-8881. PMC 3883632
 . PMID 24403822.
. PMID 24403822.
- ^ (PDF) https://www.japsonline.com/admin/php/uploads/54_pdf.pdf. Tidak memiliki atau tanpa
|title=(bantuan) - ^ "VALSARTAN | PIO Nas". pionas.pom.go.id. Diarsipkan dari versi asli tanggal 2020-01-07. Diakses tanggal 2019-11-14.
- ^ "Entresto (sacubitril/valsartan) dosing, indications, interactions, adverse effects, and more". reference.medscape.com. Diakses tanggal 2019-11-14.
- ^ Commissioner, Office of the (2019-09-11). "FDA approves a new generic valsartan". FDA (dalam bahasa Inggris). Diakses tanggal 2019-11-14.
- ^ "PENJELASAN BPOM RI TENTANG PENARIKAN OBAT ANTIHIPERTENSI YANG MENGANDUNG ZAT AKTIF VALSARTAN".

