Elektrolisis: Perbedaan antara revisi
Tidak ada ringkasan suntingan |
|||
| (58 revisi perantara oleh 33 pengguna tidak ditampilkan) | |||
| Baris 1: | Baris 1: | ||
{{wikify}} |
|||
{{unreferenced}} |
{{unreferenced}} |
||
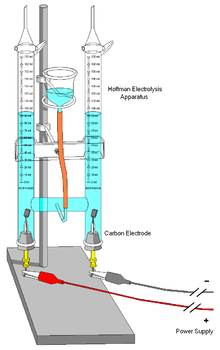
[[File:Electrolysis Apparatus.png|thumb|Ilustrasi [[Voltameter Hofmann|Alat elektrolisis Hofmann]] yang seringkali digunakan di laboratorium sekolah]] |
|||
'''Elektrolisis''' adalah penguraian suatu elektrolit oleh arus listrik. Pada sel elektrolisis. Reaksi |
|||
'''Elektrolisis''' adalah [[penguraian]] suatu [[elektrolit]] oleh [[arus listrik]] pada sel elektrolisis<ref>{{Cite web|last=Author|date=22 Oktober 2022|title=Sel Elektrolisis – Pengertian, Reaksi, Contoh Soal dan Pembahasan|url=https://www.zenius.net/blog/sel-elektrolisis|website=zenius|access-date=18 Desember 2023}}</ref>. [[Reaksi kimia]] akan terjadi jika [[Arus listrik|arus]] listrik dialirkan melalui [[Elektrolit|larutan elektrolit]], yaitu energi listrik (arus listrik) diubah menjadi energi kimia ([[Redoks|reaksi redoks]]). Tiga ciri utama, yaitu: |
|||
kimia akan terjadi jika arus listrik dialirkan melalui larutan elektrolit, yaitu energi listrik (arus listrik) |
|||
| ⚫ | |||
diubah menjadi energi kimia (reaksi redoks). Tiga ciri utama, yaitu: |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | [[Elektrode]] yang menerima elektron dari sumber arus listrik luar disebut [[katode]], sedangkan elektrode yang mengalirkan elektron kembali ke sumber arus listrik luar disebut [[anode]]. Katode adalah tempat terjadinya reaksi reduksi yang elektrodanya negatif (-) dan anode adalah tempat terjadinya reaksi [[oksidasi]] yang elektrodanya positif (+). |
||
| ⚫ | |||
==Etimologi== |
|||
Kata "elektrolisis" diperkenalkan oleh [[Michael Faraday]] pada tahun 1834,<ref>{{cite journal |last1=Oesper |first1=Ralph |last2=Speter |first2=Max |title=The Faraday-Whewell correspondence concerning electro-chemical terms |journal=The Scientific Monthly |date=1937 |volume=45 |issue=6 |pages=535–546|bibcode=1937SciMo..45..535O }}</ref> menggunakan kata [[bahasa Yunani]] ἤλεκτρον ({{IPA-grc|ɛ̌ːlektron}}) "amber", yang sejak abad ke-17 diasosiasikan dengan fenomena kelistrikan, dan λύσις ({{IPA-grc|lýsis}}) yang berarti "pelarutan". Namun demikian, elektrolisis, sebagai alat untuk mempelajari reaksi kimia dan mendapatkan elemen murni, mendahului penggunaan istilah dan deskripsi formal oleh Faraday. |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
C (Coulomb) adalah satuan muatan listrik, dan 1 C adalah muatan yang dihasilkan bila arus 1 A (Ampere) mengalir selama 1 |
C ([[Coulomb]]) adalah satuan muatan listrik, dan 1 C adalah muatan yang dihasilkan bila arus 1 A ([[Ampere]]) mengalir selama 1 detik. Tetapan fundamental listrik adalah [[konstanta Faraday]], F = 9,65 x10<sup>4</sup> C, yang didefinisikan sebagai kuantitas listrik yang dibawa oleh 1 [[mol]] elektron. Dimungkinkan untuk menghitung kuantitas [[mol]] perubahan kimia yang disebabkan oleh aliran arus listrik yang tetap mengalir untuk rentang waktu tertentu. |
||
Hantaran listrik melalui larutan elektrolit dapat dianggap sebagai aliran |
Hantaran listrik melalui larutan [[elektrolit]] dapat dianggap sebagai aliran elektron. Jadi, apabila [[elektron]] telah dapat mengalir dalam larutan elektrolit berarti listrik dapat mengalir dalam larutan tersebut. Elektron berasal dari kutub katode atau [[kutub negatif]]. Sedangkan pada anode melepaskan ion positif dan membentuk endapan pada logam katode. Di dalam larutan terurai proses: |
||
CuSO<sub>4</sub> → Cu<sup>2+</sup> + SO<sub>4</sub><sup>2-</sup> |
|||
Ion [[Tembaga|Cu<sup>2+</sup>]] ini akan berpindah menuju keping katode sedangkan ion SO<sub>4</sub><sup>2-</sup> akan menuju keping anode. Lama-lama keping katode ini akan timbul [[Reaksi pengendapan|endapan]] dan terjadi perubahan [[massa]]. Massa ini dapat dihitung dengan cara: |
|||
G = a . I . t |
G = a . I . t |
||
Di mana: |
|||
Dimana: |
|||
G = jumlah endapan tembaga Cu (gram) |
G = jumlah endapan tembaga [[Tembaga|Cu]] (gram) |
||
a = tara kimia listrik (gr/ampere.jam) |
a = tara kimia listrik (gr/ampere.jam) |
||
| Baris 32: | Baris 36: | ||
I = G/at |
I = G/at |
||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | Sel elektrolisis banyak digunakan dalam industri pembuatan [[gas]] misalnya pembuatan gas [[oksigen]], gas [[hidrogen]], atau gas [[klorin]]. Untuk menghasilkan gas oksigen dan hidrogen, Anda dapat menggunakan larutan elektrolit dari [[kation]] golongan I A, (K<sup>+</sup>, Na<sup>+</sup>), golongan II A, (Ca<sup>2+</sup>, Mg<sup>2+</sup>), Al<sup>3+</sup>, Mn<sup>2+</sup>, dan [[anion]] yang mengandung oksigen (SO<sub>4</sub><sup>2-</sup>, CO<sub>3</sub><sup>2-</sup>, NO<sub>3</sub><sup>-</sup>, PO<sub>4</sub><sup>3-</sup>, ClO<sub>4</sub><sup>-</sup>) dengan elektrode Pt atau [[karbon]]. Reaksi elektrolisis yang menghasilkan gas, misalnya elektrolisis larutan Na<sub>2</sub>SO<sub>4</sub> menggunakan [[elektrode karbon]]. |
||
| ⚫ | |||
| ⚫ | Sel elektrolisis banyak digunakan dalam industri pembuatan gas misalnya pembuatan gas oksigen, gas |
||
Reaksi yang terjadi |
Reaksi yang terjadi: |
||
Na<sub>2</sub>SO<sub>4(aq)</sub> → 2 Na<sup>+</sup><sub>(aq)</sub> + SO<sub>4</sub><sup>2-</sup><sub>(aq)</sub> |
|||
Katode (C): 2 H<sub>2</sub>O<sub>(l)</sub> + 2e<sup>-</sup> → 2 OH<sup>-</sup><sub>(aq)</sub> + H<sub>2(g)</sub> |
|||
Anode (C): 2 H<sub>2</sub>O<sub>(l)</sub> → 4 H<sup>+</sup><sub>(aq)</sub> + O<sub>2(g)</sub> + 4e<sup>-</sup> |
|||
Na2SO4 (aq) 2Na+ (aq) + SO42- |
|||
| ⚫ | Karena pada katode dan anode yang bereaksi adalah air, semakin lama air semakin berkurang sehingga perlu ditambahkan. Perlu diingat bahwa walaupun yang bereaksi adalah air, tidak berarti elektrolit Na<sub>2</sub>SO<sub>4</sub> tidak diperlukan. Elektrolit ini berguna sebagai penghantar arus listrik. |
||
Katode (C) : 2H2O (l) +2e- 2OH- (aq) +H2 (g) |
|||
| ⚫ | |||
Anode (C) : 2H2O (l) 4e- + 4H+ +O2 (g) |
|||
| ⚫ | [[Penyepuhan]] suatu logam [[emas]], [[perak]], atau [[nikel]], bertujuan menutupi logam yang penampilannya kurang baik atau menutupi logam yang mudah berkarat. Logam-logam ini dilapisi dengan logam lain yang penampilan dan daya tahannya lebih baik agar tidak berkarat. Misalnya mesin kendaraan bermotor yang terbuat dari baja umumnya dilapisi [[kromium]] agar terhindar dari [[korosi]]. Beberapa alat rumah tangga juga disepuh dengan perak sehingga lebih awet dan penampilannya tampak lebih baik. Badan sepede [[titanium]] dilapisi titanium oksida (TiO<sub>2</sub>) yang bersifat keras dan tidak dapat ditembus oleh [[oksigen]] atau [[uap air]] sehingga terhindar dari reaksi oksida yang menyebabkan korosi. Prinsip kerja proses penyepuhan adalah penggunaan sel dengan elektrolit larutan dan elektrode reaktif. Contoh jika logam atau cincin dari besi akan dilapisi emas digunakan larutan elektrolit AuCl<sub>3</sub><sub>(aq)</sub>. [[Logam besi (Fe)]] dijadikan sebagai katode, sedangkan logam emasnya (Au) sebagai anode. Reaksi yang berlangsung dalam proses penyepuhan besi dengan emas yaitu: |
||
AuCl<sub>3</sub><sub>(aq)</sub> = Au<sup>3+</sup><sub>(aq)</sub> + 3 Cl<sup>-</sup><sub>(aq)</sub> |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | Penyepuhan suatu logam emas, perak, atau nikel, bertujuan menutupi logam yang penampilannya kurang baik atau menutupi logam yang mudah berkarat. Logam-logam ini |
||
Anode (Au): Au<sub>(s)</sub> = Au<sup>3+</sup><sub>(aq)</sub> + 3e<sup>-</sup> |
|||
AuCl3 (aq) Au3+ (aq) + 3Cl- (aq) |
|||
| ⚫ | Proses yang terjadi yaitu oksidasi logam emas (anode) menjadi Au<sup>3+</sup><sub>(aq)</sub>. Kation ini akan bergerak ke katode menggantikan kation Au<sup>3+</sup> yang di reduksi di katode. Kation Au<sup>3+</sup> di katode direduksi membentuk endapan logam emas yang melapisi logam atau cincin besi. Proses ini cukup murah karena emas yang melapisi besi hanya berupa lapisan tipis. |
||
| ⚫ | |||
| ⚫ | |||
Anode (Au) : Au (s) Au3+ (aq) + 3e- |
|||
| ⚫ | Proses [[pemurnian]] logam kotor banyak dilakukan dalam pertambangan. Logam transisi yang kotor dapat dimurnikan dengan cara menempatkannya sebagai anode dan logam murni sebagai katode. Elektrolit yang digunakan adalah elektrolit yang mengandung kation logam yang dimurnikan. Contoh: proses pemurnian [[nikel]] menggunakan larutan NiSO<sub>4(aq)</sub>. Nikel murni digunakan sebagai katode, sedangkan nikel kotor (logam yang dimurnikan) digunakan sebagai anode. Reaksi yang terjadi, yaitu: |
||
NiSO<sub>4(aq)</sub> → Ni<sup>2+</sup><sub>(aq)</sub> + SO<sub>4</sub><sup>2-</sup><sub>(aq)</sub> |
|||
| ⚫ | Proses yang terjadi yaitu oksidasi logam emas (anode) menjadi |
||
| ⚫ | |||
| ⚫ | |||
| ⚫ | Proses pemurnian logam kotor banyak dilakukan |
||
| ⚫ | |||
NiSO4 (aq) Ni2+ (aq) + SO42- (aq) |
|||
| ⚫ | Logam nikel yang kotor pada anode dioksidasi menjadi ion Ni<sup>2+</sup>. Kemudian, ion Ni<sup>2+</sup> pada katode direduksi membentuk logam Ni dan bergabung dengan katode yang merupakan logam murni. Kation Ni<sup>2+</sup> di anode bergerak ke daerah katode menggantikan kation yang direduksi. Untuk mendapatkan logam nikel murni (di katode), diharuskan ada penyaringan sehingga kotoran (tanah, pasir, dan lain-lain) hanya berada di anode dan tidak berpindah ke katode sehingga daerah di katode merupakan daerah yang bersih. |
||
| ⚫ | |||
== Lihat pula == |
|||
| ⚫ | |||
* [[Metalurgi ekstraktif]] |
|||
* [[Tungku pembakaran]] |
|||
* [[Pengecoran]] |
|||
* [[Tanur Busur Listrik]] |
|||
* [[Fabrikasi logam]] |
|||
* [[Logam paduan]] |
|||
* [[Logam]] |
|||
* [[Peleburan (metalurgi)]] |
|||
* [[Pemurnian]] |
|||
==Referensi== |
|||
| ⚫ | Logam nikel yang kotor pada anode dioksidasi menjadi ion |
||
{{reflist}} |
|||
{{Authority control}} |
|||
[[Kategori:Elektrokimia]] |
[[Kategori:Elektrokimia]] |
||
[[Kategori:Proses metalurgi]] |
|||
[[Kategori:Pengolahan mineral]] |
|||
[[Kategori:Metalurgi]] |
|||
[[Kategori:Metalurgi ekstraktif]] |
|||
[[Kategori:Ekstraksi bijih]] |
|||
Revisi terkini sejak 29 Maret 2024 11.58
Elektrolisis adalah penguraian suatu elektrolit oleh arus listrik pada sel elektrolisis[1]. Reaksi kimia akan terjadi jika arus listrik dialirkan melalui larutan elektrolit, yaitu energi listrik (arus listrik) diubah menjadi energi kimia (reaksi redoks). Tiga ciri utama, yaitu:
- Ada larutan elektrolit yang mengandung ion bebas. Ion-ion ini dapat memberikan atau menerima elektron sehingga elektron dapat mengalir melalui larutan.
- Ada sumber arus listrik dari luar, seperti baterai yang mengalirkan arus listrik searah (DC).
- Ada 2 elektrode dalam sel elektrolisis.
Elektrode yang menerima elektron dari sumber arus listrik luar disebut katode, sedangkan elektrode yang mengalirkan elektron kembali ke sumber arus listrik luar disebut anode. Katode adalah tempat terjadinya reaksi reduksi yang elektrodanya negatif (-) dan anode adalah tempat terjadinya reaksi oksidasi yang elektrodanya positif (+).
Etimologi
[sunting | sunting sumber]Kata "elektrolisis" diperkenalkan oleh Michael Faraday pada tahun 1834,[2] menggunakan kata bahasa Yunani ἤλεκτρον (pengucapan Yunani: [ɛ̌ːlektron]) "amber", yang sejak abad ke-17 diasosiasikan dengan fenomena kelistrikan, dan λύσις (pengucapan Yunani: [lýsis]) yang berarti "pelarutan". Namun demikian, elektrolisis, sebagai alat untuk mempelajari reaksi kimia dan mendapatkan elemen murni, mendahului penggunaan istilah dan deskripsi formal oleh Faraday.
Hukum Elektrolisis Faraday
[sunting | sunting sumber]Di awal abad ke-19, Michael Faraday menyelidiki hubungan antara jumlah listrik yang mengalir dalam sel dan kuantitas kimia yang berubah di elektroda saat elektrolisis. Ia merangkumkan hasil pengamatannya dalam dua hukum pada tahun 1833.
C (Coulomb) adalah satuan muatan listrik, dan 1 C adalah muatan yang dihasilkan bila arus 1 A (Ampere) mengalir selama 1 detik. Tetapan fundamental listrik adalah konstanta Faraday, F = 9,65 x104 C, yang didefinisikan sebagai kuantitas listrik yang dibawa oleh 1 mol elektron. Dimungkinkan untuk menghitung kuantitas mol perubahan kimia yang disebabkan oleh aliran arus listrik yang tetap mengalir untuk rentang waktu tertentu.
Hantaran listrik melalui larutan elektrolit dapat dianggap sebagai aliran elektron. Jadi, apabila elektron telah dapat mengalir dalam larutan elektrolit berarti listrik dapat mengalir dalam larutan tersebut. Elektron berasal dari kutub katode atau kutub negatif. Sedangkan pada anode melepaskan ion positif dan membentuk endapan pada logam katode. Di dalam larutan terurai proses:
CuSO4 → Cu2+ + SO42-
Ion Cu2+ ini akan berpindah menuju keping katode sedangkan ion SO42- akan menuju keping anode. Lama-lama keping katode ini akan timbul endapan dan terjadi perubahan massa. Massa ini dapat dihitung dengan cara:
G = a . I . t
Di mana:
G = jumlah endapan tembaga Cu (gram)
a = tara kimia listrik (gr/ampere.jam)
I = kuat arus listrik (ampere)
t = lamanya pengaliran arus (jam)
Untuk tembaga nilai a = 1,186 gr/ampere.jam, karena G telah dapat diketahui maka I arus dapat diperoleh dengan:
I = G/at
Kegunaan sel elektrolisis
[sunting | sunting sumber]Pembuatan gas di laboratorium
[sunting | sunting sumber]Sel elektrolisis banyak digunakan dalam industri pembuatan gas misalnya pembuatan gas oksigen, gas hidrogen, atau gas klorin. Untuk menghasilkan gas oksigen dan hidrogen, Anda dapat menggunakan larutan elektrolit dari kation golongan I A, (K+, Na+), golongan II A, (Ca2+, Mg2+), Al3+, Mn2+, dan anion yang mengandung oksigen (SO42-, CO32-, NO3-, PO43-, ClO4-) dengan elektrode Pt atau karbon. Reaksi elektrolisis yang menghasilkan gas, misalnya elektrolisis larutan Na2SO4 menggunakan elektrode karbon.
Reaksi yang terjadi:
Na2SO4(aq) → 2 Na+(aq) + SO42-(aq)
Katode (C): 2 H2O(l) + 2e- → 2 OH-(aq) + H2(g)
Anode (C): 2 H2O(l) → 4 H+(aq) + O2(g) + 4e-
Karena pada katode dan anode yang bereaksi adalah air, semakin lama air semakin berkurang sehingga perlu ditambahkan. Perlu diingat bahwa walaupun yang bereaksi adalah air, tidak berarti elektrolit Na2SO4 tidak diperlukan. Elektrolit ini berguna sebagai penghantar arus listrik.
Proses penyepuhan
[sunting | sunting sumber]Penyepuhan suatu logam emas, perak, atau nikel, bertujuan menutupi logam yang penampilannya kurang baik atau menutupi logam yang mudah berkarat. Logam-logam ini dilapisi dengan logam lain yang penampilan dan daya tahannya lebih baik agar tidak berkarat. Misalnya mesin kendaraan bermotor yang terbuat dari baja umumnya dilapisi kromium agar terhindar dari korosi. Beberapa alat rumah tangga juga disepuh dengan perak sehingga lebih awet dan penampilannya tampak lebih baik. Badan sepede titanium dilapisi titanium oksida (TiO2) yang bersifat keras dan tidak dapat ditembus oleh oksigen atau uap air sehingga terhindar dari reaksi oksida yang menyebabkan korosi. Prinsip kerja proses penyepuhan adalah penggunaan sel dengan elektrolit larutan dan elektrode reaktif. Contoh jika logam atau cincin dari besi akan dilapisi emas digunakan larutan elektrolit AuCl3(aq). Logam besi (Fe) dijadikan sebagai katode, sedangkan logam emasnya (Au) sebagai anode. Reaksi yang berlangsung dalam proses penyepuhan besi dengan emas yaitu:
AuCl3(aq) = Au3+(aq) + 3 Cl-(aq)
Katode (cincin Fe): Au3+(aq) + 3e- = Au(s)
Anode (Au): Au(s) = Au3+(aq) + 3e-
Proses yang terjadi yaitu oksidasi logam emas (anode) menjadi Au3+(aq). Kation ini akan bergerak ke katode menggantikan kation Au3+ yang di reduksi di katode. Kation Au3+ di katode direduksi membentuk endapan logam emas yang melapisi logam atau cincin besi. Proses ini cukup murah karena emas yang melapisi besi hanya berupa lapisan tipis.
Proses pemurnian logam kotor
[sunting | sunting sumber]Proses pemurnian logam kotor banyak dilakukan dalam pertambangan. Logam transisi yang kotor dapat dimurnikan dengan cara menempatkannya sebagai anode dan logam murni sebagai katode. Elektrolit yang digunakan adalah elektrolit yang mengandung kation logam yang dimurnikan. Contoh: proses pemurnian nikel menggunakan larutan NiSO4(aq). Nikel murni digunakan sebagai katode, sedangkan nikel kotor (logam yang dimurnikan) digunakan sebagai anode. Reaksi yang terjadi, yaitu:
NiSO4(aq) → Ni2+(aq) + SO42-(aq)
Katode (Ni murni): Ni2+(aq) + 2e- → Ni (s)
Anode (Ni kotor): Ni (s) → Ni2+(aq) + 2e-
Logam nikel yang kotor pada anode dioksidasi menjadi ion Ni2+. Kemudian, ion Ni2+ pada katode direduksi membentuk logam Ni dan bergabung dengan katode yang merupakan logam murni. Kation Ni2+ di anode bergerak ke daerah katode menggantikan kation yang direduksi. Untuk mendapatkan logam nikel murni (di katode), diharuskan ada penyaringan sehingga kotoran (tanah, pasir, dan lain-lain) hanya berada di anode dan tidak berpindah ke katode sehingga daerah di katode merupakan daerah yang bersih.
Lihat pula
[sunting | sunting sumber]- Metalurgi ekstraktif
- Tungku pembakaran
- Pengecoran
- Tanur Busur Listrik
- Fabrikasi logam
- Logam paduan
- Logam
- Peleburan (metalurgi)
- Pemurnian
Referensi
[sunting | sunting sumber]- ^ Author (22 Oktober 2022). "Sel Elektrolisis – Pengertian, Reaksi, Contoh Soal dan Pembahasan". zenius. Diakses tanggal 18 Desember 2023.
- ^ Oesper, Ralph; Speter, Max (1937). "The Faraday-Whewell correspondence concerning electro-chemical terms". The Scientific Monthly. 45 (6): 535–546. Bibcode:1937SciMo..45..535O.
