Reaksi Diels–Alder: Perbedaan antara revisi
Luckas-bot (bicara | kontrib) k r2.5.2) (bot Menambah: ca:Reacció de Diels-Alder |
kTidak ada ringkasan suntingan |
||
| Baris 14: | Baris 14: | ||
[[Otto Diels|Otto Paul Hermann Diels]] dan [[Kurt Alder]] pertama kali mendokumentasikan reaksi ini pada tahun 1928. Pada tahun 1950 mereka diberikan penghargaan [[Nobel]] di bidang kimia atas hasil kerja mereka. |
[[Otto Diels|Otto Paul Hermann Diels]] dan [[Kurt Alder]] pertama kali mendokumentasikan reaksi ini pada tahun 1928. Pada tahun 1950 mereka diberikan penghargaan [[Nobel]] di bidang kimia atas hasil kerja mereka. |
||
Reaksi Diels-Alder secara umum dianggap sebagai "Mona Lisa" reaksi di kimia organik karena ia hanya memerlukan energi yang sangat sedikit untuk membentuk cincin [[sikloheksena]] yang sangat berguna<ref>Kloetzel, M. C. ''Org. React.'' '''1948''', ''4'', 1-59. (Review)</ref><ref>Holmes, H. L. ''Org. React.'' '''1948''', ''4'', 60-173. (Review)</ref><ref>''Catalytic asymmetric Diels Alder reactions'', Kagan, H. B.; Riant, O. ''[[Chem. Rev.]]'' '''1992''', ''92'', 1007-1019. (Review){{DOI|10.1021/cr00013a013}}</ref><ref>''The Diels-Alder Reaction in Total Synthesis'' [[K. C. Nicolaou]], S. A. Snyder, T. Montagnon, G. Vassilikogiannakis ''[[Angew. Chem. Int. Ed.]]'' '''2002''', ''41'', 1668-1698. (Review) {{DOI|<nowiki>10.1002/1521-3773(20020517)41:10<1668::AID-ANIE1668>3.0.CO;2-Z</nowiki>}}</ref> |
Reaksi Diels-Alder secara umum dianggap sebagai "Mona Lisa" reaksi di kimia organik karena ia hanya memerlukan energi yang sangat sedikit untuk membentuk cincin [[sikloheksena]] yang sangat berguna.<ref>Kloetzel, M. C. ''Org. React.'' '''1948''', ''4'', 1-59. (Review)</ref><ref>Holmes, H. L. ''Org. React.'' '''1948''', ''4'', 60-173. (Review)</ref><ref>''Catalytic asymmetric Diels Alder reactions'', Kagan, H. B.; Riant, O. ''[[Chem. Rev.]]'' '''1992''', ''92'', 1007-1019. (Review){{DOI|10.1021/cr00013a013}}</ref><ref>''The Diels-Alder Reaction in Total Synthesis'' [[K. C. Nicolaou]], S. A. Snyder, T. Montagnon, G. Vassilikogiannakis ''[[Angew. Chem. Int. Ed.]]'' '''2002''', ''41'', 1668-1698. (Review) {{DOI|<nowiki>10.1002/1521-3773(20020517)41:10<1668::AID-ANIE1668>3.0.CO;2-Z</nowiki>}}</ref> |
||
== Referensi == |
== Referensi == |
||
Revisi per 23 Januari 2011 03.34
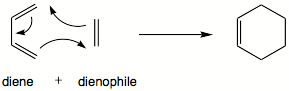
Reaksi Diels-Alder adalah reaksi kimia organik antara diena terkonjugasi dengan alkena tersubstitusi, umumnya dinamakan sebagai dienofil, membentuk sikloheksena tersubstitusi.[1][2][3] Reaksi ini dapat berjalan bahkan jika beberapa atom dari cincin yang terbentuk bukanlah karbon. Beberapa reaksi Diels-Alder adalah reversibel; reaksi dekomposisi dari sistem siklik dinamakan reaksi Retro-Diels-Alder. Reaksi retro ini umumnya terlihat pada saat analisa produk reaksi Diels-Alder menggunakan spektrometri massa.
Otto Paul Hermann Diels dan Kurt Alder pertama kali mendokumentasikan reaksi ini pada tahun 1928. Pada tahun 1950 mereka diberikan penghargaan Nobel di bidang kimia atas hasil kerja mereka.
Reaksi Diels-Alder secara umum dianggap sebagai "Mona Lisa" reaksi di kimia organik karena ia hanya memerlukan energi yang sangat sedikit untuk membentuk cincin sikloheksena yang sangat berguna.[4][5][6][7]
Referensi
- ^ Diels, O.; Alder, K. (1928). "Synthesen in der hydroaromatischen Reihe". Liebigs Annalen der Chemie. 460 (1): 98 – 122. doi:10.1002/jlac.19284600106.
- ^ Synthesis of the hydro aromatic sequence, Ann. 1929, 470, 62.
- ^ Synthesis in the hydroaromatic series, IV. Announcement: The rearrangement of malein acid anhydride on arylated diene, triene and fulvene, Diels, O.; Alder, K. Ber. 1929, 62, 2081 & 2087.
- ^ Kloetzel, M. C. Org. React. 1948, 4, 1-59. (Review)
- ^ Holmes, H. L. Org. React. 1948, 4, 60-173. (Review)
- ^ Catalytic asymmetric Diels Alder reactions, Kagan, H. B.; Riant, O. Chem. Rev. 1992, 92, 1007-1019. (Review)doi:10.1021/cr00013a013
- ^ The Diels-Alder Reaction in Total Synthesis K. C. Nicolaou, S. A. Snyder, T. Montagnon, G. Vassilikogiannakis Angew. Chem. Int. Ed. 2002, 41, 1668-1698. (Review) doi:10.1002/1521-3773(20020517)41:10<1668::AID-ANIE1668>3.0.CO;2-Z 10.1002/1521-3773(20020517)41:10<1668::AID-ANIE1668>3.0.CO;2-Z
Pranala luar
- Asymmetric Hetero-Diels-Alder Reactions
- Semi-empirical calculations of the Diels-Alder reaction.
- Endo Addition Rule
