Asam karbonat: Perbedaan antara revisi
Tampilan
Konten dihapus Konten ditambahkan
Tidak ada ringkasan suntingan |
Tidak ada ringkasan suntingan |
||
| Baris 1: | Baris 1: | ||
{{Chembox |
{{Chembox |
||
| ImageFile = |
| ImageFile = Carbonic-acid-3D-balls.png |
||
| Section1 = {{Chembox Identifiers |
| Section1 = {{Chembox Identifiers |
||
| CASNo = 463-79-6 |
| CASNo = 463-79-6 |
||
| Baris 11: | Baris 10: | ||
}} |
}} |
||
}} |
}} |
||
[[Berkas:Carbonic-acid-2D.svg|thumb|left|Struktur asam karbonat secara dua dimensi.]] |
|||
'''Asam karbonat''' adalah asam organik dengan rumus kimia H<sub>2</sub>CO<sub>3</sub>. Asam karbonat termasuk asam lemah. |
'''Asam karbonat''' adalah asam organik dengan rumus kimia H<sub>2</sub>CO<sub>3</sub>. Asam karbonat termasuk asam lemah. |
||
Revisi per 12 Oktober 2012 06.27

| |
| Penanda | |
|---|---|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| Sifat | |
| H2CO3 | |
| Massa molar | 62.03 g/mol |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
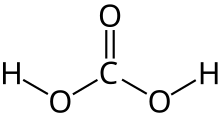
Asam karbonat adalah asam organik dengan rumus kimia H2CO3. Asam karbonat termasuk asam lemah.
Persamaan Reaksi Kimia
Ketika karbon dioksida (CO2) larut dalam air (H2O) maka akan menghasilkan asam karbonat.
- CO2 + H2O
 H2CO3. Asam karbonat bisa berubah menjadi ion bikarbonat (HCO3-) dan atom hidrogen.
H2CO3. Asam karbonat bisa berubah menjadi ion bikarbonat (HCO3-) dan atom hidrogen.
External links
- http://www.insightempire.com/carbonic-acid/
- Ask a Scientist: Carbonic Acid Decomposition
- Why was the existence of carbonic acid unfairly doubted for so long?
- Carbonic acid/bicarbonate/carbonate equilibrium in water: pH of solutions, buffer capacity, titration and species distribution vs. pH computed with a free spreadsheet
- How to calculate concentration of Carbonic Acid in Water
