Periodisitas sifat unsur
artikel ini perlu dirapikan agar memenuhi standar Wikipedia. |
Artikel ini tidak memiliki bagian pembuka yang sesuai dengan standar Wikipedia. |
Unsur-unsur kimia yang terdapat di alam memiliki sifat-sifat yang khas. Sifat-sifat tersebut ternyata memiliki keteraturan yang disusun dalam suatu tabel periodik. Berikut Ini akan dibahas periodisitas sifat unsur yang meliputi ukuran atom, energi ionisasi, afinitas elektron, keelektronegatifan, dan sifat logam. Selain itu, ditemukan juga beberapa unsur yang tidak mengikuti keteraturan tersebut.
Sejarah
Penggolongan unsur dimulai oleh Dobereiner yang didasarkan pada triad. Kemudian Newland menggolongkan unsur berdasarkan hukum oktaf. Kedua cara ini menghubungkan antara massa atom relatif dengan sifat unsur.

Setelah itu, Mendeleev menggolongkan unsur di dalam sebuah tabel periodik[1]. Tabel periodik tersebut menyebutkan bahwa sifat unsur adalah fungsi massa atom relatifnya. Kemudian Moseley menemukan dan menyusun unsur berdasarkan nomor atom. Lalu muncullah hukum periodik modern yang menyatakan bahwa sifat unsur merupakan fungsi periodik nomor atomnya.
Sistem periodik modern ini disusun berdasarkan konfigurasi elektron dari unsur-unsur. Unsur dibagi menjadi 4 blok, yakni blok s, p, d, dan f. Kemudian dibagi menjadi 2 golongan, yaitu golongan utama (blok s dan p) dan golongan transisi (blok d dan f). Unsur dalam satu golongan memiliki elektron valensi yang sama sedangkan unsur dalam satu periode memiliki jumlah kulit yang sama. Unsur yang memiliki kemampuan untuk melepas elektron digolongkan sebagai logam dan unsur yang memiliki kemampuan untuk menerima elektron digolongkan sebagai nonlogam. Terdapat unsur yang memiliki kemampuan di antara keduanya, yakni memiliki kecenderungan melepaskan atau menerima elektron digolongkan sebagai metaloid.
Sifat-sifat Periodik
Unsur-unsur baik dalam satu golongan maupun satu periode memang memiliki kemiripan. Namun, di antara unsur-unsur tersebut memiliki perbedaan tertentu. Sifat-sifat yang berbeda tersebut berubah dengan kecenderungan tertentu sesuai dengan berubahnya nomor atom. Kecenderungan tersebut berulang dalam golongan dan periode berikutnya sehingga disebut dengan sifat periodik. Sifat-sifat periodik tersebut adalah sebagai berikut.
Ukuran Atom
Dalam menentukan ukuran atom pendekatan yang dapat digunakan adalah memahami daerah keberadaan elektron dalam suatu orbital atom dan menentukan jaraknya terhadap inti. Daerah keberadaan elektron tersebut dianggap bulat, sehingga dapat ditentukan jari-jarinya.
Jari – jari atom
Jarak lintasan terluar dari atom terhadap inti atom. Dalam lintasan tersebut ditemukan keberadaan elektron.

Jari-jari kovalen
Jari-jari pada ikatan kovalen adalah setengah jarak antar 2 inti atom dalam ikatan tunggal kovalen.
Jari-jari non Logam(Jari-jari van der Walls)
Pada atom-atom yang bersentuhan namun tidak berikatan memiliki jarak tanpa-ikatan yang terdekat. Jarak ini disebut dengan jari-jari van der Walls.
Jari-jari Logam
Setengah jarak dua atom Kristal padat unsur logam disebut dengan jari-jari logam. Jari-jari ini mirip dengan jari-jari kovalen.
Jari – jari ion
Ukuran jari-jari ion pada logam akan berbeda dengan aslinya. Jari-jari ion positif lebih kecil dari jari-jari kovalen dan sebaliknya jari-jari ion negatif lebih besar dari jari-jari kovalen. Ketika suatu atom kehilangan elektron disebut kation dan ketika suatu atom menarik elektron disebut anion.
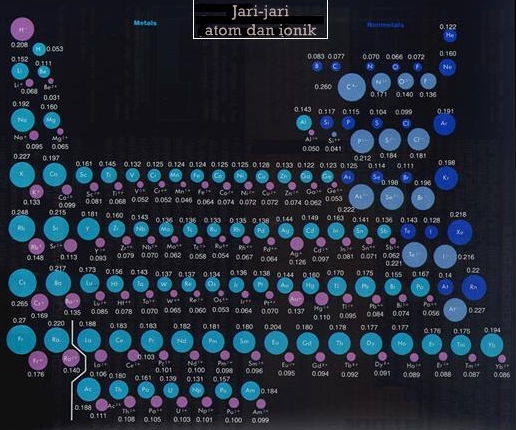
Ketika sebuah atom kehilangan elektronnya, tarikan inti terhadap elektron terluar dari atom akan semakin besar, sehingga akan terjadi suatu penciutan terhadap kulit dan menyebabkan jari-jari terlihat mengecil. Begitu juga sebaliknya, ketika sebuah atom mendapatkan sebuah elektron, tarikan inti terhadap elektron terluarnya semakin kecil, sehingga jari-jari atom tersebut terlihat lebih besar.
Keteraturan:
Dalam suatu periode, dari kiri ke kanan akan terjadi pengecilan jari-jari atom. Hal ini terjadi karena jumlah valensi terus bertambah namun tidak diikuti dengan penambahan kulit.
Secara vertikal (golongan), penambahan suatu jari-jari atom pada unsur menemukan keteraturan dari atas ke bawah. Hal ini seiring dengan bertambahnya jumlah kulit atom dari golongan unsur.

Energi ionisasi (EI)
Ionisasi erat kaitannya dengan ion, aktivitas ion pada keadaan tertentu adalah pelepasan dan penarikan elektron, ionisasi dikatakan sebagai pelepasan satu elektron dari suatu atom netral. Sehingga, energi ionisasi dijabarkan sebagai sejumlah energi yang dibutuhkan untuk melepas satu elektron dari atom netralnya.
Dalam ilmu yang berkembang, dikenal adanya energi ionisasi pertama(I1), energi ionisasi kedua (I2), energi ionisasi ketiga, energi ionisasi keempat, energi ionisasi suksesif (berturut-turut), dan seterusnya. Angka 1 dan 2 pada energi ionisasi menunjukkan di orbital manakah elektron tersebut telah hilang.
Pada tabel periodik unsur dikenal beberapa keteraturan terhadap arah golongan dan periode. Namun, keteraturan ini tidak absolute.
Keteraturan berdasarkan periode
Dalam periode, EI suatu unsur ditemukan semakin bertambah dari arah kiri dan kanan. Hal ini disebabkna karena adanya penambahan muatan atom namun dalam jumlah kulit yang tetap.
Keteraturan berdasarkan golongan
Secara vertikal, penambahan jumlah EI ditemukan dari bawah ke atas pada suatu golongan. Hal ini dapat dikaitkan dengan ukuran dari atom suatu unsur dimana semakin kecil ukuran atom berarti semakin dekat jarak elektron valensi terhadap inti atom sehingga gaya tarik inti semakin besar dan untuk melakukan pelepasan elektron tersebut diperlukan energi yang sangat besar. Namun secara garis besar, keteraturan ini tidak pernah absolute.
Faktor yang mempengaruhi energi ionisasi adalah sebagai berikut.
- Muatan pada inti.
- Jarak dari elektron pada inti.
Namun, pada suatu periode terdapat beberapa unsur yang tidak mengikuti keteraturan tersebut seperti Be dan Mg, serta N dan P.
| Li (520) | Be (900) | B (800) | C (1086) | N (1402) | O (1314) |
| Na (496) | Mg (738) | Al (577) | Si (786) | P (1012) | S (999) |
Hal ini terjadi karena adanya energi pasangan (coupling energy), yakni energi yang dimiliki oleh orbital penuh dan energi tambahan yang dimiliki oleh orbital setengah penuh.
Afinitas Elektron
Berseberangan dengan energi ionisasi, afinitas elektron dapat dikatakan sebagai sejumlah energi yang dilepaskan suatu atom saat atom tersebut menambahkan suatu elektronnya menjadi suatu anionnya.
Terjadi pula pengecualian pada unsur dengan orbital s yang terisi penuh dan p setengah penuh, seperti pada unsur Be dan Mg, serta N dan P.
| Li (-60) | Be (+100) | B (-27) | C (-122) | N (+9) | O (-141) |
| Na (-53) | Mg (+33) | Al (-44) | Si (-134) | P (+72) | S (-200) |
Pada orbital unsur yang mengalami pengecualian memiliki daya tarik tambahan terhadap elektronnya sehingga muatan efektif pada elektron yang masuk lebih kecil. Hal ini mengakibatkan untuk menambahkan satu elektron membutuhkan energi dari luar.
Elektronegatifitas
Elektronegatifitas dapat dijabarkan sebagai kemampuan suatu atom untuk menarik elektron dari atom lain. Elektronegatifitas ini dapat dipangaruhi oleh jari-jari atom dan gaya tarik inti terhadap elektron terluar dari suatu atom.
Keteraturan:
- Secara vertikal dalam golongan, keelektronegatifan suatu atom akan semakin kecil. Hal ini karena kekuatan gaya tarik inti semakin melemah dan cenderung melepaskan elektron.
- Secara horizontal, keelektronegatifan semakin ke kanan semakin besar. Hal ini karena semakin banyak elektron pada kulit terluar dan probability untuk menarik elektron lain semakin besar.
Sifat Kelogaman
sifat kimia dari unsur-unsur logam dianggap dapat muncul dari kemampuan unsur untuk melepas elektron untuk membentuk lautan elektron yang mengikat kation bersama-sama dan membentuk ikatan logam[2] Dalam tabel periodik, sifat kelogaman unsur-unsur semakin berkurang dalam satu periode dan semakin bertambah dari atas ke bawah dalam satu golongan. Unsur yang bersifat logam memiliki ciri khas yakni mudah melepaskan elektron sehingga dapat dihubungkan dengan energi ionisasi, yakni sejumlah energi yang dibutuhkan untuk melepas satu elektron dari atom netralnya.
Sumber
Achmad, Hiskia. 1992. Kimia Unsur dan Radiokimia. Bandung: PT Citra Aditya Bakti
Atkins,P.W., T.L. Overton, J.P. Rourke, M.T. Weller, and F.A. Armstrong. 2010. Inorganic Chemistry. Great Britain: Oxford University Press
Heslop, R.B., P.L. Robinson. 1960. Inorganic Chemistry , A Guide to Advanced Study. London: Elsevier Publishing Company
Macmillan. 1957. A Text Book of Inorganic Chemistry. New York: St Martin’s Press
Mackay, K.M., R. Ann Mackay. 1974. Introduction to Modern Inorganic Chemistry 2nd Edition. Kingswood: International Textbook Company Limited
Petrucci, Ralph H – Suminar. 1996. Kimia Dasar, Prinsip dan Terapan Modern. Jakarta: Erlangga
Rosenberg, Jerome L. – Jasjfi. 1992. Seri Buku Schaum Teori dan Soal-Soal Kimia Dasar. Jakarta: Erlangga
Syukri, S. 1999. Kimia Dasar. Bandung: ITB
Referensi
- ^ Tabel periodik
- ^ Atkins,P.W., T.L. Overton, J.P. Rourke, M.T. Weller, and F.A. Armstrong. (2010) Inorganic Chemistry, p.263
