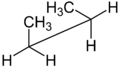
Rumus struktur

Rumus struktur dari suatu senyawa kimia adalah representasi grafis dari struktur molekul, yang menunjukkan bagaimana atom tersusun.[1] Ikatan kimia dalam molekul juga ditunjukkan, baik secara eksplisit maupun implisit. Tidak seperti rumus kimia, yang memiliki jumlah simbol terbatas dan hanya memiliki kekuatan deskriptif terbatas, rumus struktural memberikan representasi geometrik lengkap dari struktur molekul. Sebagai contoh, banyak senyawa kimia ada dalam bentuk isomerik yang berbeda, yang memiliki struktur enansiomerik yang berbeda namun memiliki rumus kimia yang sama. Rumus struktur dapat menunjukkan pengaturan atom dalam ruang tiga dimensi dengan cara yang mungkin tidak dapat dilakukan oleh rumus kimia.
Beberapa format 'penamaan' kimia yang sistematis, seperti dalam basis data kimia, digunakan yang setara dengan, dan sekuat struktur geometris.[2] Sistem tata nama senyawa kimia ini termasuk SMILES, InChI dan CML.[3][4] Nama kimia yang sistematis ini dapat dikonversi menjadi rumus struktural dan sebaliknya, namun kimiawan hampir selalu menggambarkan reaksi kimia atau sintesis dengan menggunakan rumus struktural daripada nama kimia, karena rumus struktural memungkinkan kimiawan untuk memvisualisasikan molekul dan perubahan struktural yang terjadi di dalamnya selama reaksi kimia.
Rumus terkondensasi
Dalam publikasi organik-kimia awal, di mana penggunaan grafis sangat terbatas, sistem tipografi muncul untuk menggambarkan struktur organik dalam garis teks. Meskipun sistem ini cenderung bermasalah dalam aplikasi pada senyawa siklik, namun tetap merupakan cara mudah untuk merepresentasikan struktur sederhana:
CH3CH2OH (etanol)
Tanda kurung digunakan untuk menunjukkan beberapa kelompok identik, menunjukkan keterikatan pada atom non-hidrogen terdekat di sebelah kiri saat muncul dalam rumus, atau ke atom di sebelah kanan saat muncul pada awal rumus:
(CH3)2CHOH or CH(CH3)2OH (2-propanol)
Dalam semua kasus, semua atom diperlihatkan, termasuk atom hidrogen.
Rumus kerangka
Rumus kerangka adalah notasi standar untuk molekul organik yang lebih kompleks. Dalam jenis diagram ini, pertama kali digunakan oleh ahli kimia organik Friedrich August Kekulé von Stradonitz, atom karbon tersirat berada di simpul (sudut) dan garis ujung segmen garis daripada diindikasikan dengan simbol atom C. Atom hidrogen yang terikat pada atom karbon tidak ditunjukkan: setiap atom karbon dipahami terkait dengan atom hidrogen yang cukup untuk memberi atom karbon empat ikatan. Kehadiran muatan positif atau negatif muatan listrik di sebuah atom karbon menggantikan salah satu atom hidrogen tersirat. Atom hidrogen yang menempel pada atom selain karbon harus ditulis secara eksplisit.
-
Rumus kerangka asam asetat, CH3COOH
Struktur Lewis
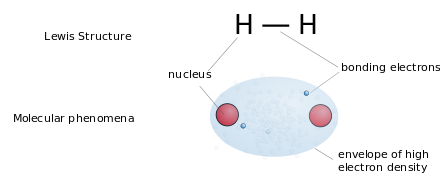
Struktur Lewis (atau "struktur titik Lewis") adalah rumus grafis datar yang menunjukkan konektivitas atom dan pasangan elektron bebas atau tidak berpasangan, namun bukan struktur tiga dimensi.[5] Notasi ini banyak digunakan untuk molekul kecil. Setiap baris mewakili dua elektron dari ikatan tunggal. Dua atau tiga garis sejajar antara pasangan atom mewakili ikatan rangkap dua atau tiga. Sebagai alternatif, pasang titik dapat digunakan untuk mewakili pasangan ikatan. Selain itu, semua elektron yang tidak terikat (dipasangkan atau tidak berpasangan) dan setiap muatan formal pada atom ditunjukkan.[6][7]
-
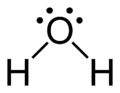
Struktur Lewis dari air
Indikasi stereokimia
Terdapat eberapa metode untuk menggambarkan pengaturan tiga dimensi atom dalam molekul (stereokimia).
Stereokimia dalam rumus kerangka

Kiralitas dalam rumus kerangka ditunjukkan dengan metode proyeksi Natta. Ikatan terjepit padat atau putus-putus mewakili ikatan yang menunjuk ke atas-bidang atau di bawah bidang kertas.
Stereokimia yang tidak ditentukan
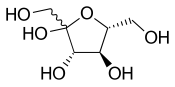
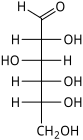
Ikatan tunggal bergelombang mewakili stereokimia yang tidak diketahui atau tidak ditentukan atau campuran isomer. Sebagai contoh, diagram yang berdekatan menunjukkan molekul fruktosa dengan ikatan bergelombang pada gugus HOCH2- tersebut pada sebelah kiri. Dalam kasus ini dua struktur cincin yang mungkin berada dalam ekuilibrium kimia satu sama lain dan juga dengan struktur rantai terbuka. Cincin itu terus terbuka dan tertutup, terkadang ditutup dengan satu stereokimia dan kadang-kadang dengan yang lain.
Rumus kerangka dapat menggambarkan isomerisme cis dan trans dari alkena. Ikatan tunggal bergelombang adalah cara standar untuk mewakili stereokimia yang tidak diketahui atau tidak ditentukan atau campuran isomer (seperti pusat stereo tetrahedral). Sebuah ikatan silang telah digunakan kadang-kadang, namun tidak lagi dianggap sebagai gaya yang dapat diterima untuk penggunaan umum.[8]
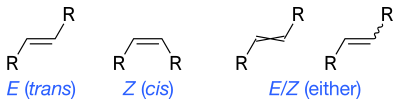
Perspektif gambar
Proyeksi Newman dan proyeksi sawhorse
Proyeksi Newman dan proyeksi sawhorse digunakan untuk menggambarkan konformasi kimia tertentu atau untuk membedakan stereokimia visinal. Dalam kedua kasus tersebut, dua atom karbon spesifik dan ikatan penghubungnya merupakan pusat perhatian. Satu-satunya perbedaan adalah perspektif yang sedikit berbeda: proyeksi Newman yang melihat langsung ke bawah ikatan bunga, proyeksi kuda-kuda melihat ikatan yang sama tetapi dari sudut pandang miring yang bagus. Dalam proyeksi Newman, sebuah lingkaran digunakan untuk mewakili bidang yang tegak lurus terhadap ikatan, yang membedakan substituen pada karbon depan dari substituen pada karbon belakang. Dalam proyeksi sawhorse, karbon depan biasanya di sebelah kiri dan selalu sedikit lebih rendah:
-
Proyeksi Newman dari butana
-
Proteksi sawhorse dari butana
Konformasi sikloheksana
Konformasi tertentu dari sikloheksana dan senyawa cincin kecil lainnya dapat ditunjukkan dengan menggunakan konvensi standar. Sebagai contoh, konformasi kursi standar sikloheksana melibatkan pandangan perspektif dari sedikit di atas bidang rata-rata atom karbon dan menunjukkan dengan jelas gugus mana yang aksial dan yang ekuatorial. Ikatan di depan mungkin atau mungkin tidak disorot dengan garis atau irisan yang lebih kuat.
-
Konformasi kursi beta-D-Glukosa
Proyeksi Haworth
Proyeksi Haworth digunakan untuk gula siklik. Posisi aksial dan ekuator tidak dibedakan; Sebagai gantinya, substituen diposisikan tepat di atas atau di bawah cincin tempat mereka terhubung. Substituen hidrogen biasanya dihilangkan.
-
Proyeksi Haworth beta-D-Glukosa
Proyeksi Fischer
Proyeksi Fischer banyak digunakan untuk monosakarida linear. Pada setiap pusat karbon tertentu, garis ikatan vertikal setara dengan tanda titik stereokimia, yang diarahkan menjauh dari pengamat, sementara garis horizontal setara dengan irisan, mengarah ke pengamat. Proyeksi ini sama sekali tidak realistis, karena sakarida tidak akan pernah mengadopsi konformasi multi eklips ini. Meskipun demikian, proyeksi Fischer adalah cara sederhana untuk menggambarkan stereocenters sekuensial ganda yang tidak memerlukan atau menyiratkan pengetahuan tentang konformasi yang sebenarnya:
Lihat pula
Referensi
- ^ Chang, Raymond (2005). Kimia Dasar: Konsep-Konsep Inti Edisi Ketiga Jilid 1 (edisi ke-3rd). Jakarta: Erlangga. ISBN 979-781-039-9.
- ^ Hepler-Smith, Evan (2015). ""Just as the Structural Formula Does": Names, Diagrams, and the Structure of Organic Chemistry at the 1892 Geneva Nomenclature Congress": 1–28. doi:10.1179/1745823414Y.0000000006.
- ^ Opler, A.; Baird, N. (1959). "Display of chemical structural formulas as digital computer output". Amer. Doc. 10: 59–63. doi:10.1002/asi.5090100107.
- ^ Opler, A. (1959). "On the automatic manipulation of representations of chemical structures". Amer. Doc. 10 (2): 130. doi:10.1002/asi.5090100206.
- ^ Cotton, F. Albert; Wilkinson, Geoffrey; Murillo, Carlos A.; Bochmann, Manfred (1999), Advanced Inorganic Chemistry (edisi ke-6th), New York: Wiley-Interscience, ISBN 0-471-19957-5
- ^ Gillespie, R.J.; Popelier, P.L.A. (2001). Chemical Bonding and Molecular Geometry: From Lewis to Electron Densities. Oxford: Oxford University Press. ISBN 978-019-510-496-7.
- ^ Auvert, G. (2014). "Improvement of the Lewis-Abegg-Octet Rule Using an "Even-Odd" Rule in Chemical Structural Formulas: Application to Hypo and Hypervalences of Stable Uncharged Gaseous Single-Bonded Molecules with Main Group Elements". Open Journal of Physical Chemistry. 4 (2). doi:10.4236/ojpc.2014.42009.
- ^ J. Brecher (2006). "Graphical representation of stereochemical configuration (IUPAC Recommendations 2006)" (PDF). Pure Appl. Chem. 78 (10): 1897–1970. doi:10.1351/pac200678101897.