Asam laktat
Tampilan
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC (preferensi)
2-Hydroxypropanoic acid[1] | |||
| Nama lain
Lactic acid[1]
Milk acid | |||
| Penanda | |||
| |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
| Nomor RTECS | {{{value}}} | ||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C3H6O3 | |||
| Massa molar | 90,08 g·mol−1 | ||
| Titik lebur | 53 °C | ||
| Titik didih | 122 °C (252 °F; 395 K) @ 15 mmHg | ||
| Keasaman (pKa) | 3.86,[2] 15.1[3] | ||
| Termokimia | |||
| Entalpi pembakaran standar ΔcH |
1361.9 kJ/mol, 325.5 kcal/mol, 15.1 kJ/g, 3.61 kcal/g | ||
| Farmakologi | |||
| Kode ATC | G01 QP53AG02 | ||
| Bahaya | |||
| Piktogram GHS |  [4] [4]
| ||
| H315, H318[4] | |||
| P280, P305+351+338[4] | |||
| Senyawa terkait | |||
Anion lain
|
laktat | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
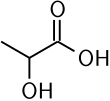
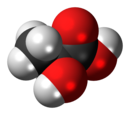
Asam laktat (Nama IUPAC: asam 2-hidroksipropanoat (CH3-CHOH-COOH), dikenal juga sebagai asam susu) adalah senyawa kimia penting dalam beberapa proses biokimia. Seorang ahli kimia Swedia, Carl Wilhelm Scheele, pertama kali mengisolasinya pada tahun 1780. Secara struktur, ia adalah asam karboksilat dengan satu gugus hidroksil yang menempel pada gugus karboksil. Dalam air, ia terlarut lemah dan melepas proton (H+), membentuk ion laktat. Asam ini juga larut dalam alkohol dan bersifat menyerap air (higroskopik).
Asam ini memiliki simetri cermin (kiralitas), dengan dua isomer: asam L-(+)-laktat atau asam (S)-laktat dan, cerminannya, iasam D-(-)-laktat atau asam (R)-laktat. Hanya isomer yang pertama (S) aktif secara biologi.
Pranala luar
- Corn Plastic to the Rescue
- Lactic Acid: Information and Resources
- Lactic Acid Is Not Muscles' Foe, It's Fuel
- Fitzgerald M (January 26, 2010). "The Lactic Acid Myths". Competitor Running.
- ^ a b Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. hlm. 748. doi:10.1039/9781849733069-00648. ISBN 978-0-85404-182-4.
- ^ Dawson RM, et al. (1959). Data for Biochemical Research. Oxford: Clarendon Press.
- ^ Silva AM, Kong X, Hider RC (October 2009). "Determination of the pKa value of the hydroxyl group in the alpha-hydroxycarboxylates citrate, malate and lactate by 13C NMR: implications for metal coordination in biological systems". Biometals. 22 (5): 771–8. doi:10.1007/s10534-009-9224-5. PMID 19288211.
- ^ a b c Sigma-Aldrich Co., DL-Lactic acid.