Sinarizin

| |
|---|---|
| Nama sistematis (IUPAC) | |
| (E)-1-(Difenilmetil)-4-(3-fenilprop-2-enil)piperazina | |
| Data klinis | |
| Nama dagang | Stugeron, Stunarone, Cinarin, dll |
| AHFS/Drugs.com | International Drug Names |
| Kat. kehamilan | ? |
| Status hukum | P (UK) |
| Rute | Oral |
| Data farmakokinetik | |
| Bioavailabilitas | Lemah[1] |
| Metabolisme | Menyeluruh[2][3] |
| Waktu paruh | 3–4 jam[4] |
| Ekskresi | ⅓ urin, ⅔ feses[2] |
| Pengenal | |
| Nomor CAS | 298-57-7 |
| Kode ATC | N07CA02 |
| PubChem | CID 1547484 |
| DrugBank | DB00568 |
| ChemSpider | 1264793 |
| UNII | 3DI2E1X18L |
| KEGG | D01295 |
| ChEBI | CHEBI:31403 |
| ChEMBL | CHEMBL43064 |
| Data kimia | |
| Rumus | C26H28N2 |
| SMILES | eMolecules & PubChem |
| |
Sinarizin adalah antihistamin dan penghambat saluran kalsium dari kelompok difenilmetilpiperazin.[5] Obat ini diresepkan untuk mual dan muntah akibat mabuk gerak[6] atau sumber lain seperti kemoterapi,[7] vertigo,[8] atau penyakit Ménière.[9] Sinarizin adalah salah satu penyebab utama parkinsonisme akibat obat.[5]
Sinarizin pertama kali disintesis sebagai R1575 oleh Janssen Pharmaceuticals pada tahun 1955. Nama bukan hak miliknya berasal dari substituen sinamil pada salah satu atom nitrogen, digabungkan dengan akhiran generik "-rizin" untuk "vasodilator antihistamin/otak (atau perifer)".[10] Obat ini tidak tersedia di Amerika Serikat atau Kanada. Obat ini juga disebut-sebut sebagai salah satu obat yang paling banyak digunakan untuk mabuk laut di Angkatan Laut Britania Raya.[11]
Kegunaan dalam Medis
Sinarizin sebagian besar digunakan untuk mengobati mual dan muntah yang berhubungan dengan mabuk gerak,[6] vertigo,[8] penyakit Ménière,[9] atau sindrom Cogan.[2] Obat ini adalah salah satu dari sedikit obat yang memiliki efek menguntungkan dalam pengobatan kronis vertigo dan tinitus yang berhubungan dengan penyakit Ménière.[12]
Dalam sebuah studi klinis (n=181), pengobatan dengan sinarizin mengurangi terjadinya pengalaman vertigo sedang sebesar 65,8% dan vertigo ekstrem sebesar 89,8%.[8]
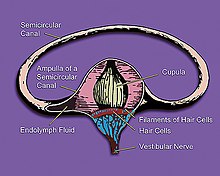
Obat ini bekerja dengan mengganggu transmisi sinyal antara alat vestibular di telinga bagian dalam dan pusat muntah di hipotalamus dengan membatasi aktivitas sel rambut vestibular yang mengirimkan sinyal tentang gerakan.[13] Kesenjangan pemrosesan sinyal antara reseptor gerak telinga bagian dalam dan indera penglihatan dihilangkan, sehingga kebingungan otak apakah seseorang sedang bergerak atau berdiri berkurang. Muntah saat mabuk gerak bisa menjadi mekanisme kompensasi fisiologis otak untuk mencegah seseorang bergerak sehingga dapat menyesuaikan diri dengan persepsi sinyal, namun alasan evolusi sebenarnya dari penyakit ini saat ini tidak diketahui.[14]
Ketika diresepkan untuk masalah keseimbangan dan vertigo, sinarizin biasanya diminum dua atau tiga kali sehari tergantung pada jumlah masing-masing dosis dan bila digunakan untuk mengobati mabuk perjalanan, pil diminum setidaknya dua jam sebelum perjalanan dan setiap empat jam selama perjalanan.[15] Namun, penelitian terbaru pada tahun 2012 yang membandingkan efek sinarizin dengan skopolamin transdermal untuk pengobatan mabuk laut, menyimpulkan bahwa skopolamin dilaporkan jauh lebih efektif dan memiliki lebih sedikit efek samping dibandingkan sinarizin.[16] Hal ini mengarah pada kesimpulan bahwa skopolamin transdermal kemungkinan merupakan pilihan yang lebih baik untuk pengobatan mabuk perjalanan pada awak angkatan laut dan pelancong laut lainnya. Namun, karena meningkatnya tingkat rasa kantuk yang disebabkan oleh obat tersebut, penggunaan obat ini umumnya terbatas pada pilot dan awak pesawat yang harus selalu waspada.[6]
Selain itu, sinarizin dapat digunakan pada penyelam skuba tanpa peningkatan risiko toksisitas oksigen sistem saraf pusat yang dapat menyebabkan sawan, dan merupakan risiko tinggi dalam penyelaman oksigen sirkuit tertutup. Hal ini juga relevan bagi penyelam yang mungkin harus menjalani terapi dekompresi hipobarik, yang menggunakan tekanan oksigen tinggi dan juga dapat terpengaruh oleh risiko toksisitas oksigen SSP yang disebabkan oleh sinarizin. Namun, sinarizin tidak meningkatkan risiko toksisitas, dan faktanya bukti menunjukkan bahwa sinarizin mungkin bermanfaat dalam membantu menunda toksisitas O2 pada sistem saraf pusat.[17] Ada juga bukti bahwa sinarizin dapat digunakan sebagai obat antiasma yang efektif bila diminum secara teratur.[18]
Selain pengobatan anti-vertigo, sinarizin juga dapat dipandang sebagai obat nootropika karena kemampuan vasorelaksasinya (akibat blokade saluran kalsium), yang sebagian besar terjadi di otak, dan fakta bahwa sinarizin juga digunakan sebagai obat penenang labirin.[19][20] Sinarizin menghambat aliran kalsium ke dalam sel darah merah, sehingga meningkatkan elastisitas dinding sel, sehingga meningkatkan fleksibilitasnya dan membuat darah menjadi kurang kental. Hal ini memungkinkan darah mengalir lebih efisien dan efektif melalui pembuluh yang menyempit untuk membawa oksigen ke jaringan yang rusak.[2] Hal ini juga efektif dikombinasikan dengan nootropika lain, terutama pirasetam; dalam kombinasi seperti itu, masing-masing obat mempotensiasi obat lain dalam meningkatkan suplai oksigen otak.[21] Sebuah penelitian pada hewan yang membandingkan efektivitas sinarizin dan flunarizin (turunan sinarizin yang 2,5-15 kali lebih kuat[22] untuk pengobatan iskemia serebral global sementara), ditemukan bahwa cinnarizine membantu memperbaiki kelainan fungsional iskemia, tetapi tidak membantu kerusakan pada neuron. Flunarizine menawarkan lebih banyak perlindungan saraf, namun kurang efektif dalam mengobati perubahan perilaku selanjutnya.[23]
Sinarizin juga terbukti menjadi pengobatan lini kedua yang berharga untuk vaskulitis urtikaria idiopatik.[24]
Efek Samping
Efek samping yang dialami saat mengonsumsi sinarizin berkisar dari yang ringan hingga yang cukup parah. Kemungkinan efek samping termasuk parkinsonisme akibat obat,[22] mengantuk, berkeringat, mulut kering, sakit kepala, masalah kulit, lesu, iritasi saluran cerna, reaksi hipersensitivitas, masalah pergerakan, kekakuan otot, dan tremor.[15] Karena sinarizin dapat menyebabkan kantuk dan penglihatan kabur, penting bagi pengguna untuk memerhatikan kenormalan reaksi sebelum mengemudi, mengoperasikan mesin, atau melakukan pekerjaan lain yang dapat berbahaya jika mereka tidak sepenuhnya waspada atau tidak dapat melihat dengan baik.[6]
Sinarizin menyebabkan parkinsonisme akut dan kronis karena afinitasnya terhadap reseptor D2,[22] yang secara kuat membantah kegunaan sebenarnya untuk meningkatkan kesehatan neurologis. Efek antagonis sinarizin terhadap reseptor dopamin D2 di striatum menyebabkan gejala depresi, tremor, kekakuan otot, tardive diskinesia, dan akatisia. 17 dari 100 kasus parkinsonisme baru dikaitkan dengan pemberian sinarizin atau flunarizin.[5] Parkinsonisme yang disebabkan oleh obat-obatan adalah penyebab utama kedua dari parkinsonisme.[22] Bukti menunjukkan bahwa ini adalah salah satu metabolit sinarizin, yakni C-2, yang memiliki peran aktif dalam berkontribusi terhadap perkembangan parkinsonisme akibat obat.[3] Orang-orang yang paling berisiko adalah pasien lanjut usia, khususnya wanita, dan pasien yang telah mengonsumsi obat dalam jangka waktu yang lebih lama.[25] Ada juga bukti bahwa pasien dengan riwayat keluarga Parkinson atau kecenderungan genetik terhadap penyakit ini lebih mungkin mengembangkan bentuk penyakit ini yang disebabkan oleh obat sebagai akibat dari pengobatan sinarizin.[26]
Selain memusuhi reseptor D2, pengobatan dengan sinarizin menyebabkan berkurangnya dopamin dan serotonin prasinaptik, serta perubahan transpor dopamin vesikular. Pengobatan kronis dengan sinarizin membangun konsentrasi obat yang cukup tinggi sehingga mengganggu gradien elektrokimia proton yang diperlukan untuk mengemas dopamin ke dalam vesikel. Sinarizin, pKa = 7.4, bertindak sebagai protonofor, yang mencegah produksi gradien elektrokimia yang bergantung pada MgATP yang penting untuk pengangkutan dan penyimpanan dopamin ke dalam vesikel, dan dengan demikian menurunkan tingkat dopamin di neuron ganglia basal dan menyebabkan gejala Parkinson.[5]
Beberapa kasus overdosis sinarizin pada anak dan dewasa telah dilaporkan dengan efek termasuk berbagai gejala seperti mengantuk, koma, muntah, hipotonia, pingsan, dan kejang.[27] Komplikasi kognitif kemungkinan besar disebabkan oleh efek antihistaminik sinarizin, sedangkan efek motorik disebabkan oleh sifat antidopaminergik. Dalam kasus overdosis, pasien harus dibawa ke dan diobservasi di rumah sakit untuk mengetahui potensi komplikasi neurologis.
Farmakokinetik
Sinarizin paling sering dikonsumsi secara oral, dalam bentuk tablet, dengan frekuensi dan jumlah dosis yang bervariasi tergantung alasan minum obat. Setelah tertelan, zat tersebut diserap cukup cepat dan mencapai konsentrasi plasma puncak dalam 1-3 jam pasca pemberian.[28][4][29] Cmax, tingkat maksimum obat di area yang diuji (biasanya plasma darah), telah diukur sebesar 275 ± 36 ng/mL; tmax, waktu untuk mencapai konsentrasi maksimum, adalah 3,0 ± 0,5 jam.[4] AUC∞, yang dapat digunakan untuk memperkirakan bioavailabilitas, adalah 4437 ± 948 ng·h/mL.[4] Waktu paruh eliminasi bervariasi antara 3,4–60 jam, bergantung pada usia.[29] Namun, rata-rata waktu paruh terminal untuk subjek sukarelawan muda yang diberikan 75 mg sinarizin, ditemukan 23,6 ± 3,2 jam.[4]
Sebuah penelitian yang memberikan sinarizin dosis 75 mg, dua kali sehari selama dua belas hari, kepada sukarelawan sehat, mengamati bahwa sinarizin memang terakumulasi di dalam tubuh, dengan faktor akumulasi kondisi tetap sebesar 2,79 ± 0,23.[4] Namun, AUCT untuk jangka waktu tersebut (T=12 hari) tidak berbeda nyata dengan AUC∞ yang diperkirakan dari pemberian dosis tunggal. Sebagai senyawa basa yang sangat lemah dan juga lipofilik dengan kelarutan dalam air yang rendah, sinarizin mampu melewati sawar darah otak melalui difusi sederhana.[30][1] Karena sifat inilah ia mampu memberikan efeknya pada aliran darah otak di otak.[31]
Bioavailabilitas sinarizin yang diberikan secara oral biasanya rendah dan bervariasi karena tingginya insiden degradasi.[1] Namun, telah ditemukan bahwa ketika diberikan secara intravena dalam emulsi lipid, farmakokinetik dan distribusi jaringan yang lebih baik dapat dicapai. Pemberian emulsi lipid memiliki AUC yang lebih tinggi dan pembersihan yang lebih rendah dibandingkan bentuk larutan, yang berarti terdapat peningkatan bioavailabilitas sinarizin, yang memungkinkan peningkatan efek terapeutik. Farmakokinetik plasma sinarizin yang diberikan secara intravena mengikuti model tiga kompartemen, pertama dengan fase distribusi cepat, diikuti dengan fase distribusi lebih lambat, dan diakhiri dengan eliminasi sangat lambat. Vss (volume distribusi nyata keadaan tunak) untuk pemberian emulsi lipid adalah 2× lebih rendah (6,871 ± 1,432 L/kg) dibandingkan dengan sinarizin yang diberikan dalam larutan (14,018 ± 5,598 L/kg) dan ditemukan bahwa secara signifikan lebih sedikit sinarizin yang diserap ke dalam paru-paru dan otak dalam kondisi emulsi lipid.[32] Hal ini penting karena akan mengurangi kemungkinan efek samping toksik pada sistem saraf pusat.
Farmakodinamik
Sinarizin diklasifikasikan sebagai antagonis selektif saluran ion kalsium yang dioperasikan dengan tegangan tipe T, karena pengikatannya memblokir saluran dan membuatnya tetap inert.[2][25] Ia memiliki nilai Ki (konstanta penghambatan) sebesar 22 nM.[33] Ia juga diketahui memiliki efek antihistaminik, antiserotoninergik, dan antidopaminergik,[25] mengikat reseptor histamin H1, dan reseptor dopaminergik (D2).[3] IC50 (konsentrasi penghambatan setengah maksimal) sinarizin untuk penghambatan kontraksi otot polos adalah 60 mM[34] dan telah terbukti bahwa obat ini lebih disukai berikatan dengan saluran kalsium targetnya ketika saluran tersebut berada dalam keadaan terbuka, dibandingkan dengan konformasi tertutup.[35] Dalam pengobatan mual dan mabuk gerak, sebelumnya ada hipotesis bahwa sinarizin memberikan efeknya dengan menghambat arus kalsium dalam saluran gerbang tegangan pada sel rambut vestibular tipe II di telinga bagian dalam.[9] Namun, bukti yang lebih baru mendukung gagasan bahwa pada tingkat farmakologis yang relevan (0,3-0,5 μM), sinarizin tidak mengurangi vertigo vestibular dengan memblokir saluran kalsium, melainkan dengan menghambat arus kalium (K+) yang diaktifkan oleh peningkatan tekanan hidrostatik pada sel-sel rambut. Memang benar bahwa sinarizin juga menghilangkan arus kalsium dalam sel rambut vestibular; hanya saja hal ini hanya terjadi pada konsentrasi obat yang lebih tinggi (3 μM).[13] Penghambatan arus ini berfungsi untuk mengurangi vertigo dan mual akibat gerakan dengan meredam reaktivitas berlebihan sel-sel rambut vestibular, yang mengirimkan informasi tentang keseimbangan dan gerakan ke otak.
| Aksi sinarizin | Target Aksi |
|---|---|
| Antagonis saluran ion kalsium | Saluran kalsium tipe T |
| Antihistaminik | Reseptor H1 |
| Antiserotonergic | Reseptor 5-HT2[36] |
| Antidopaminergik | Reseptor D2 |
Eliminasi
Setelah pemberian, sinarizin dimetabolisme sepenuhnya di dalam tubuh dan metabolitnya dieliminasi sepertiganya melalui urin dan dua pertiganya melalui feses.[2]
Referensi
- ^ a b c Kalava SB, Demirel M, Yazan Y (2005). "Physicochemical characterization and dissolution properties of cinnarizine solid dispersions". Turish Journal of Pharmaceutical Sciences (dalam bahasa Turki). 2 (2): 51–62.
- ^ a b c d e f Deka, C.V.R. (2006). "Role of Cinnarizine in Peripheral Vertigo". Vertigo Viewpoint. 4 (1): 2–4.
- ^ a b c Kariya S, Isozaki S, Masubuchi Y, Suzuki T, Narimatsu S (November 1995). "Possible pharmacokinetic and pharmacodynamic factors affecting parkinsonism inducement by cinnarizine and flunarizine". Biochemical Pharmacology. 50 (10): 1645–50. doi:10.1016/0006-2952(95)02057-8. PMID 7503767.
- ^ a b c d e f Castañeda-Hernández G, Vargas-Alvarado Y, Aguirre F, Flores-Murrieta FJ (May 1993). "Pharmacokinetics of cinnarizine after single and multiple dosing in healthy volunteers". Arzneimittel-Forschung. 43 (5): 539–42. PMID 8328998.
- ^ a b c d Terland O, Flatmark T (June 1999). "Drug-induced parkinsonism: cinnarizine and flunarizine are potent uncouplers of the vacuolar H+-ATPase in catecholamine storage vesicles". Neuropharmacology. 38 (6): 879–82. doi:10.1016/s0028-3908(98)00233-0. PMID 10465691.
- ^ a b c d Nicholson AN, Stone BM, Turner C, Mills SL (June 2002). "Central effects of cinnarizine: restricted use in aircrew". Aviation, Space, and Environmental Medicine. 73 (6): 570–4. PMID 12056673.
- ^ Wilder-Smith CH, Schimke J, Osterwalder B, Senn HJ (1991). "Cinnarizine for prevention of nausea and vomiting during platin chemotherapy". Acta Oncologica. 30 (6): 731–4. doi:10.3109/02841869109092448
 . PMID 1958394.
. PMID 1958394.
- ^ a b c Pianese CP, Hidalgo LO, González RH, Madrid CE, Ponce JE, Ramírez AM, Morán LM, Arenas JE, Rubio AT, Uribe JO, Abiuso J, Hanuch E, Alegría J, Volpi C, Flaskamp R, Sanjuán AP, Gómez JM, Hernández J, Pedraza A, Quijano D, Martínez C, Castañeda JR, Guerra OJ, F GV (May 2002). "New approaches to the management of peripheral vertigo: efficacy and safety of two calcium antagonists in a 12-week, multinational, double-blind study". Otology & Neurotology. 23 (3): 357–63. doi:10.1097/00129492-200205000-00023. PMID 11981396.
- ^ a b c Arab SF, Düwel P, Jüngling E, Westhofen M, Lückhoff A (June 2004). "Inhibition of voltage-gated calcium currents in type II vestibular hair cells by cinnarizine". Naunyn-Schmiedeberg's Archives of Pharmacology. 369 (6): 570–5. doi:10.1007/s00210-004-0936-3. PMID 15138660.
- ^ "The use of stems in the selection of International Nonproprietary Names (INN) for pharmaceutical substances 2011" (PDF). WHO. Diakses tanggal 2015-03-12.
- ^ Lucertini M, Mirante N, Casagrande M, Trivelloni P, Lugli V (May 2007). "The effect of cinnarizine and cocculus indicus on simulator sickness". Physiology & Behavior. 91 (1): 180–90. doi:10.1016/j.physbeh.2007.02.008. PMID 17434541.
- ^ Ganança MM, Caovilla HH, Munhoz MS, Ganança CF, da Silva ML, Serafini F, Ganança FF (2007). "Optimizing the pharmacological component of integrated balance therapy". Brazilian Journal of Otorhinolaryngology. 73 (1): 12–8. doi:10.1016/s1808-8694(15)31116-2
 . PMC 9443544
. PMC 9443544  Periksa nilai
Periksa nilai |pmc=(bantuan). PMID 17505593. - ^ a b Haasler T, Homann G, Duong Dinh TA, Jüngling E, Westhofen M, Lückhoff A (December 2009). "Pharmacological modulation of transmitter release by inhibition of pressure-dependent potassium currents in vestibular hair cells". Naunyn-Schmiedeberg's Archives of Pharmacology. 380 (6): 531–8. doi:10.1007/s00210-009-0463-3. PMID 19830405.
- ^ Yates BJ, Miller AD, Lucot JB (November 1998). "Physiological basis and pharmacology of motion sickness: an update". Brain Research Bulletin. 47 (5): 395–406. doi:10.1016/s0361-9230(98)00092-6. PMID 10052567.
- ^ a b "Stugeron 15". NHS. Diarsipkan dari versi asli tanggal 2012-05-07. Diakses tanggal 2012-10-21.
- ^ Gil A, Nachum Z, Tal D, Shupak A (2012). "A comparison of cinnarizine and transdermal scopolamine for the prevention of seasickness in naval crew: a double-blind, randomized, crossover study". Clinical Neuropharmacology. 35 (1): 37–9. doi:10.1097/WNF.0b013e31823dc125. PMID 22139622.
- ^ Arieli R, Shupak A, Shachal B, Shenedrey A, Ertracht O, Rashkovan G (1999). "Effect of the anti-motion-sickness medication cinnarizine on central nervous system oxygen toxicity". Undersea & Hyperbaric Medicine. 26 (2): 105–9. PMID 10372430.
- ^ Emanuel MB, Chamberlain JA, Whiting S, Rigden BG, Craven AH (February 1979). "Cinnarizine in the treatment of chronic asthma". British Journal of Clinical Pharmacology. 7 (2): 189–95. doi:10.1111/j.1365-2125.1979.tb00920.x. PMC 1429430
 . PMID 367414.
. PMID 367414.
- ^ Saletu B, Grünberger J (1980). "Antihypoxidotic and nootropic drugs: proof of their encephalotropic and pharmacodynamic properties by quantitative EEG investigations". Progress in Neuro-Psychopharmacology. 4 (4–5): 469–89. doi:10.1016/0364-7722(80)90017-x. PMID 7012879.
- ^ Towse G (September 1980). "Cinnarizine--a labyrinthine sedative". The Journal of Laryngology and Otology. 94 (9): 1009–15. doi:10.1017/s0022215100089787. PMID 7000939.
- ^ RomPharm. Pyracin (piractam 400 mg and cinnarizine 25 mg). 2008 [cited 2012 10/20].
- ^ a b c d Teive HA, Troiano AR, Germiniani FM, Werneck LC (June 2004). "Flunarizine and cinnarizine-induced parkinsonism: a historical and clinical analysis". Parkinsonism & Related Disorders. 10 (4): 243–5. doi:10.1016/j.parkreldis.2003.12.004. PMID 15120099.
- ^ Poignet H, Beaughard M, Lecoin G, Massingham R (October 1989). "Functional, behavioral, and histological changes induced by transient global cerebral ischemia in rats: effects of cinnarizine and flunarizine". Journal of Cerebral Blood Flow and Metabolism. 9 (5): 646–54. doi:10.1038/jcbfm.1989.92
 . PMID 2777934.
. PMID 2777934.
- ^ Tosoni C, Lodi-Rizzini F, Cinquini M, Pasolini G, Venturini M, Sinico RA, Calzavara-Pinton P (March 2009). "A reassessment of diagnostic criteria and treatment of idiopathic urticarial vasculitis: a retrospective study of 47 patients". Clinical and Experimental Dermatology. 34 (2): 166–70. doi:10.1111/j.1365-2230.2008.02891.x. PMID 18681869.
- ^ a b c Fabiani G, Pastro PC, Froehner C (September 2004). "Parkinsonism and other movement disorders in outpatients in chronic use of cinnarizine and flunarizine". Arquivos de Neuro-Psiquiatria. 62 (3B): 784–8. doi:10.1590/S0004-282X2004000500008
 . PMID 15476069.
. PMID 15476069.
- ^ Serrano A, Menéndez J, Casarejos MJ, Solano RM, Gallego E, Sánchez M, et al. (August 2005). "Effects of cinnarizine, a calcium antagonist that produces human parkinsonism, in parkin knock out mice". Neuropharmacology. 49 (2): 208–219. doi:10.1016/j.neuropharm.2005.03.003. PMID 15993444.
- ^ Turner D, Lurie Y, Finkelstein Y, Schmid T, Gopher A, Kleid D, Bentur Y (May 2006). "Pediatric cinnarizine overdose and toxicokinetics" (PDF). Pediatrics. 117 (5): e1067–9. CiteSeerX 10.1.1.566.5819
 . doi:10.1542/peds.2005-2059. PMID 16636115.
. doi:10.1542/peds.2005-2059. PMID 16636115.
- ^
Spagnoli A, Tognoni G (July 1983). "'Cerebroactive' drugs. Clinical pharmacology and therapeutic role in cerebrovascular disorders". Drugs. 26 (1): 44–69. doi:10.2165/00003495-198326010-00003
 . PMID 6349963.
. PMID 6349963.
- ^ a b Nowacka-Krukowska H, Rakowska M, Neubart K, Kobylińska M (2007). "High-performance liquid chromatographic assay for cinnarizine in human plasma". Acta Poloniae Pharmaceutica. 64 (5): 407–11. PMID 18540159.
- ^ Kornhuber J, Henkel AW, Groemer TW, Städtler S, Welzel O, Tripal P, Rotter A, Bleich S, Trapp S (July 2010). "Lipophilic cationic drugs increase the permeability of lysosomal membranes in a cell culture system". Journal of Cellular Physiology. 224 (1): 152–64. doi:10.1002/jcp.22112. PMID 20301195.
- ^ Emanuel MB (July 1979). "Specific calcium antagonists in the treatment of peripheral vascular disease". Angiology. 30 (7): 454–69. doi:10.1177/000331977903000704. PMID 464337.
- ^ Shi S, Chen H, Lin X, Tang X (January 2010). "Pharmacokinetics, tissue distribution and safety of cinnarizine delivered in lipid emulsion". International Journal of Pharmaceutics. 383 (1–2): 264–70. doi:10.1016/j.ijpharm.2009.09.025. PMID 19770029.
- ^ Klein M, Musacchio JM (October 1989). "High affinity dextromethorphan binding sites in guinea pig brain. Effect of sigma ligands and other agents". The Journal of Pharmacology and Experimental Therapeutics. 251 (1): 207–15. PMID 2477524.
- ^ Silver PJ, Dachiw J, Ambrose JM, Pinto PB (September 1985). "Effects of the calcium antagonists perhexiline and cinnarizine on vascular and cardiac contractile protein function". The Journal of Pharmacology and Experimental Therapeutics. 234 (3): 629–35. PMID 3162016.
- ^ López MG, Moro MA, Castillo CF, Artalejo CR, García AG (March 1989). "Variable, voltage-dependent, blocking effects of nitrendipine, verapamil, diltiazem, cinnarizine and cadmium on adrenomedullary secretion". British Journal of Pharmacology. 96 (3): 725–31. doi:10.1111/j.1476-5381.1989.tb11874.x. PMC 1854390
 . PMID 2720300.
. PMID 2720300.
- ^ Pukhal'skaya TG, Kolosova OA, Men'shikov MY, Vein AM (July 2000). "Effects of calcium antagonists on serotonin-dependent aggregation and serotonin transport in platelets of patients with migraine". Bulletin of Experimental Biology and Medicine. 130 (7): 633–5. doi:10.1007/BF02682090. PMID 11140571.
Pranala Luar
![]() Media tentang Cinnarizine di Wikimedia Commons
Media tentang Cinnarizine di Wikimedia Commons
