Spektrum pancar


Spektrum pancar atau spektrum emisi unsur kimia atau senyawa kimia merupakan spektrum frekuensi dari radiasi elektromagnetik yang dipancarkan karena adanya atom atau molekul membuat transisi dari keadaan energi tinggi ke keadaan energi yang lebih rendah. Energi foton yang dipancarkan foton adalah sama dengan perbedaan energi antara kedua keadaan. Ada banyak kemungkinan transisi elektron untuk masing-masing atom, dan setiap transisi memiliki perbedaan energi spesifik. Kumpulan transisi yang berbeda ini, yang menyebabkan perbedaan panjang gelombang yang dipancarkan, sehingga membuat sebuah spektrum emisi. Masing-masing spektrum emisi unsur adalah unik. Oleh karena itu, spektroskopi dapat digunakan untuk mengidentifikasi unsur-unsur dalam bahan yang tidak diketahui komposisinya. Demikian pula, spektrum emisi molekul dapat digunakan dalam analisis kimia suatu zat.
Emisi
[sunting | sunting sumber]Dalam fisika, emisi adalah suatu proses ketika suatu partikel yang berada pada keadaan energi mekanika kuantum yang lebih tinggi berubah ke keadaan yang lebih rendah melalui emisi foton, sehingga menghasilkan cahaya. Frekuensi cahaya yang dipancarkan adalah fungsi dari energi transisi. Sesuai dengan hukum kekekalan energi, perbedaan antara kedua keadaan sama dengan energi yang dibawa oleh foton. Keadaan energi transisi dapat menyebabkan emisi dengan rentang frekuensi yang lebar. Misalnya, sinar tampak yang dipancarkan oleh keadaan elektronik dalam atom dan molekul (kemudian fenomena ini disebut fluoresensi atau fosforesensi). Sebaliknya, transisi kelopak nuklir dapat memancarkan sinar gamma berenergi tinggi, sementara transisi spin nuklir memancarkan gelombang radio berenergi rendah.
Pancaran sinar suatu objek menjadi ukuran jumlah cahaya yang dipancarkannya. Ini dapat terkait dengan sifat lain objek tersebut melalui hukum Stefan–Boltzmann. Untuk sebagian besar zat, jumlah emisi bervariasi sesuai suhu dan komposisi spektroskopik obyeknya, sehingga menyebabkan penampakan suhu warna dan garis emisi. Pengukuran yang tepat pada banyak panjang gelombang memungkinkan identifikasi zat melalui spektroskopi emisi.
Emisi radiasi biasanya dijelaskan menggunakan mekanika kuantum semi klasik: tingkat energi partikel dan jarak ditentukan dari mekanika kuantum, dan cahaya diperlakukan sebagai medan listrik berosilasi yang dapat mendorong transisi jika berada dalam resonansi dengan frekuensi alami sistem. Masalah mekanik kuantum diberi perlakuan dengan menggunakan teori perturbasi tergantung waktu dan menyebabkan hasil umum yang dikenal sebagai aturan emas Fermi. Deskripsi ini telah digantikan oleh elektrodinamika kuantum, walaupun versi semi klasik tetap lebih berguna dalam perhitungan yang paling praktis.
Asal-usul
[sunting | sunting sumber]Ketika elektron dalam atom tereksitasi, misalnya dengan dipanaskan, energi tambahan akan mendorong elektron ke orbital berenergi lebih tinggi. Ketika elektron turun kembali dan meninggalkan keadaan tereksitasi, energi dipancarkan kembali dalam bentuk foton. Panjang gelombang (atau ekuivalen, frekuensi) foton ditentukan oleh perbedaan energi antara kedua keadaan. Foton yang dipancarkan ini membentuk spektrum unsur.
Fakta bahwa hanya warna-warna tertentu yang muncul dalam emisi spektrum atom suatu unsur berarti bahwa hanya frekuensi tertentu dari cahaya yang dipancarkan. Masing-masing frekuensi ini berkaitan dengan energi sesuai rumus:
- ,
dengan adalah energi foton, adalah frekuensi, dan adalah konstanta Planck. Ini menyimpulkan bahwa hanya foton dengan energi tertentu yang dipancarkan oleh atom. Prinsip dari spektrum emisi atom menjelaskan beragam warna papan neon, serta hasil uji nyala bahan kimia (dijelaskan di bawah).
Frekuensi cahaya yang dapat dipancarkan oleh atom bergantung pada keadaan elektron di dalamnya. Ketika tereksitasi, sebuah elektron berpindah ke tingkat energi atau orbital yang lebih tinggi. Ketika elektron jatuh kembali ke keadaan dasar, ia memancarkan cahaya.

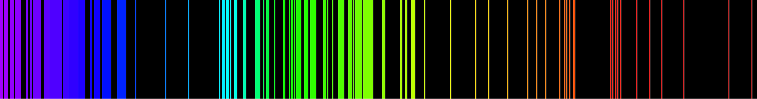
Gambar di atas tersebut menunjukkan spektrum emisi hidrogen sinar tampak. Jika hanya satu atom hidrogen yang ada, maka hanya satu panjang gelombang yang akan teramati pada saat tertentu. Beberapa kemungkinan emisi teramati karena sampel mengandung banyak atom hidrogen dengan keadaan energi awal yang berbeda dan mencapai keadaan energi akhir yang berbeda pula. Kombinasi yang berbeda ini menyebabkan emisi simultan pada panjang gelombang yang berbeda.
Radiasi dari molekul
[sunting | sunting sumber]Seperti transisi elektronik yang dibahas di atas, energi dari molekul juga dapat berubah melalui transisi rotasi, vibrasi, dan vibronik (gabungan vibrasional dan elektronik). Energi transisi ini sering menyebabkan rapatnya jarak antar kelompok garis spektrum yang berbeda, yang dikenal sebagai pita spektrum. Pita spektrum yang belum terpecahkan mungkin muncul sebagai spektrum kontinum.
Spektroskopi emisi
[sunting | sunting sumber]Cahaya terdiri dari radiasi elektromagnetik dari panjang gelombang yang berbeda. Oleh karena itu, ketika unsur-unsur atau senyawanya dipanaskan di atas api atau busur listrik mereka memancarkan energi dalam bentuk cahaya. Analisis dari cahaya ini, dengan bantuan spektroskop, memberi kita spektrum diskontinu. Spektroskop atau spektrometer adalah alat yang digunakan untuk memisahkan komponen cahaya yang memiliki panjang gelombang yang berbeda. Spektrum muncul dalam serangkaian garis yang disebut garis spektrum. Garis spektrum ini disebut spektrum atom ketika ia berasal dari sebuah atom dalam bentuk unsur. Setiap unsur memiliki spektrum atom yang berbeda. Pembentukan garis spektrum oleh atom-atom suatu unsur menunjukkan bahwa atom dapat memancarkan energi hanya dalam jumlah tertentu. Ini mengarah pada kesimpulan bahwa elektron terikat bukan tidak memiliki sejumlah energi tetapi hanya sejumlah energi tertentu.
Spektrum emisi dapat digunakan untuk menentukan komposisi material, karena ia berbeda untuk masing-masing unsur dalam tabel periodik. Salah satu contohnya adalah spektroskopi astronomi: mengidentifikasi komposisi bintang melalui analisis sinar yang diterima. Karakteristik spektrum emisi beberapa unsur terlihat jelas dengan mata telanjang ketika unsur-unsur ini dipanaskan. Misalnya, ketika kawat platina dicelupkan ke dalam larutan stronsium nitrat dan dikenakan nyala api, atom stronsium akan memancarkan warna merah. Serupa dengan stronsium, ketika tembaga dikenakan nyala api, nyala api akan berwarna hijau. Karakteristik khas ini memungkinkan unsur-unsur diidentifikasi melalui spektrum emisi atomnya. Tidak semua sinar yang diemisikan dapat diterima mata telanjang, karena spektrum juga mencakup sinar ultraviolet dan inframerah. Suatu emisi terbentuk ketika gas yang tereksitasi dilihat langsung melalui spektroskop.

Spektroskopi emisi adalah teknik spektroskopi yang mempelajari panjang gelombang foton yang dipancarkan oleh atom atau molekul selama transisi dari keadaan tereksitasi ke tingkat energi yang lebih rendah. Setiap unsur memancarkan seperangkat panjang gelombang diskrit yang spesifik sesuai dengan struktur elektron, dan dengan mengamati panjang gelombang ini komposisi unsur dalam sampel dapat ditentukan. Spektroskopi emisi dikembangkan di akhir abad ke-19 dan upaya-upaya dalam penjelasan teoretis tentang spektrum emisi atom mengarahkan pada mekanika kuantum.
Ada banyak cara atom naik ke keadaan tereksitasi. Interaksi dengan radiasi elektromagnetik digunakan dalam spektroskopi fluoresensi, proton atau partikel yang lebih berat lainnya dalam emisi sinar X induksi partikel, dan elektron atau foton sinar X dalam spektroskopi sinar X energi terdispersi atau fluoresensi sinar X. Metode paling sederhana adalah memanaskan sampel hingga suhu tinggi, sehingga eksitasi terbentuk melalui tumbukan antar atom sampel. Metode ini digunakan dalam spektroskopi emisi nyala, dan merupakan metode yang digunakan oleh Anders Jonas Ångström ketika ia menemukan fenomena garis emisi diskrit pada tahun 1850-an.[1]
Meskipun garis emisi disebabkan oleh transisi antara keadaan energi terkuantisasi dan dapat sangat tajam pada awalnya, mereka memiliki lebar tertentu, yaitu mereka tersusun atas lebih dari satu panjang gelombang cahaya. Perluasan garis spektrum ini memiliki beragam penyebab.
Spektroskopi emisi sering kali dirujuk sebagai spektroskopi emisi optik karena sifat cahaya yang dipancarkan.
Sejarah
[sunting | sunting sumber]Garis emisi dari gas panas pertama kali ditemukan[butuh rujukan] oleh Ångström, dan teknik ini dikembangkan lebih lanjut oleh David Alter, Gustav Kirchhoff dan Robert Bunsen.
Lihat sejarah spektroskopi untuk lebih jelasnya.
Teknik eksperimen spektroskopi emisi nyala
[sunting | sunting sumber]Larutan yang mengandung zat yang akan dianalisis ditarik ke dalam pembakar dan didispersikan ke dalam api sebagai semprotan butiran halus. Pelarut menguap lebih dulu, meninggalkan halus partikel padat halus yang bergeser ke wilayah terpanas nyala api di mana dihasilkan atom dan ion gas. Di sini, elektron tereksitasi seperti dijelaskan di atas. Merupakan kelaziman menggunakan monokromator untuk memudahkan deteksi.
Pada tingkat sederhana, spektroskopi emisi nyala dapat diamati menggunakan nyala api dan sampel garam logam. Metode analisis kualitatif ini disebut uji nyala api. Misalnya, natrium garam yang ditaruh dalam nyala api akan menyala kuning yang berasal dari ion natrium, sementara ion stronsium (yang digunakan pada suar jalan) memberi warna merah. Kawat tembaga kawat akan membuat nyala api berwarna biru, namun dengan adanya klorida memberikan warna hijau (kontribusi molekuler oleh CuCl).
Koefisien emisi
[sunting | sunting sumber]Koefisien emisi adalah koefisien daya output per satuan waktu suatu sumber elektromagnetik, suatu nilai hitung dalam fisika. Koefisien emisi gas bervariasi sesuai panjang gelombang cahaya. Ia memiliki satuan ms−3sr−1.[2] Ini juga digunakan sebagai ukuran emisi lingkungan (berdasarkan massa) per MWh pembangkit listrik, lihat: faktor emisi.
Hamburan cahaya
[sunting | sunting sumber]Dalam hamburan Thomson partikel bermuatan memancarkan radiasi di bawah cahaya yang jatuh. Partikel mungkin elektron biasa, sehingga koefisien emisi memiliki aplikasi praktis.
Jika X dV dΩ dλ adalah energi yang dihamburkan oleh unsur volume dV ke sudut padatan dΩ antara panjang gelombang λ dan λ+dλ per satuan waktu maka koefisien Emisi adalah X.
Nilai X dalam hamburan Thomson dapat diprediksi dari insiden flux, kepadatan partikel bermuatan dan diferensial penampang Thomsonnya (area/sudut padatan).
Emisi spontan
[sunting | sunting sumber]Badan hangat memancarkan foton yang memiliki koefisien emisi monokromatik yang berkaitan dengan suhu dan daya radiasi total. Hal ini kadang-kadang disebut koefisien Einstein kedua, dan dapat disimpulkan dari teori mekanika kuantum.
Lihat juga
[sunting | sunting sumber]- Tabel emisi spektrum dari lampu pelepasan gas
- Garis spektral atom
- Formula Rydberg
- Garis-garis Fraunhofer
- Pergeseran isotop
- Pergeseran isomer
- Penyerapan spektrum
- Spektroskopi elektromagnetik
- Spektroskopi penyerapan
- Persamaan Dioda meliputi koefisien emisi
- Fisika plasma
- Koefisien emisi koefisien ini juga diberikan untuk emisi elektron balistik sekunder.
- Luminous koefisien
- Garis spektral
- Teori spektral
Referensi
[sunting | sunting sumber]- ^ Incorporated, SynLube. "Spectroscopy Oil Analysis". www.synlube.com (dalam bahasa Inggris). Diakses tanggal 2017-02-24.
- ^ Carroll, Bradley W. (2007). An Introduction to Modern Astrophysics. CA, USA: Pearson Education. hlm. 256. ISBN 0-8053-0402-9.
Pranala luar
[sunting | sunting sumber]- Emission spectra of atmospheric gases Diarsipkan 2013-03-25 di Wayback Machine.
- NIST Physical Reference Data—Atomic Spectroscopy Data
- Color Simulation of Element Emission Spectrum Based on NIST data Diarsipkan 2006-11-10 di Wayback Machine.
- Hydrogen emission spectrum Diarsipkan 2008-11-20 di Wayback Machine.
- Emissions Spectrum Java Applet Diarsipkan 2015-02-15 di Wayback Machine.
- Astrophysics lecture slides on the emission coefficient Diarsipkan 2010-04-01 di Wayback Machine. from University of Chicago.

