Radon
| Radon | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
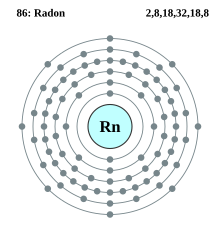 Konfigurasi elektron radon | ||||||||||||||||||||||||||||
Garis spektrum radon | ||||||||||||||||||||||||||||
| Sifat umum | ||||||||||||||||||||||||||||
| Nama, lambang | radon, Rn | |||||||||||||||||||||||||||
| Pengucapan | /radon/[1] | |||||||||||||||||||||||||||
| Penampilan | gas tak berwarna | |||||||||||||||||||||||||||
| Radon dalam tabel periodik | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Nomor atom (Z) | 86 | |||||||||||||||||||||||||||
| Golongan | golongan 18 (gas mulia) | |||||||||||||||||||||||||||
| Periode | periode 6 | |||||||||||||||||||||||||||
| Blok | blok-p | |||||||||||||||||||||||||||
| Kategori unsur | gas mulia | |||||||||||||||||||||||||||
| Nomor massa | [222] | |||||||||||||||||||||||||||
| Konfigurasi elektron | [Xe] 4f14 5d10 6s2 6p6 | |||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 32, 18, 8 | |||||||||||||||||||||||||||
| Sifat fisik | ||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | gas | |||||||||||||||||||||||||||
| Titik lebur | 202,0 K (−71,15 °C, −96,07 °F) | |||||||||||||||||||||||||||
| Titik didih | 211,5 K (−61,7 °C, −79,1 °F) | |||||||||||||||||||||||||||
| Kerapatan (pada STS) | 9,73 g/L | |||||||||||||||||||||||||||
| saat cair, pada t.d. | 4,4 g/cm3 | |||||||||||||||||||||||||||
| Titik kritis | 377 K, 6,28 MPa[2] | |||||||||||||||||||||||||||
| Kalor peleburan | 3,247 kJ/mol | |||||||||||||||||||||||||||
| Kalor penguapan | 18,10 kJ/mol | |||||||||||||||||||||||||||
| Kapasitas kalor molar | 5R/2 = 20,786 J/(mol·K) | |||||||||||||||||||||||||||
Tekanan uap
| ||||||||||||||||||||||||||||
| Sifat atom | ||||||||||||||||||||||||||||
| Bilangan oksidasi | 0, +2, +6 | |||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 2,2 | |||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 1037 kJ/mol | |||||||||||||||||||||||||||
| Jari-jari kovalen | 150 pm | |||||||||||||||||||||||||||
| Jari-jari van der Waals | 220 pm | |||||||||||||||||||||||||||
| Lain-lain | ||||||||||||||||||||||||||||
| Kelimpahan alami | dari peluruhan | |||||||||||||||||||||||||||
| Struktur kristal | kubus berpusat muka (fcc) | |||||||||||||||||||||||||||
| Konduktivitas termal | 3,61×10−3 W/(m·K) | |||||||||||||||||||||||||||
| Arah magnet | nonmagnetik | |||||||||||||||||||||||||||
| Nomor CAS | 10043-92-2 | |||||||||||||||||||||||||||
| Sejarah | ||||||||||||||||||||||||||||
| Penemuan | E. Rutherford dan Robert B. Owens (1899) | |||||||||||||||||||||||||||
| Isolasi pertama | W. Ramsay dan R. Whytlaw-Gray (1910) | |||||||||||||||||||||||||||
| Isotop radon yang utama | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
Radon adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Rn dan nomor atom 86. Radon juga termasuk dalam kelompok gas mulia dan beradioaktif. Radon terbentuk dari penguraian radium. Radon juga gas yang paling berat dan berbahaya bagi kesehatan. Rn-222 mempunyai waktu paruh 3,8 hari dan digunakan dalam radioterapi. Radon dapat memicu kanker paru paru dan telah menyebabkan 20.000 kematian di Uni Eropa setiap tahunnya.
Karakteristik
Radon tidak mudah bereaksi secara kimia, tetapi beradioaktif, radon juga adalah gas alami (senyawa gas terberat adalah tungsten heksaflorida, WF6). Pada suhu dan tekanan ruang, radon tidak berwarna tetapi apabila didinginkan hingga membeku, radon akan berwarna kuning, sedang kan radon cair berwarna merah jingga.
Penumpukan gas Radon secara alamiah di atmosfer bumi terjadi amat perlahan sehingga air yang menyentuh udara bebas terus kehilangan Radon karena proses “Volatilisasi. Air bawah tanah mempunyai kandungan Radon lebih tinggi di bandingkan air permukaan.
Kegunaan
Radon kadang digunakan oleh beberapa rumah sakit untuk kegunaan terapeutik. Radon tersebut di peroleh dengan pemompaan dari sumber Radium dan disimpan dalam tabung kecil yang disebut ‘’benih’’ atau ‘’jarum’’. Radon sudah jarang digunakan lagi namun, mengingat rumah sakit sekarang bisa mendapatkan benih dari ‘’supplier’’ yang menghasilkan benih dengan tingkat peluruhan yang dikehendaki. biasanya digunakan kobalt dan caesium yang tahan selama beberapa tahun, sehingga lebih praktis ditinjau dari segi logistik.
Karena peluruhannya yang cukup cepat, radon juga digunakan dalam penyelidikan hidrologi yang mengkaji interaksi antara air bawah tanah, anak sungai dan sungai. Peningkatan radon dalam anak sungai atau sungai merupakan petunjuk penting bahwa terdapat sumber air bawah tanah.
Sejarah
Nama radon berasal dari radium. Radon ditemukan pada tahun 1900 oleh Friedrich Ernst Dorn, yang menggelarnya sebagai pancaran radium. Pada tahun 1908 William Ramsay dan Robert Whytlaw-Gray, yang menamakannya niton (dari bahasa latin nitens berarrti "yang berkilauan"; simbol Nt), mengisolasinya, menentukan kepadatannya dan mereka menemukan bahwa Radon adalah gas paling berat pada masa itu (dan sampai sekarang). Semenjak 1923 unsur 87 ini disebut Radon.
Sumber
Rata rata, terdapat satu molekul radon dalam 1 x 1021 molekul udara. Radon dapat ditemukan di beberapa mata air dan mata air panas. Kota Misasa, Jepang, terkenal karena mata airnya yang kaya dengan radium yang menghasilkan radon.
Radon dibebaskan dari tanah secara alamiah, apalagi di kawasan bertanah di Granit. Radon juga mungkin dapat berkumpul di ruang bawah tanah dan tempat tinggal (Namun ini juga bergantung bagaimana rumah itu di rawat dan ventilasinya) Uni Eropa mennentukan bahwa batas aman kandungan radon adalah 400 Bq/meter3 untuk rumah lama, dan 200 Bq/m3 untuk rumah baru. ‘’Environmental Protection Agency’’ Amerika mennyarankan untuk melakukan tindakan segera bagi semua rumah dengan kepekatan Radon melebihi 148 Bq/m3 (diukur sebagai4 pCi/L). Hampir satu rumah setiap 15 di A.S. mempunyai kadar radon yang tinggi menurut statistik (U.S. Surgeon General) dan EPA mencadangkan agar semua rumah diuji bagi radon. Sejak 1985 di Amerika, jutaan rumah telah diuji kandungan radonnya.
Persenyawaan
Pengujian menunjukkan bahwa flor dapat bereaksi dengan radon dan membentuk senyawa radon florida. Senyawa radon klathrat juga pernah ditemukan.
Isotop
Diketahui ada dua puluh Isotop radon yang diketahui. Yang paling stabil adalah Rn-222 yang merupakan produk sampingan dari peluruhan radium-236, Rn-222 mempunyai waktu parah 3,823 hari (330.307,2 detik) dan memancarkan partikel alpha. Rn-220 adalah produk sampingan dari peluruhan thorium dan disebut thoron. Waktu paruhnya 55.6 dan juga memancarkan sinar Alfa. Radon-219 diturunkan dari actinium.
Tindakan Pencegahan
Radon adalah gas karsinogen. Radon adalah bahan beradioaktif dan harus ditangai secara hati-hati. Adalah sangat berbahaya untuk menghirup unsur ini karena Radon menghasilkan partikel alpha.
Radon juga menghasilkan hasil peluruhan berbentuk padat, dan akibatnya, cenderung membentuk debu halus yang mudah memasuki jalur udara dan melekat permanen dalam jaringan paru-paru, menghasilkan paparan lokal yang parah. Ruang di mana radium, aktinium, atau thorium disimpan perlu diangin-anginkan dengan baik agar tidak terakumulasi dalam udara. Akumulai radon berpontensi mengancam kesehatan dalam tambang uranium dan timah hitam. Pengumpulan radon dalam rumah juga merupakan suatu penemuan yang cukup baru dan kebanyakan penyakit kanker paru-paru dikaitkan dengan pengumpulan radon setiap tahun. Radon dalam rumah dianggarkan menyebabkan kematian akibat kanker paru-paru sekitar 21,000 orang setiap tahun di U.S. Radon adalah penyebab utama kanker paru-paru di U.S. hari ini.
Referensi
- ^ (Indonesia) "Radon". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (edisi ke-92). Boca Raton, FL: CRC Press. hlm. 4.122. ISBN 1439855110.
Daftar Pustaka
- Los Alamos National Laboratory - Radon
- Cancer Research UK study and building procedures to mitigate risks.
- Leonard A. Cole, Element of Risk: The Politics of Radon (American Association for the Advancement of Science Press, 1993). (a scholarly source critical of U.S. and EPA domestic radon policy)
Pranala luar
- WebElements.com - Radon
- EnvironmentalChemistry.com - Radon
- Indoor Air - Radon (Rn)
- Radon Brochure SCK.CEN Belgian Nuclear Research Centre, Mol, Belgium
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


