Rubidium
37Rb Rubidium | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Sampel rubidium di dalam ampul kaca | |||||||||||||||||||||||||||||||||||||||||
Garis spektrum rubidium | |||||||||||||||||||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||||||||||||||||||
| Pengucapan | /rubidium/[1] | ||||||||||||||||||||||||||||||||||||||||
| Penampilan | abu-abu putih | ||||||||||||||||||||||||||||||||||||||||
| Rubidium dalam tabel periodik | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 37 | ||||||||||||||||||||||||||||||||||||||||
| Golongan | golongan 1 (logam alkali) | ||||||||||||||||||||||||||||||||||||||||
| Periode | periode 5 | ||||||||||||||||||||||||||||||||||||||||
| Blok | blok-s | ||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | logam alkali | ||||||||||||||||||||||||||||||||||||||||
| Berat atom standar (Ar) |
| ||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Kr] 5s1 | ||||||||||||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 8, 1 | ||||||||||||||||||||||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | ||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 312,45 K (39,30 °C, 102,74 °F) | ||||||||||||||||||||||||||||||||||||||||
| Titik didih | 961 K (688 °C, 1270 °F) | ||||||||||||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 1,532 g/cm3 | ||||||||||||||||||||||||||||||||||||||||
| saat cair, pada t.l. | 1,46 g/cm3 | ||||||||||||||||||||||||||||||||||||||||
| Titik tripel | 312,41 K, ? kPa[2] | ||||||||||||||||||||||||||||||||||||||||
| Titik kritis | 2093 K, 16 MPa (diekstrapolasi)[2] | ||||||||||||||||||||||||||||||||||||||||
| Kalor peleburan | 2,19 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Kalor penguapan | 69 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 31,060 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | −1, +1 (oksida basa kuat) | ||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 0,82 | ||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 403 kJ/mol ke-2: 2632,1 kJ/mol ke-3: 3859,4 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 248 pm | ||||||||||||||||||||||||||||||||||||||||
| Jari-jari kovalen | 220±9 pm | ||||||||||||||||||||||||||||||||||||||||
| Jari-jari van der Waals | 303 pm | ||||||||||||||||||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||||||||||||||||||
| Kelimpahan alami | primordial | ||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | kubus berpusat badan (bcc) | ||||||||||||||||||||||||||||||||||||||||
| Kecepatan suara batang ringan | 1300 m/s (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||
| Ekspansi kalor | 90 µm/(m·K)[3] (pada s.k.) | ||||||||||||||||||||||||||||||||||||||||
| Konduktivitas termal | 58,2 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||
| Resistivitas listrik | 128 nΩ·m (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||
| Arah magnet | paramagnetik[4] | ||||||||||||||||||||||||||||||||||||||||
| Suseptibilitas magnetik molar | +17,0×10−6 cm3/mol (303 K)[5] | ||||||||||||||||||||||||||||||||||||||||
| Modulus Young | 2,4 GPa | ||||||||||||||||||||||||||||||||||||||||
| Modulus curah | 2,5 GPa | ||||||||||||||||||||||||||||||||||||||||
| Skala Mohs | 0,3 | ||||||||||||||||||||||||||||||||||||||||
| Skala Brinell | 0,216 MPa | ||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 7440-17-7 | ||||||||||||||||||||||||||||||||||||||||
| Sejarah | |||||||||||||||||||||||||||||||||||||||||
| Penemuan | R. Bunsen dan G. Kirchhoff (1861) | ||||||||||||||||||||||||||||||||||||||||
| Isolasi pertama | G. Hevesy | ||||||||||||||||||||||||||||||||||||||||
| Isotop rubidium yang utama | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
Rubidium adalah sebuah unsur kimia dengan lambang Rb dan nomor atom 37. Rubidium adalah sebuah logam abu-abu keputihan yang sangat lunak dalam golongan logam alkali. Logam rubidium memiliki kesamaan dengan logam kalium dan logam sesium dalam penampilan fisik, kelembutan dan konduktivitas.[6] Rubidium tidak dapat disimpan di bawah oksigen atmosfer, karena reaksi eksoterm yang sangat tinggi akan terjadi, kadang-kadang bahkan mengakibatkan logam ini terbakar.[7]
Rubidium adalah logam alkali pertama dalam golongannya yang memiliki massa jenis lebih tinggi dari air, sehingga ia tenggelam, tidak seperti logam di atasnya dalam golongannya. Rubidium memiliki berat atom standar 85,4678. Di Bumi, rubidium alami terdiri dari dua isotop: 72% di antaranya adalah 85Rb yang stabil, dan 28% sisanya adalah 87Rb yang sedikit radioaktif, dengan waktu paruh 48,8 miliar tahun—lebih dari tiga kali lebih lama dari perkiraan usia alam semesta.
Ahli kimia Jerman Robert Bunsen dan Gustav Kirchhoff menemukan rubidium pada tahun 1861 dengan teknik yang baru dikembangkan, yaitu spektroskopi nyala api. Nama unsur ini berasal dari kata Latin rubidus, yang berarti merah tua, dari warna spektrum emisinya. Senyawa rubidium memiliki berbagai aplikasi kimia dan elektronik. Logam rubidium mudah diuapkan dan memiliki rentang penyerapan spektral yang nyaman, menjadikannya target yang sering digunakan untuk manipulasi atom dengan laser. Rubidium bukanlah nutrisi yang diketahui untuk organisme hidup mana pun. Namun, ion rubidium memiliki sifat yang sama dan muatan yang sama seperti ion kalium, dan secara aktif diambil dan diperlakukan oleh sel hewan dengan cara yang sama.
Karakteristik
[sunting | sunting sumber]
Rubidium adalah logam yang sangat lembut, ulet, dan berwarna putih keperakan.[8] Ia merupakan logam alkali stabil yang paling elektropositif kedua dan meleleh pada suhu 393 °C (739 °F). Seperti logam alkali lainnya, logam rubidium bereaksi hebat dengan air. Seperti halnya kalium (yang sedikit kurang reaktif) dan sesium (yang sedikit lebih reaktif), reaksi ini biasanya cukup kuat untuk menyalakan gas hidrogen yang dihasilkannya. Rubidium juga telah dilaporkan menyala secara spontan di udara.[8] Ia membentuk amalgam dengan raksa dan paduan dengan emas, besi, sesium, natrium, dan kalium, tetapi tidak dengan litium (walaupun rubidium dan litium berada dalam golongan yang sama).[9]

Rubidium memiliki energi ionisasi yang sangat rendah, hanya 406 kJ/mol.[10] Rubidium dan kalium menunjukkan warna ungu yang sangat mirip dalam uji nyala api, dan untuk membedakan kedua unsur tersebut memerlukan analisis yang lebih canggih, seperti spektroskopi.[butuh rujukan]
Senyawa
[sunting | sunting sumber]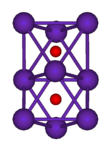
Rubidium klorida (RbCl) mungkin merupakan senyawa rubidium yang paling banyak digunakan: di antara beberapa klorida lainnya, ia digunakan untuk menginduksi sel hidup untuk mengambil DNA; ia juga digunakan sebagai biomarker, karena di alam, ia hanya ditemukan dalam jumlah kecil pada organisme hidup dan bila ada, menggantikan kalium. Senyawa rubidium umum lainnya adalah rubidium hidroksida (RbOH) yang korosif, bahan awal untuk sebagian besar proses kimia berbasis rubidium; rubidium karbonat (Rb2CO3), digunakan dalam beberapa kaca optik, dan rubidium tembaga sulfat, Rb2SO4·CuSO4·6H2O. Rubidium perak iodida (RbAg4I5) memiliki konduktivitas suhu kamar tertinggi dari setiap kristal ionik yang diketahui, sifat yang dimanfaatkan dalam baterai film tipis dan aplikasi lainnya.[11][12]
Rubidium akan membentuk sejumlah oksida bila terkena udara, termasuk rubidium monoksida (Rb2O), Rb6O, dan Rb9O2; rubidium dalam oksigen berlebih akan menghasilkan superoksida RbO2. Rubidium akan membentuk garam dengan halogen, menghasilkan rubidium fluorida, rubidium klorida, rubidium bromida, dan rubidium iodida.[13]
Isotop
[sunting | sunting sumber]Meskipun rubidium merupakan unsur monoisotop, rubidium di kerak bumi terdiri dari dua isotop: 85Rb yang stabil (72,2%) dan 87Rb (27,8%) yang radioaktif.[14] Rubidium alami bersifat radioaktif, dengan aktivitas spesifik sekitar 670 Bq/g, cukup untuk mengekspos film gulung secara signifikan dalam 110 hari.[15][16] Tiga puluh isotop rubidium tambahan telah disintesis dengan waktu paruh kurang dari 3 bulan; sebagian besar dari mereka sangat radioaktif dan memiliki sedikit kegunaan.[17]
Rubidium-87 memiliki waktu paruh 48,8×109 tahun, lebih dari tiga kali usia alam semesta (13,799±0,021)×109 tahun,[18] menjadikannya sebagai nuklida primordial. Ia dengan mudah menggantikan kalium dalam mineral, dan karena itu cukup tersebar luas. Rb telah digunakan secara luas dalam penanggalan batuan; 87Rb meluruh melalui peluruhan beta menjadi 87Sr yang stabil. Selama kristalisasi fraksional, Sr cenderung terkonsentrasi di plagioklas, meninggalkan Rb dalam fase cair. Oleh karena itu, rasio Rb/Sr dalam sisa magma dapat meningkat dari waktu ke waktu, dan diferensiasi yang berkembang menghasilkan batuan dengan rasio Rb/Sr yang meningkat. Rasio tertinggi (10 atau lebih) terjadi pada pegmatit. Jika jumlah awal Sr diketahui atau dapat diekstrapolasi, maka umurnya dapat ditentukan dengan pengukuran konsentrasi Rb dan Sr dan rasio 87Sr/86Sr. Tanggalnya menunjukkan usia sebenarnya dari mineralnya hanya jika batuannya tidak mengalami ubahan (lihat penanggalan rubidium–stronsium).[19][20]
Rubidium-82, salah satu isotop nonalami rubidium, dihasilkan oleh peluruhan penangkapan elektron dari stronsium-82 dengan waktu paruh 25,36 hari. Dengan waktu paruh 76 detik, rubidium-82 meluruh melalui emisi positron menjadi kripton-82 yang stabil.[14]
Keterjadian
[sunting | sunting sumber]Rubidium adalah unsur paling melimpah kedua puluh tiga di kerak Bumi, kira-kira sebanyak seng dan agak lebih umum daripada tembaga.[21] Ia terjadi secara alami dalam mineral leusit, polusit, karnalit, dan zinwaldit, yang mengandung sebanyak 1% rubidium oksida. Lepidolit mengandung antara 0,3% dan 3,5% rubidium, dan merupakan sumber komersial dari unsur ini.[22] Beberapa mineral kalium dan kalium klorida juga mengandung unsur ini dalam jumlah yang signifikan secara komersial.[23]
Air laut mengandung rata-rata 125 µg/L rubidium dibandingkan dengan nilai kalium yang jauh lebih tinggi, yaitu 408 mg/L, dan nilai sesium yang jauh lebih rendah, yaitu 0,3 µg/L.[24] Rubidium adalah unsur paling melimpah ke-18 di air laut.[25]
Karena jari-jari ionnya yang besar, rubidium merupakan salah satu "unsur yang tidak kompatibel."[26] Selama kristalisasi magma, rubidium terkonsentrasi bersama dengan analognya yang lebih berat, sesium, dalam fase cair dan mengkristal terakhir. Oleh karena itu, deposit rubidium dan cesium terbesar adalah badan bijih zona pegmatit yang dibentuk oleh proses pengayaan ini. Karena rubidium menggantikan kalium dalam kristalisasi magma, pengayaan ini jauh kurang efektif dibandingkan dengan sesium. Badan bijih pegmatit zona yang mengandung sejumlah sesium yang dapat ditambang sebagai polusit atau mineral litium lepidolit juga merupakan sumber rubidium sebagai produk sampingan.[21]
Dua sumber penting rubidium adalah endapan polusit yang kaya di Danau Bernic, Manitoba, Kanada, dan rubiklin ((Rb,K)AlSi3O8) yang ditemukan sebagai pengotor dalam polusit di pulau Elba di Italia, dengan kandungan rubidium 17,5%.[27] Kedua endapan tersebut juga merupakan sumber sesium.[butuh rujukan]
Produksi
[sunting | sunting sumber]
Meskipun rubidium lebih melimpah di kerak Bumi daripada sesium, aplikasinya yang terbatas dan kurangnya mineral yang kaya akan rubidium membatasi produksi senyawa rubidium hingga 2 hingga 4 ton per tahun.[21] Beberapa metode tersedia untuk memisahkan kalium, rubidium, dan sesium. Kristalisasi fraksional rubidium dan tawas sesium (Cs,Rb)Al(SO4)2·12H2O akan menghasilkan tawas rubidium murni setelah 30 langkah berikutnya. Dua metode lain dilaporkan, proses klorostanat dan proses ferosianida.[21][28]
Selama beberapa tahun pada 1950-an dan 1960-an, produk sampingan dari produksi kalium yang disebut Alkarb adalah sumber utama rubidium. Alkarb mengandung 21% rubidium, sisanya adalah kalium dan sedikit sesium.[29] Saat ini produsen sesium terbesar, seperti Tambang Tanco di Manitoba, Kanada, memproduksi rubidium sebagai produk sampingan dari polusit.[21]
Sejarah
[sunting | sunting sumber]
Rubidium ditemukan pada tahun 1861 oleh Robert Bunsen dan Gustav Kirchhoff, di Heidelberg, Jerman, dalam mineral lepidolite melalui spektroskopi nyala api. Karena garis merah terang dalam spektrum pancarnya, mereka memilih nama yang berasal dari kata Latin rubidus, yang berarti "merah tua".[30][31]
Rubidium adalah komponen minor dalam lepidolit. Kirchhoff dan Bunsen memproses 150 kg lepidolit yang hanya mengandung 0,24% rubidium monoksida (Rb2O). Baik kalium maupun rubidium membentuk garam yang tidak larut dengan asam kloroplatinat, tetapi garam-garam tersebut menunjukkan sedikit perbedaan kelarutan dalam air panas. Oleh karena itu, rubidium heksakloroplatinat (Rb2PtCl6) yang kurang larut dapat diperoleh dengan kristalisasi fraksional. Setelah reduksi heksakloroplatinat dengan hidrogen, proses tersebut menghasilkan 0,51 gram rubidium klorida (RbCl) untuk studi lebih lanjut. Bunsen dan Kirchhoff memulai isolasi skala besar pertama dari senyawa sesium dan rubidium dengan 44.000 liter (12.000 US gal) air mineral, yang menghasilkan 7,3 gram sesium klorida dan 9,2 gram rubidium klorida.[30][31] Rubidium adalah unsur kedua, tak lama setelah sesium, yang ditemukan dengan spektroskopi, hanya satu tahun setelah penemuan spektroskop oleh Bunsen dan Kirchhoff.[32]
Kedua ilmuwan tersebut menggunakan rubidium klorida untuk memperkirakan berat atom unsur baru ini sebesar 85,36 (nilai yang diterima saat ini adalah 85,47).[30] Mereka mencoba menghasilkan rubidium unsur dengan elektrolisis rubidium klorida cair, tetapi alih-alih logam, mereka memperoleh zat homogen biru, yang "baik di bawah mata telanjang maupun di bawah mikroskop tidak menunjukkan sedikit pun zat logam". Mereka menganggap bahwa itu adalah subklorida (Rb2Cl); namun, produk tersebut kemungkinan merupakan campuran koloid dari logam rubidium dan rubidium klorida.[33] Dalam upaya kedua untuk menghasilkan rubidium metalik, Bunsen mampu mereduksi rubidium dengan memanaskan rubidium tartrat yang hangus. Meskipun rubidium sulingan bersifat piroforik, mereka mampu menentukan densitas dan titik leburnya. Kualitas penelitian pada tahun 1860-an ini dapat dinilai dengan fakta bahwa kepadatan yang mereka tentukan berbeda kurang dari 0,1 g/cm3 dan titik lebur yang mereka tentukan berbeda kurang dari 1 °C dari nilai yang diterima saat ini.[34]
Radioaktivitas kecil dari rubidium ditemukan pada tahun 1908, tetapi itu ditemukan sebelum teori mengenai isotop dipublikasikan pada tahun 1910, dan tingkat aktivitas yang rendah (waktu paruh lebih dari 1010 tahun) membuat interpretasi menjadi rumit. Peluruhan 87Rb menjadi 87Sr yang stabil melalui peluruhan beta yang sekarang telah terbukti masih didiskusikan pada akhir 1940-an.[35][36]
Rubidium memiliki nilai industri yang kecil sebelum tahun 1920-an.[37] Sejak itu, penggunaan rubidium yang paling penting adalah penelitian dan pengembangan, terutama dalam aplikasi kimia dan elektronik. Pada tahun 1995, rubidium-87 digunakan untuk menghasilkan kondensat Bose–Einstein,[38] di mana penemunya, Eric Allin Cornell, Carl Edwin Wieman dan Wolfgang Ketterle, memenangkan Penghargaan Nobel Fisika pada tahun 2001.[39]
Aplikasi
[sunting | sunting sumber]
Senyawa rubidium kadang-kadang digunakan dalam kembang api untuk memberi mereka warna ungu.[40] Rubidium juga telah dipertimbangkan untuk digunakan dalam generator termoelektrik menggunakan prinsip magnetohidrodinamika, di mana ion rubidium panas dilewatkan melalui medan magnet.[41] Mereka menghantarkan listrik dan bertindak seperti armatur sehingga menghasilkan arus listrik. Rubidium, khususnya 87Rb, adalah salah satu spesies atom yang paling umum digunakan untuk pendinginan laser dan kondensasi Bose–Einstein. Fitur yang diinginkan untuk aplikasi ini termasuk ketersediaan sinar laser dioda yang murah pada panjang gelombang yang relevan dan suhu sedang yang diperlukan untuk mendapatkan tekanan uap yang substansial.[42][43] Untuk aplikasi atom dingin yang membutuhkan interaksi merdu, 85Rb lebih disukai karena spektrum Feshbachnya yang kaya.[44]
Rubidium telah digunakan untuk polarisasi 3He, menghasilkan volume gas 3He yang termagnetisasi, dengan spin inti yang sejajar dan bukan acak. Uap rubidium dipompa secara optik oleh laser, dan Rb yang terpolarisasi akan mempolarisasi 3He melalui interaksi hiperfin.[45] Sel 3He yang terpolarisasi spin tersebut berguna untuk pengukuran polarisasi neutron dan untuk memproduksi berkas neutron terpolarisasi untuk tujuan lain.[46]
Unsur resonansi dalam jam atom menggunakan struktur hiperfin dari tingkat energi rubidium, dan rubidium berguna untuk pengaturan waktu dengan presisi tinggi. Ia digunakan sebagai komponen utama dari referensi frekuensi sekunder (osilator rubidium) di pemancar situs sel dan transmisi elektronik lainnya, jaringan, dan peralatan uji. Standar rubidium ini sering digunakan dengan GPS untuk menghasilkan "standar frekuensi primer" yang memiliki akurasi lebih tinggi dan lebih murah daripada standar sesium.[47][48] Standar rubidium seperti itu sering diproduksi secara massal untuk industri telekomunikasi.[49]
Potensi atau penggunaan rubidium lainnya saat ini termasuk fluida kerja dalam turbin uap, sebagai penangkap dalam tabung vakum, dan sebagai komponen fotosel.[50] Rubidium juga digunakan sebagai bahan dalam jenis kaca khusus, dalam produksi superoksida dengan membakar oksigen, dalam studi saluran ion kalium dalam biologi, dan sebagai uap dalam magnetometer atom.[51] Secara khusus, 87Rb digunakan dengan logam alkali lainnya dalam pengembangan magnetometer bebas relaksasi pertukaran spin (spin-exchange relaxation-free, SERF).[51]
Rubidium-82 digunakan untuk tomografi emisi positron. Rubidium sangat mirip dengan kalium, dan jaringan dengan kandungan kalium tinggi juga akan mengakumulasi rubidium radioaktif. Salah satu kegunaan utamanya adalah pencitraan perfusi miokard. Sebagai akibat dari perubahan sawar darah otak pada tumor otak, rubidium mengumpulkan lebih banyak pada tumor otak daripada jaringan otak normal, memungkinkan penggunaan radioisotop rubidium-82 dalam kedokteran nuklir untuk menemukan dan menggambarkan tumor otak.[52] Rubidium-82 memiliki waktu paruh yang sangat singkat, yaitu 76 detik, dan produksi dari peluruhan stronsium-82 harus dilakukan dekat dengan pasien.[53]
Pengaruh rubidium diuji pada depresi manik dan depresi.[54][55] Pasien dialisis yang menderita depresi menunjukkan penipisan rubidium, dan oleh karena itu suplementasi dapat membantu selama depresi.[56] Dalam beberapa tes, rubidium diberikan sebagai rubidium klorida hingga 720 mg per hari selama 60 hari.[57][58]
| Bahaya | |
|---|---|
| Piktogram GHS |  
|
| Keterangan bahaya GHS | {{{value}}} |
| H260, H314 | |
| P223, P231+232, P280, P305+351+338, P370+378, P422[59] | |
Tindakan pencegahan dan efek biologis
[sunting | sunting sumber]Rubidium bereaksi hebat dengan air dan dapat menyebabkan kebakaran. Untuk memastikan keamanan dan kemurniannya, logam ini biasanya disimpan di bawah minyak mineral kering atau disegel dalam ampul kaca dalam atmosfer lengai. Rubidium akan membentuk peroksida pada paparan bahkan pada sejumlah kecil udara yang menyebar ke dalam minyak, dan penyimpanan tunduk pada tindakan pencegahan yang sama seperti penyimpanan kalium metalik.[60]
Rubidium, seperti natrium dan kalium, hampir selalu memiliki bilangan oksidasi +1 ketika dilarutkan dalam air, bahkan dalam konteks biologis. Tubuh manusia cenderung memperlakukan ion Rb+ seolah-olah mereka adalah ion kalium, dan oleh karena itu mengonsentrasikan rubidium dalam cairan intraseluler tubuh (yaitu, di dalam sel).[61] Ion-ion tersebut tidak terlalu beracun; orang dengan berat badan 70 kg mengandung rata-rata 0,36 g rubidium, dan peningkatan nilai ini sebesar 50 hingga 100 kali tidak menunjukkan efek negatif pada orang yang diuji.[62] Waktu paruh biologis rubidium pada manusia adalah 31–46 hari.[54] Meskipun substitusi parsial kalium oleh rubidium dimungkinkan, ketika lebih dari 50% kalium dalam jaringan otot tikus diganti dengan rubidium, tikus tersebut akan mati.[63][64]
Referensi
[sunting | sunting sumber]- ^ (Indonesia) "Rubidium". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ a b Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (edisi ke-92). Boca Raton, FL: CRC Press. hlm. 4.122. ISBN 1439855110.
- ^ Cverna, Fran (2002). "Ch. 2 Thermal Expansion". ASM Ready Reference: Thermal properties of metals (PDF). ASM International. ISBN 978-0-87170-768-0.
- ^ Lide, D. R., ed. (2005). "Magnetic susceptibility of the elements and inorganic compounds". CRC Handbook of Chemistry and Physics (PDF) (edisi ke-86). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. hlm. E110. ISBN 0-8493-0464-4.
- ^ "Electrical conductivity of the Elements". Diakses tanggal 29 Juli 2022.
Rubidium Conductivity
- ^ "Reactions of Group 1 Elements with Oxygen". 3 Oktober 2013. Diakses tanggal 29 Juli 2022.
Rubidium & Cesium/ Reactions with Oxygen
- ^ a b Ohly, Julius (1910). "Rubidium". Analysis, detection and commercial value of the rare metals. Mining Science Pub. Co.
- ^ Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). "Vergleichende Übersicht über die Gruppe der Alkalimetalle". Lehrbuch der Anorganischen Chemie (dalam bahasa Jerman) (edisi ke-91–100). Walter de Gruyter. hlm. 953–955. ISBN 978-3-11-007511-3.
- ^ Moore, John W; Stanitski, Conrad L; Jurs, Peter C (2009). Principles of Chemistry: The Molecular Science. hlm. 259. ISBN 978-0-495-39079-4.
- ^ Smart, Lesley; Moore, Elaine (1995). "RbAg4I5". Solid state chemistry: an introduction
 . CRC Press. hlm. 176–177. ISBN 978-0-7487-4068-0.
. CRC Press. hlm. 176–177. ISBN 978-0-7487-4068-0.
- ^ Bradley, J. N.; Greene, P. D. (1967). "Relationship of structure and ionic mobility in solid MAg4I5". Trans. Faraday Soc. 63: 2516. doi:10.1039/TF9676302516.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- ^ a b Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties", Nuclear Physics A, 729: 3–128, Bibcode:2003NuPhA.729....3A, doi:10.1016/j.nuclphysa.2003.11.001
- ^ Strong, W. W. (1909). "On the Possible Radioactivity of Erbium, Potassium and Rubidium". Physical Review. Series I. 29 (2): 170–173. Bibcode:1909PhRvI..29..170S. doi:10.1103/PhysRevSeriesI.29.170.
- ^ Lide, David R; Frederikse, H. P. R (June 1995). CRC handbook of chemistry and physics: a ready-reference book of chemical and physical data. hlm. 4–25. ISBN 978-0-8493-0476-7.
- ^ "Universal Nuclide Chart". nucleonica. Diarsipkan dari versi asli
 tanggal 19 Februari 2017. Diakses tanggal 29 Juli 2022.
tanggal 19 Februari 2017. Diakses tanggal 29 Juli 2022.
- ^ Planck Collaboration (2016). "Planck 2015 results. XIII. Cosmological parameters (Lihat Tabel 4 di halaman 31)". Astronomy & Astrophysics. 594: A13. arXiv:1502.01589
 . Bibcode:2016A&A...594A..13P. doi:10.1051/0004-6361/201525830.
. Bibcode:2016A&A...594A..13P. doi:10.1051/0004-6361/201525830.
- ^ Attendorn, H.-G.; Bowen, Robert (1988). "Rubidium-Strontium Dating". Isotopes in the Earth Sciences. Springer. hlm. 162–165. ISBN 978-0-412-53710-3.
- ^ Walther, John Victor (2009) [1988]. "Rubidium-Strontium Systematics". Essentials of geochemistry. Jones & Bartlett Learning. hlm. 383–385. ISBN 978-0-7637-5922-3.
- ^ a b c d e Butterman, William C.; Brooks, William E.; Reese, Jr., Robert G. (2003). "Mineral Commodity Profile: Rubidium" (PDF). United States Geological Survey. Diakses tanggal 30 Juli 2022.
- ^ Wise, M. A. (1995). "Trace element chemistry of lithium-rich micas from rare-element granitic pegmatites". Mineralogy and Petrology. 55 (13): 203–215. Bibcode:1995MinPe..55..203W. doi:10.1007/BF01162588.
- ^ Norton, J. J. (1973). "Lithium, cesium, and rubidium—The rare alkali metals". Dalam Brobst, D. A.; Pratt, W. P. United States mineral resources. Paper 820. U.S. Geological Survey Professional. hlm. 365–378. Diarsipkan dari versi asli tanggal 21 Juli 2010. Diakses tanggal 30 Juli 2022.
- ^ Bolter, E.; Turekian, K.; Schutz, D. (1964). "The distribution of rubidium, cesium and barium in the oceans". Geochimica et Cosmochimica Acta. 28 (9): 1459. Bibcode:1964GeCoA..28.1459B. doi:10.1016/0016-7037(64)90161-9.
- ^ William A. Hart |title=The Chemistry of Lithium, Sodium, Potassium, Rubidium, Caesium, and Francium |page=371
- ^ McSween Jr., Harry Y; Huss, Gary R (2010). Cosmochemistry. hlm. 224. ISBN 978-0-521-87862-3.
- ^ Teertstra, David K.; Cerny, Petr; Hawthorne, Frank C.; Pier, Julie; Wang, Lu-Min; Ewing, Rodney C. (1998). "Rubicline, a new feldspar from San Piero in Campo, Elba, Italy". American Mineralogist. 83 (11–12 Part 1): 1335–1339. Bibcode:1998AmMin..83.1335T. doi:10.2138/am-1998-11-1223.
- ^ bulletin 585. United States. Bureau of Mines. 1995.
- ^ "Cesium and Rubidium Hit Market". Chemical & Engineering News. 37 (22): 50–56. 1959. doi:10.1021/cen-v037n022.p050.
- ^ a b c Kirchhoff, G.; Bunsen, R. (1861). "Chemische Analyse durch Spectralbeobachtungen" (PDF). Annalen der Physik und Chemie. 189 (7): 337–381. Bibcode:1861AnP...189..337K. doi:10.1002/andp.18611890702. hdl:2027/hvd.32044080591324.
- ^ a b Weeks, Mary Elvira (1932). "The discovery of the elements. XIII. Some spectroscopic discoveries". Journal of Chemical Education. 9 (8): 1413–1434. Bibcode:1932JChEd...9.1413W. doi:10.1021/ed009p1413.
- ^ Ritter, Stephen K. (2003). "C&EN: It's Elemental: The Periodic Table – Cesium". American Chemical Society. Diakses tanggal 30 Juli 2022.
- ^ Zsigmondy, Richard (2007). Colloids and the Ultra Microscope. Read books. hlm. 69. ISBN 978-1-4067-5938-9. Diakses tanggal 30 Juli 2022.
- ^ Bunsen, R. (1863). "Ueber die Darstellung und die Eigenschaften des Rubidiums". Annalen der Chemie und Pharmacie. 125 (3): 367–368. doi:10.1002/jlac.18631250314.
- ^ Lewis, G. M. (1952). "The natural radioactivity of rubidium". Philosophical Magazine. Series 7. 43 (345): 1070–1074. doi:10.1080/14786441008520248.
- ^ Campbell, N. R.; Wood, A. (1908). "The Radioactivity of Rubidium". Proceedings of the Cambridge Philosophical Society. 14: 15.
- ^ Butterman, W. C.; Reese, Jr., R. G. "Mineral Commodity Profiles Rubidium" (PDF). United States Geological Survey. Diakses tanggal 30 Juli 2022.
- ^ "Press Release: The 2001 Nobel Prize in Physics". Diakses tanggal 30 Juli 2022.
- ^ Levi, Barbara Goss (2001). "Cornell, Ketterle, and Wieman Share Nobel Prize for Bose-Einstein Condensates". Physics Today. 54 (12): 14–16. Bibcode:2001PhT....54l..14L. doi:10.1063/1.1445529
 .
.
- ^ Koch, E.-C. (2002). "Special Materials in Pyrotechnics, Part II: Application of Caesium and Rubidium Compounds in Pyrotechnics". Journal Pyrotechnics. 15: 9–24. Diarsipkan dari versi asli tanggal 13 Juli 2011. Diakses tanggal 30 Juli 2022.
- ^ Boikess, Robert S; Edelson, Edward (1981). Chemical principles. hlm. 193. ISBN 978-0-06-040808-4.
- ^ Eric Cornell; et al. (1996). "Bose-Einstein condensation (all 20 articles)". Journal of Research of the National Institute of Standards and Technology. 101 (4): 419–618. doi:10.6028/jres.101.045. PMC 4907621
 . PMID 27805098. Diarsipkan dari versi asli tanggal 14 Oktober 2011. Diakses tanggal 30 Juli 2022.
. PMID 27805098. Diarsipkan dari versi asli tanggal 14 Oktober 2011. Diakses tanggal 30 Juli 2022.
- ^ Martin, J. L.; McKenzie, C. R.; Thomas, N. R.; Sharpe, J. C.; Warrington, D. M.; Manson, P. J.; Sandle, W. J.; Wilson, A. C. (1999). "Output coupling of a Bose-Einstein condensate formed in a TOP trap". Journal of Physics B: Atomic, Molecular and Optical Physics. 32 (12): 3065. arXiv:cond-mat/9904007
 . Bibcode:1999JPhB...32.3065M. doi:10.1088/0953-4075/32/12/322.
. Bibcode:1999JPhB...32.3065M. doi:10.1088/0953-4075/32/12/322.
- ^ Chin, Cheng; Grimm, Rudolf; Julienne, Paul; Tiesinga, Eite (2010-04-29). "Feshbach resonances in ultracold gases". Reviews of Modern Physics. 82 (2): 1225–1286. arXiv:0812.1496
 . Bibcode:2010RvMP...82.1225C. doi:10.1103/RevModPhys.82.1225.
. Bibcode:2010RvMP...82.1225C. doi:10.1103/RevModPhys.82.1225.
- ^ Gentile, T. R.; Chen, W. C.; Jones, G. L.; Babcock, E.; Walker, T. G. (2005). "Polarized 3He spin filters for slow neutron physics" (PDF). Journal of Research of the National Institute of Standards and Technology. 110 (3): 299–304. doi:10.6028/jres.110.043. PMC 4849589
 . PMID 27308140. Diarsipkan dari versi asli (PDF) tanggal 21 Desember 2016. Diakses tanggal 30 Juli 2022.
. PMID 27308140. Diarsipkan dari versi asli (PDF) tanggal 21 Desember 2016. Diakses tanggal 30 Juli 2022.
- ^ "Neutron spin filters based on polarized helium-3". NIST Center for Neutron Research 2002 Annual Report. Diakses tanggal 30 Juli 2022.
- ^ Eidson, John C (2006-04-11). "GPS". Measurement, control, and communication using IEEE 1588. hlm. 32. ISBN 978-1-84628-250-8.
- ^ King, Tim; Newson, Dave (1999-07-31). "Rubidium and crystal oscillators". Data network engineering. hlm. 300. ISBN 978-0-7923-8594-3.
- ^ Marton, L. (1977-01-01). "Rubidium Vapor Cell". Advances in electronics and electron physics. ISBN 978-0-12-014644-4.
- ^ Mittal (2009). Introduction To Nuclear And Particle Physics. hlm. 274. ISBN 978-81-203-3610-0.
- ^ a b Li, Zhimin; Wakai, Ronald T.; Walker, Thad G. (2006). "Parametric modulation of an atomic magnetometer". Applied Physics Letters. 89 (13): 23575531–23575533. Bibcode:2006ApPhL..89m4105L. doi:10.1063/1.2357553. PMC 3431608
 . PMID 22942436.
. PMID 22942436.
- ^ Yen, C. K.; Yano, Y.; Budinger, T. F.; Friedland, R. P.; Derenzo, S. E.; Huesman, R. H.; O'Brien, H. A. (1982). "Brain tumor evaluation using Rb-82 and positron emission tomography". Journal of Nuclear Medicine. 23 (6): 532–7. PMID 6281406.
- ^ Jadvar, H.; Anthony Parker, J. (2005). "Rubidium-82". Clinical PET and PET/CT. hlm. 59. ISBN 978-1-85233-838-1.
- ^ a b Paschalis, C.; Jenner, F. A.; Lee, C. R. (1978). "Effects of rubidium chloride on the course of manic-depressive illness". J R Soc Med. 71 (9): 343–352. doi:10.1177/014107687807100507. PMC 1436619
 . PMID 349155.
. PMID 349155.
- ^ Malekahmadi, P.; Williams, John A. (1984). "Rubidium in psychiatry: Research implications". Pharmacology Biochemistry and Behavior. 21: 49–50. doi:10.1016/0091-3057(84)90162-X. PMID 6522433.
- ^ Canavese, Caterina; Decostanzi, Ester; Branciforte, Lino; Caropreso, Antonio; Nonnato, Antonello; Sabbioni, Enrico (2001). "Depression in dialysis patients: Rubidium supplementation before other drugs and encouragement?". Kidney International. 60 (3): 1201–2. doi:10.1046/j.1523-1755.2001.0600031201.x
 . PMID 11532118.
. PMID 11532118.
- ^ Lake, James A. (2006). Textbook of Integrative Mental Health Care. New York: Thieme Medical Publishers. hlm. 164–165. ISBN 978-1-58890-299-3.
- ^ Torta, R.; Ala, G.; Borio, R.; Cicolin, A.; Costamagna, S.; Fiori, L.; Ravizza, L. (1993). "Rubidium chloride in the treatment of major depression". Minerva Psichiatrica. 34 (2): 101–110. PMID 8412574.
- ^ "Rubidium 276332". Sigma-Aldrich.
- ^ Martel, Bernard; Cassidy, Keith (1 Juli 2004). "Rubidium". Chemical risk analysis: a practical handbook. hlm. 215. ISBN 978-1-903996-65-2.
- ^ Relman, A. S. (1956). "The Physiological Behavior of Rubidium and Cesium in Relation to That of Potassium". The Yale Journal of Biology and Medicine. 29 (3): 248–62. PMC 2603856
 . PMID 13409924.
. PMID 13409924.
- ^ Fieve, Ronald R.; Meltzer, Herbert L.; Taylor, Reginald M. (1971). "Rubidium chloride ingestion by volunteer subjects: Initial experience". Psychopharmacologia. 20 (4): 307–14. doi:10.1007/BF00403562. PMID 5561654.
- ^ Meltzer, H. L. (1991). "A pharmacokinetic analysis of long-term administration of rubidium chloride". Journal of Clinical Pharmacology. 31 (2): 179–84. doi:10.1002/j.1552-4604.1991.tb03704.x. PMID 2010564. Diarsipkan dari versi asli tanggal 9 Juli 2012.
- ^ Follis, Richard H., Jr. (1943). "Histological effects in rats resulting from adding rubidium or cesium to a diet deficient in potassium". AJP: Legacy Content. 138 (2): 246–250. doi:10.1152/ajplegacy.1943.138.2.246.
Bacaan lebih lanjut
[sunting | sunting sumber]- Meites, Louis (1963). Handbook of Analytical Chemistry (New York: McGraw-Hill Book Company, 1963)
- Steck, Daniel A. "Rubidium-87 D Line Data" (PDF). Laboratorium Nasional Los Alamos (laporan teknikal LA-UR-03-8638). Diarsipkan dari versi asli (PDF) tanggal 2 November 2013. Diakses tanggal 30 Juli 2022.
Pranala luar
[sunting | sunting sumber] "Rubidium". Encyclopædia Britannica. 23 (edisi ke-11). 1911. hlm. 809.
"Rubidium". Encyclopædia Britannica. 23 (edisi ke-11). 1911. hlm. 809.- Rubidium di The Periodic Table of Videos (Universitas Nottingham)
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


