Pirimidina: Perbedaan antara revisi
JohnThorne (bicara | kontrib) Tidak ada ringkasan suntingan |
−Kategori:Heterolingkar dua nitrogen; −Kategori:Diazina; ±Kategori:Cincin enam atom→Kategori:Cincin aromatik sederhana menggunakan HotCat |
||
| (20 revisi perantara oleh 8 pengguna tidak ditampilkan) | |||
Baris 51:
}}
'''Pirimidina''' ({{lang-en|Pyrimidine}}) adalah suatu [[senyawa organik]] [[heterosiklik]] [[aromatik]] yang mirip dengan [[piridina]].<ref name="isbn0-582-27843-0">{{cite book
== Keberadaan dan sejarah ==
[[
Sistem cincin pirimidina banyak dijumpai dalam alam<ref name=Lagoja1>{{Cite journal
| author = Lagoja, Irene M.
Baris 67:
| doi = 10.1002/cbdv.200490173
| pmid = 17191918
| access-date = 2014-12-13
| archive-date = 2017-02-15
| archive-url = https://web.archive.org/web/20170215012342/http://homepage.univie.ac.at/mario.barbatti/papers/pyrazine_pyrimidine/pyrimidine.pdf
| dead-url = yes
}}</ref>
sebagai senyawa berfusi substitusi dan cincin serta derivatifnya, termasuk [[#Nukleotida|nukleotida]], [[tiamina]] (vitamin B1) dan [[alloxan]]. Juga didapati dalam banyak senyawa sintetik seperti [[barbiturat]] dan obat [[HIV]], [[zidovudine]]. Meskipun derivatif pirimidina seperti [[asam urat]] dan alloxan telah dikenal sejak awal abad ke-19, sintesis pirimidina dalam laboratorium baru dilakukan pada tahun 1879,<ref name=Lagoja1/> ketika Grimaux melaporkan pembuatan [[asam barbiturat]] dari [[urea]] Ivy dan [[asam malonat]] dengan katalis [[fosfor oxiklorida]].<ref name=Grimaux1879>{{Cite journal
| author = Grimaux, E.
| year = 1879
Baris 80 ⟶ 82:
| url = http://visualiseur.bnf.fr/ark:/12148/bpt6k30457/f85.image
}}</ref>
Studi sistematik pirimidina dimulai<ref name="ElderfieldVol6">{{cite book
| author = [[Adolf Pinner|Pinner, A.]]
| year = 1884
Baris 123 ⟶ 125:
melalui konversi [[asam barbiturat]] menjadi 2,4,6-trikloropirimidina diikuti oleh reduksi menggunakan debu [[seng]] dalam air panas.
== Nomenklatur ==
Nomenklatur pirimidina tergolong sederhana. Namun, sebagaimana heterosiklik lainnya, gugus hidroksil tautomerik menghasilkan komplikasi karena mereka adanya terutama dalam bentuk amida siklik. Misalnya, 2-hidroksipirimidina lebih tepat dinamai [struktur] 2-pirimidon. Tersedia daftar sebagian nama-nama trivial dari berbagai pirimidina.<ref name="BrownPyrimidines1994p5">{{cite book
<!--▼
Physical properties are shown in the data box. A more extensive discussion, including spectra, can be found in Brown ''et al.''<ref name="BrownPyrimidines1994p242">{{cite book |author=Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. |title=The Pyrimidines |publisher=John Wiley & Sons |location=New York |year=1994 |pages=242–244 |isbn=0-471-50656-7|url= |accessdate=}}</ref>▼
==
▲
Per the classification by Albert<ref name="Albert1968p56">{{cite book |author=Albert, Adrien |title=Heterocyclic Chemistry, an Introduction |publisher=Athlone Press |location=London |year=1968 |pages=56–62 |isbn= |url= |accessdate=}}</ref> six-membered heterocyclics can be described as π-deficient. Substitution by electronegative groups or additional nitrogen atoms in the ring significantly increase the π-deficiency. These effects also decrease the basicity.<ref name="Albert1968p437">{{cite book |author=Albert, Adrien |title=Heterocyclic Chemistry, an Introduction |publisher=Athlone Press |location=London |year=1968 |pages=437–439 |isbn= |url= |accessdate=}}</ref> ▼
== Sifat kimia ==
Like pyridines, in pyrimidines the π-electron density is decreased to an even greater extent. Therefore [[electrophilic aromatic substitution]] is more difficult while [[nucleophilic aromatic substitution]] is facilitated. An example of the last reaction type is the displacement of the [[amino]] group in 2-aminopyrimidine by chlorine<ref>[[Organic Syntheses]], Coll. Vol. 4, p.182 (1963); Vol. 35, p.34 (1955) [http://www.orgsynth.org/orgsyn/pdfs/CV4P0182.pdf Link]</ref> and its reverse.<ref>[[Organic Syntheses]], Coll. Vol. 4, p.336 (1963); Vol. 35, p.58 (1955) [http://www.orgsynth.org/orgsyn/pdfs/CV4P0336.pdf Link]</ref> ▼
▲
▲
Ketersediaan pasangan elektron tunggal ([[kadar basa]]) menurun dibandingkan [[piridina]]. Dibandingkan piridina, [[N-alkilasi]] dan [[N-oksidasi]] lebih sulita. Nilai [[pKa]] untuk pirimidina terprotonasi adalah 1,23 dibandingkan 5,30 untuk piridina. Protonasi dan tambahan elektrofilik lain akan terjadi pada hanya satu [[nitrogen]] karena deaktivasi lebih lanjut oleh nitrogen kedua.<ref name="JouleMills5thp250"/> Posisi 2-, 4-, dan 6- pada cincin pirimidina merupakan analog kekurangan elektron dari senyawa pyridina dan nitro- serta dinitrobenzena. Posisi 5 lebih rendah tingkat kekurangan elektronnya dan substituen di sana sangat stabil. Namun, substitusi eletrofilik relatif lancar pada posisi 5, termasuk [[nitrasi]] dan halogenasi.<ref name="BrownPyrimidines1994p4">{{cite book|author=Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D.|title=The Pyrimidines|publisher=John Wiley & Sons|location=New York|year=1994|pages=[https://archive.org/details/pyrimidines0000unse/page/4 4]–8|isbn=0-471-50656-7|url=https://archive.org/details/pyrimidines0000unse|accessdate=}}</ref>
Reduksi dalam [[stabilisasi resonansi]] pirimidina dapat lebih menghasilkan reaksi adisi dan pemutusan cincin daripada substitusi. Salah satu manifestasinya dapat diamati pada "[[Dimroth rearrangement]]".
Pyrimidine is also found in meteorites, but scientists still do not know its origin. Pyrimidine also photolytically decomposes into [[uracil]] under UV light.<ref name="pmid19778279">{{cite journal |author=Nuevo M, Milam SN, Sandford SA, Elsila JE, Dworkin JP |title=Formation of uracil from the ultraviolet photo-irradiation of pyrimidine in pure H<sub>2</sub>O ices |journal=Astrobiology |volume=9 |issue=7 |pages=683–695 |year=2009 |pmid=19778279 |doi=10.1089/ast.2008.0324|bibcode = 2009AsBio...9..683N }}</ref>▼
▲
As is often the case with parent heterocyclic ring systems, the synthesis of pyrimidine is not that common and is usually performed by removing functional groups from derivatives. Primary syntheses in quantity involving [[formamide]] have been reported.<ref name="BrownPyrimidines1994p241">{{cite book |author=Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. |title=The Pyrimidines |publisher=John Wiley & Sons |location=New York |year=1994 |pages=241–2 |isbn=0-471-50656-7|url= |accessdate=}}</ref>▼
== Sintesis ==
As a class, pyrimidines are typically synthesized by the “Principal Synthesis” involving cyclization of beta-dicarbonyl compounds with N-C-N compounds. Reaction of the former with amidines to give 2-substituted pyrimidines, with urea to give 2-pyrimidiones, and guanidines to give 2-aminopyrimidines are typical.<ref name="BrownPyrimidines1994p149">{{cite book |author=Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. |title=The Pyrimidines |publisher=John Wiley & Sons |location=New York |year=1994 |pages=149–239 |isbn=0-471-50656-7|url= |accessdate=}}</ref>▼
▲
Pyrimidines can be prepared via the [[Biginelli reaction]]. Many other methods rely on [[condensation]] of [[carbonyl]]s with diamines for instance the synthesis of 2-Thio-6-methyluracil from [[thiourea]] and [[ethyl acetoacetate]] <ref>[[Organic Syntheses]], Coll. Vol. 4, p.638 (1963); Vol. 35, p.80 (1955) [http://www.orgsynth.org/orgsyn/pdfs/CV4P0638.pdf Link]</ref> or the synthesis of 4-methylpyrimidine with 4,4-dimethoxy-2-butanone and [[formamide]].<ref>[[Organic Syntheses]], Coll. Vol. 5, p.794 (1973); Vol. 43, p.77 (1963) [http://www.orgsynth.org/orgsyn/pdfs/CV5P0794.pdf Link]</ref>▼
▲
▲<!--
▲
<!--
A novel method is by reaction of certain [[amide]]s with [[carbonitrile]]s under electrophilic activation of the amide with 2-chloro-pyridine and [[trifluoromethanesulfonic anhydride]]:<ref>''Single-Step Synthesis of Pyrimidine Derivatives'' Mohammad Movassaghi and Matthew D. Hill [[J. Am. Chem. Soc.]]; '''2006'''; 128(44) pp 14254–14255; (Communication) {{DOI|10.1021/ja066405m}}</ref>
-->
:[[
== Reaksi ==
▲:[[Image:PyrimidineSynthAmideCarbonitrile.png|400px|Pyrimidine Synthesis Movassaghi 2006]]
<!--
Substitusi-C eletrofilik pirimidina terjadi pada posisi 5, yang paling rendah tingkat kekurangan elektronnya. Nitration, [[nitrosation]], [[azo coupling]], halogenation, [[sulfonation]], formylation, hydroxymethylation, and aminomethylation have been observed with substituted pyrimidines.<ref name="BrownPyrimidines1994p9">{{cite book |author=Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. |title=The Pyrimidines |publisher=John Wiley & Sons |location=New York |year=1994 |pages=[https://archive.org/details/pyrimidines0000unse/page/9 9]–13 |isbn=0-471-50656-7|url=https://archive.org/details/pyrimidines0000unse|accessdate=}}</ref>
Nucleophilic C-substitution should be facilitated at the 2-, 4-, and 6-positions but there are only a few examples. Amination and hydroxylation has been observed for substituted pyrimidines. Reactions with Grignard or alkyllithium reagents yield 4-alkyl- or 4-aryl pyrimidine after aromatization.<ref name="BrownPyrimidines1994p14">{{cite book |author=Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. |title=The Pyrimidines |publisher=John Wiley & Sons |location=New York |year=1994 |pages=
▲Because of the decreased basicity compared to pyridine, electrophilic substitution of pyrimidine is less facile. [[Protonation]] or [[alkylation]] typically takes place at only one of the ring nitrogen atoms. Mono N-oxidation occurs by reaction with peracids.<ref name="JouleMills5thp253">{{cite book | title=Heterocyclic Chemistry |edition=5th |editor1-last=Joule |editor1-first=John A. |editor2-last=Mills |editor2-first=Keith |publisher=Wiley |location=Oxford |year=2010 |pages=253–4 |quote= |isbn=978-1-405-13300-5 |oclc= |doi= |url= |accessdate=}}</ref>
-->
== Nukleotida ==
▲Nucleophilic C-substitution should be facilitated at the 2-, 4-, and 6-positions but there are only a few examples. Amination and hydroxylation has been observed for substituted pyrimidines. Reactions with Grignard or alkyllithium reagents yield 4-alkyl- or 4-aryl pyrimidine after aromatization.<ref name="BrownPyrimidines1994p14">{{cite book |author=Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. |title=The Pyrimidines |publisher=John Wiley & Sons |location=New York |year=1994 |pages=14–15 |isbn=0-471-50656-7|url= |accessdate=}}</ref>
[[
[[urasil]] (U), merupakan derivatif pirimidina:
▲[[File:Blausen 0324 DNA Pyrimidines.png|thumb|250px|The pyrimidine nitrogen bases found in DNA and RNA.]]
▲Three [[nucleobase]]s found in [[nucleic acid]]s, [[cytosine]] (C), [[thymine]] (T), and
{|
|-
| [[
|-
| <center>Sitosina/Cytosine ('''C''')</center> || <center>
|}
Dalam [[RNA]], komplemen [[adenina]] (A) adalah [[urasil]] (U) bukannya [[timina]] (T), sehingga pasangan yang dibentuk adalah [[adenina]]:[[urasil]] (A:U) dan [[guanina]]:[[sitosina]] (G:C).
<!--
Very rarely, thymine can appear in RNA, or uracil in DNA. Other than the three major pyrimidine bases presented, some minor pyrimidine bases can also occur in [[nucleic acids]]. These minor pyrimidines are usually [[Methylation|methylated]] versions of major ones and are postulated to have regulatory functions.<ref>Nelson David L. and Michael M. Cox. ''Principles of Biochemstry'', ed. 5. W.H. Freeman and Company (2008) p. 272–274.</ref>
Baris 191 ⟶ 193:
{{Reflist|2}}
{{Nukleobasa, nukleosida, dan nukleotida}}
[[Kategori:Pirimidina| ]]
[[Kategori:Basa aromatik]]
[[Kategori:Cincin aromatik sederhana]]
| |||
Revisi terkini sejak 5 Desember 2022 14.37
| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Pyrimidine
| |||
| Nama lain
1,3-Diazine, m-Diazine
| |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
| KEGG | |||
| MeSH | pyrimidine | ||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C4H4N2 | |||
| Massa molar | 80.088 g mol−1 | ||
| Densitas | 1.016 g cm−3 | ||
| Titik lebur | 20 °C (68 °F; 293 K) | ||
| Titik didih | 123 °C (253 °F; 396 K) | ||
| Keasaman (pKa) | 1.10[1] (protonated pyrimidine) | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
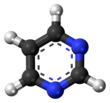
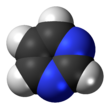
Pirimidina (bahasa Inggris: Pyrimidine) adalah suatu senyawa organik heterosiklik aromatik yang mirip dengan piridina.[2] Satu dari tiga diazina (senyawa heterosiklik enam karbon dengan dua nitrogen pada cincin), mempunyai nitrogen pada posisi 1 dan 3 dalam cincin.[3] Kedua diazina lain adalah pirazina (nitrogen pada posisi 1 dan 4) dan piridazina ( pada posisi 1 dan 2). Dalam asam nukleat, ketiga tipe basa nukleotida merupakan derivat pirimidin yaitu: sitosina (= cytosine) (C), timina (T), dan urasil (U).
Keberadaan dan sejarah
[sunting | sunting sumber]
Sistem cincin pirimidina banyak dijumpai dalam alam[4] sebagai senyawa berfusi substitusi dan cincin serta derivatifnya, termasuk nukleotida, tiamina (vitamin B1) dan alloxan. Juga didapati dalam banyak senyawa sintetik seperti barbiturat dan obat HIV, zidovudine. Meskipun derivatif pirimidina seperti asam urat dan alloxan telah dikenal sejak awal abad ke-19, sintesis pirimidina dalam laboratorium baru dilakukan pada tahun 1879,[4] ketika Grimaux melaporkan pembuatan asam barbiturat dari urea Ivy dan asam malonat dengan katalis fosfor oxiklorida.[5] Studi sistematik pirimidina dimulai[6] pada tahun 1884 oleh Pinner,[7] yang melakukan sintesis derivatif melalui kondensasi etil asetoasetat dengan amidina. Pinner pertama kali mengusulkan nama “pyrimidin” pada tahun 1885.[8] Senyawa induk pertama kali dibuat oleh Gabriel & Colman pada tahun 1900,[9] [10] melalui konversi asam barbiturat menjadi 2,4,6-trikloropirimidina diikuti oleh reduksi menggunakan debu seng dalam air panas.
Nomenklatur
[sunting | sunting sumber]Nomenklatur pirimidina tergolong sederhana. Namun, sebagaimana heterosiklik lainnya, gugus hidroksil tautomerik menghasilkan komplikasi karena mereka adanya terutama dalam bentuk amida siklik. Misalnya, 2-hidroksipirimidina lebih tepat dinamai [struktur] 2-pirimidon. Tersedia daftar sebagian nama-nama trivial dari berbagai pirimidina.[11]
Sifat fisika
[sunting | sunting sumber]Sifat-sifat fisika dapat dilihat pada kotak info. Diskusi lebih mendalam, termasuk spektrum, dapat dilihat dalam Brown et al.[12]
Sifat kimia
[sunting | sunting sumber]Menurut klasifikasi Albert[13] heterosiklik enam karbon dapat dikatakan "π-deficient" ("kekurangan π"). Substitusi oleh gugus elektronegatif atau atom nitrogen tambahan dalam cincin secara signifikan meningkatkan "kekurangan π" itu. Efek ini juga menurunkan kadar basa.[14]
Sebagaimana piridina, dalam pirimidina densitas elektron π menurun sampai taraf lebih besar. Karenanya, substitusi aromatik elektrofilik lebih sulit sementara substitusi aromatik nukleofilik terbantu. Contoh jenis reaksi terakhir adalah penghilangan gugus amino dalam 2-aminopirimidina oleh klor.[15] dan reaksi sebaliknya.[16]
Ketersediaan pasangan elektron tunggal (kadar basa) menurun dibandingkan piridina. Dibandingkan piridina, N-alkilasi dan N-oksidasi lebih sulita. Nilai pKa untuk pirimidina terprotonasi adalah 1,23 dibandingkan 5,30 untuk piridina. Protonasi dan tambahan elektrofilik lain akan terjadi pada hanya satu nitrogen karena deaktivasi lebih lanjut oleh nitrogen kedua.[3] Posisi 2-, 4-, dan 6- pada cincin pirimidina merupakan analog kekurangan elektron dari senyawa pyridina dan nitro- serta dinitrobenzena. Posisi 5 lebih rendah tingkat kekurangan elektronnya dan substituen di sana sangat stabil. Namun, substitusi eletrofilik relatif lancar pada posisi 5, termasuk nitrasi dan halogenasi.[17]
Reduksi dalam stabilisasi resonansi pirimidina dapat lebih menghasilkan reaksi adisi dan pemutusan cincin daripada substitusi. Salah satu manifestasinya dapat diamati pada "Dimroth rearrangement".
Pirimidina juga ditemukan pada meteorit, tetapi para ilmuwan masih tidak tahu asal usulnya. Pirimidina juga secara fotolitik mengalami dekomposisi menjadi urasil di bawah cahaya UV.[18]
Sintesis
[sunting | sunting sumber]Sebagaimana sering kali dijumpai pada sistem heterosiklik induk, sintesis pirimidina tidak begitu lazim dan biasanya dilakukan dengan menghilangan gugus fungsi dari derivatif. Sintesis primer dalam jumlah besar melibatkan formamida telah dilaporkan.[19]
Sebagai suatu kelas, pirimidina biasanya disintesis melalui “Principal Synthesis” melibatkan siklisasi senyawa beta-dikarbonil dengan senyawa N-C-N. Reaksi sebelumnya dengan amidina menghasilkan substitusi pirimidina pada posisi 2, biasanya dengan urea menghasilkan 2-pirimidion, dan dengan guanidina menghasilkan 2-aminopirimidina.[20]
Reaksi
[sunting | sunting sumber]Karena menurunnya kadar basa dibandingkan piridina, substitusi elektrofilik pirimidina kurang lancar. Protonasi atau alkilasi biasanya berlangsung pada hanya satu atom nitrogen dalam cincin. Oksidasi-N mono terjadi melalui reaksi dengan perasida.[21]
Nukleotida
[sunting | sunting sumber]
Tiga nucleobase yang ditemukan dalam asam nukleat, yaitu sitosina/cytosine (C), timina (T), dan urasil (U), merupakan derivatif pirimidina:
 |
 |
 |
Dalam DNA dan RNA, basa-basa ini membentuk ikatan hidrogen dengan purina komplementer. Jadi, dalam DNA, senyawa purina adenina (A) dan guanina (G) masing-masing berpasangan dengan senyawa pirimidina timina (T) dan sitosina (C), membentuk pasangan-pasangan A:T dan G:C.
Dalam RNA, komplemen adenina (A) adalah urasil (U) bukannya timina (T), sehingga pasangan yang dibentuk adalah adenina:urasil (A:U) dan guanina:sitosina (G:C).
Lihat pula
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ Brown, H.C., et al., in Baude, E.A. and Nachod, F.C., Determination of Organic Structures by Physical Methods, Academic Press, New York, 1955.
- ^ Gilchrist, Thomas Lonsdale; Gilchrist, T. L. (1997). Heterocyclic chemistry. New York: Longman. ISBN 0-582-27843-0.
- ^ a b Joule, John A.; Mills, Keith, ed. (2010). Heterocyclic Chemistry (edisi ke-5th). Oxford: Wiley. hlm. 250. ISBN 978-1-405-13300-5.
- ^ a b Lagoja, Irene M. (2007). "Pyrimidine as Constituent of Natural Biologically Active Compounds" (PDF). Chemistry and Biodiversity. 2 (1): 1–50. doi:10.1002/cbdv.200490173. PMID 17191918. Diarsipkan dari versi asli (PDF) tanggal 2017-02-15. Diakses tanggal 2014-12-13.
- ^ Grimaux, E. (1879). "Synthèse des dérivés uriques de la série de l'alloxane". Comptes rendus hebdomadaires des séances de l'Académie des Sciences. 88: 85–87.
- ^ Kenner, G.W.; Todd, Sir Alexander (1957). Elderfield, R.C., ed. Heterocyclic Compounds, Volume 6. New York: Wiley. hlm. 235.
- ^ Pinner, A. (1884). "Ueber die Einwirkung von Acetessigëther auf die Amidine". Berichte der Deutschen Chemischen Gesellschaft. A17: 2519–2520.
- ^ Pinner, A. (1885). "Ueber die Einwirkung von Acetessigëther auf die Amidine. Pyrimidine". Berichte der Deutschen Chemischen Gesellschaft. A18: 759–760.
- ^ Gabriel, S. (1900). "Pyrimidin aus Barbitursäure". Berichte der Deutschen Chemischen Gesellschaft. A33: 3666.
- ^ Lythgoe, B.; Rayner, L. S. (1951). "Substitution Reactions of Pyrimidine and its 2- and 4-Phenyl Derivatives". Journal of the Chemical Society: 2323–2329. doi:10.1039/JR9510002323.
- ^ Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. (1994). The Pyrimidines. New York: John Wiley & Sons. hlm. 5–6. ISBN 0-471-50656-7.
- ^ Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. (1994). The Pyrimidines. New York: John Wiley & Sons. hlm. 242–244. ISBN 0-471-50656-7.
- ^ Albert, Adrien (1968). Heterocyclic Chemistry, an Introduction. London: Athlone Press. hlm. 56–62.
- ^ Albert, Adrien (1968). Heterocyclic Chemistry, an Introduction. London: Athlone Press. hlm. 437–439.
- ^ Organic Syntheses, Coll. Vol. 4, p.182 (1963); Vol. 35, p.34 (1955) Link
- ^ Organic Syntheses, Coll. Vol. 4, p.336 (1963); Vol. 35, p.58 (1955) Link
- ^ Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. (1994). The Pyrimidines. New York: John Wiley & Sons. hlm. 4–8. ISBN 0-471-50656-7.
- ^ Nuevo M, Milam SN, Sandford SA, Elsila JE, Dworkin JP (2009). "Formation of uracil from the ultraviolet photo-irradiation of pyrimidine in pure H2O ices". Astrobiology. 9 (7): 683–695. Bibcode:2009AsBio...9..683N. doi:10.1089/ast.2008.0324. PMID 19778279.
- ^ Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. (1994). The Pyrimidines. New York: John Wiley & Sons. hlm. 241–2. ISBN 0-471-50656-7.
- ^ Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. (1994). The Pyrimidines. New York: John Wiley & Sons. hlm. 149–239. ISBN 0-471-50656-7.
- ^ Joule, John A.; Mills, Keith, ed. (2010). Heterocyclic Chemistry (edisi ke-5th). Oxford: Wiley. hlm. 253–4. ISBN 978-1-405-13300-5.