Elektrokimia: Perbedaan antara revisi
k r2.6.5) (bot Menambah: sq:Elektrokimia |
Wagino Bot (bicara | kontrib) k Bot: Merapikan artikel |
||
| (34 revisi perantara oleh 23 pengguna tidak ditampilkan) | |||
| Baris 1: | Baris 1: | ||
[[Berkas:Lead acid cell. |
[[Berkas:Lead acid cell.svg|jmpl|[[Baterai]] asam-timbal|199x199px]] |
||
'''Elektrokimia''' adalah cabang [[Kimia|ilmu kimia]] fisik yang mempelajari aspek [[Listrik|kelistrikan]] dari [[reaksi kimia]]. [[Elemen]] yang digunakan dalam reaksi elektrokimia dikarakterisasikan dengan banyaknya [[elektron]] yang dimiliki. Secara umum elektrokimia terbagi dalam dua kelompok, yaitu [[sel galvani]] dan [[Elektrolisis|sel elektrolisis]]. Reaksi elektrokimia dapat berlangsung secara spontan, yaitu ketika dua [[elektroda]] yang direndam di dalam cairan [[elektrolit]] dihubungkan dengan untai [[listrik]].<ref>{{Cite web|title=Electrochemical reaction {{!}} chemistry|url=https://www.britannica.com/science/electrochemical-reaction|website=Encyclopedia Britannica|language=en|access-date=2020-09-13}}</ref><ref>{{Cite web|title=Electrochemistry {{!}} Encyclopedia.com|url=https://www.encyclopedia.com/science-and-technology/chemistry/chemistry-general/electrochemistry#:~:text=Electrochemistry%20deals%20with%20the%20links,electric%20energy%20by%20chemical%20reactions.|website=www.encyclopedia.com|access-date=2020-09-13}}</ref> Elektrokimia digunakan untuk pemurnian dan pelapisan [[logam]] serta [[elektrosintesis]]. {{Sfn|Ningsih|2016|p=99}} |
|||
'''Elektrokimia''' adalah ilmu yang mempelajari aspek [[elektronik]] dari reaksi kimia. [[Elemen]] yang digunakan dalam [[reaksi kimia|reaksi]] elektrokimia dikarakterisasikan dengan banyaknya [[elektron]] yang dimiliki. |
|||
Elektrokimia secara umum terbagi dalam dua kelompok, yaitu [[sel galvani]] dan [[sel elektrolisis]]. |
|||
== Jenis == |
|||
Metode elektrokimia didasarkan pada [[Redoks|reaksi redoks]] yang menggabungkan proses oksidasi dan reduksi. Reaksi ini dilakukan pada elektroda yang sama maupun yang berbeda. Sistem elektrokimia terbentuk melalui reaksi elektrokimia yang ditimbulkan oleh [[sel elektrokimia]]. Sel elektrokimia terbagi menjadi dua jenis yaitu sel galvani dan sel elektrolisis. Sel galvani menghasilkan listrik karena adanya reaksi spontan, sedangkan sel elektrolisis menghasilkan listrik karena adanya reaksi yang tidak spontan.{{Sfn|Ningsih|2016|p=99}} Reaksi yang terjadi pada sel elektrolisis disebabkan oleh perbedaan potensial yang dipicu dari luar sistem.<ref>{{Cite journal|last=Farandy|first=Gustav|last2=Suwandi|last3=Fitriyanti|first3=Nurwulan|date=Desember 2020|title=PENGARUH KONSENTRASI DAN TEMPERATUR TERHADAP DAYADAN TEGANGAN KELUARAN LISTRIK PADA BATERAI AIR GARAMDENGAN METODE SEL ELEKTROKIMIA|url=https://openlibrary.telkomuniversity.ac.id/pustaka/files/163227/jurnal_eproc/pengaruh-konsentrasi-dan-temperatur-terhadap-daya-dan-tegangan-keluaran-listrik-pada-baterai-air-garam-dengan-metode-sel-elektrokimia.pdf|journal=e-Proceeding of Engineering|volume=7|issue=3|pages=9278-9285|isbn=2355-9365}}</ref> |
|||
== Redoks == |
|||
[[Berkas:Redox reaction.png|jmpl|Ilustrasi reaksi redoks]] |
|||
[[Redoks]] merupakan istilah yang menjelaskan berubahnya [[bilangan oksidasi]] (keadaan oksidasi) atom-atom dalam sebuah [[reaksi kimia]]. Istilah redoks berasal dari dua konsep, yaitu '''red'''uksi dan '''oks'''idasi.<ref>{{Cite web|title=Redox Reactions|url=http://www.chemistry.wustl.edu/~coursedev/Online%20tutorials/Redox.htm|website=www.chemistry.wustl.edu|access-date=2020-09-14}}</ref><ref>{{Cite web|title=Definitions of oxidation and reduction (redox)|url=https://www.chemguide.co.uk/inorganic/redox/definitions.html|website=www.chemguide.co.uk|access-date=2020-09-14}}</ref> |
|||
* '''''Oksidasi''''' menjelaskan '''''pelepasan''''' [[elektron]] oleh sebuah [[molekul]], [[atom]], atau [[ion]] |
|||
* '''''Reduksi''''' menjelaskan '''''penambahan''''' [[elektron]] oleh sebuah [[molekul]], [[atom]], atau [[ion]]. |
|||
=== [[Oksidator]] dan [[reduktor]] === |
|||
Oksidator adalah zat yang mengoksidasi zat lain dalam suatu reaksi redoks. Sedangkan reduktor adalah zat yang mereduksi zat lain dalam suatu reaksi redoks.<ref>{{Cite web|title=Oxidizing and Reducing Agents|url=https://chemed.chem.purdue.edu/genchem/topicreview/bp/ch19/oxred_3.php|website=chemed.chem.purdue.edu|access-date=2020-09-14}}</ref> |
|||
* '''Oksidator''' adalah zat yang '''mengalami reduksi'''. |
|||
* '''Reduktor''' adalah zat yang '''mengalami oksidasi'''. |
|||
== Fenomena alam == |
|||
=== Korosi === |
|||
[[Korosi]] merupakan kerusakan logam yang terjadi akibat reaksi elektrokimia ataupun reaksi kimia secara langsung. Peristiwa korosi yang paling umum ditemukan adalah [[karat]] pada [[besi]], [[noda]] pada [[perak]], serta [[platina]] hijau yang terbentuk pada [[tembaga]] dan [[Kuningan (logam)|kuningan]]. Medium korosi dapat dalam keadaan kering maupun basah. Contoh korosi yang berlangsung di dalam medium kering yaitu karat logam besi oleh gas [[oksigen]] atau oleh gas [[belerang dioksida]]. Sedangkan contoh korosi yang berlangsung dalam medium basah yaitu besi yang direndam dalam [[asam klorida]]. Kerusakan akibat korosi memberikan kerugian dalam bidang [[industri]] maupun [[ekonomi]].<ref>{{Cite book|last=Subarkah, C. Z., dan Chusni, M. M.|first=|date=2018|url=http://digilib.uinsgd.ac.id/21824/1/Nilai%20Keislaman%20Pada%20Pembelajaran%20Elektrokimia.pdf|title=Nilai Keislaman pada Pembelajaran Elektrokimia|location=Bandung|publisher=Pusat Penelitian dan Penerbitan, Universitas Islam Negeri Sunan Gunung Djati Bandung|isbn=978-602-582-301-5|pages=69|url-status=live|quote="Korosi pada umumnya digunakan sebagai istilah untuk kerusakan logam pada proses elektrokimia. Contoh peristiwa korosi sangat banyak dan yang paling umum adalah karat pada besi. Selain itu, noda pada perak, platina hijau yang terbentuk pada tembaga dan kuningan. Korosi mengakibatkan berbagai kerusakan dalam bidang industri maupun perekonomian (...). Dua jenis mekanisme utama dari korosi adalah berdasarkan reaksi kimia secara langsung, dan reaksi elektrokimia. Korosi dapat terjadi didalam medium kering dan juga medium basah. Sebagai contoh korosi yang berlangsung di dalam medium kering adalah penyerangan logam besi oleh gas oksigen (O2) atau oleh gas belerang dioksida (SO2), sedangkan korosi yang berlangsung dalam medium basah contohnya adalah besi yang direndam dalam HCl (...)."}}</ref> |
|||
== Penerapan == |
|||
=== Elektrosintesis === |
|||
Elektrosintesis adaah salah satu teknik [[Sintesis kimia|sintesis]] yang diterapkan pada bahan [[Senyawa anorganik|anorganik]]. Prinsip dasar elektrosintesis adalah elektrokimia. Peralatan yang digunakan dalam proses elektrosintesis yaitu dua atau tiga batang elektroda yang dihubungkan dengan [[arus listrik]]. Pengaturan kecepatan rekasi dilakukan dengan mengatur [[Gaya gerak proton|beda potensial]] dan tingkat kerapatan arus listrik pada batas-batas yang diinginkan. Sintesis yang menggunakan metode elektrosintesis mudah untuk dikendalikan dan memiliki tingkat [[Pencemaran|polusi]] yang sangat rendah.{{Sfn|Ningsih|2016|p=100}} |
|||
=== Tranduser gas === |
|||
[[Transduser]] gas merupakan transduser yang berfungsi untuk mengetahui keberadaan atau mengukur kuantitas suatu gas tertentu. Salah satu prinsip kerja yang dapat diterapkan pada transduser gas ialah [[sensor]] gas elektrokimia.{{Sfn|Yusro dan Diamah|2019|p=82}} Gas target akan memberikan reaksi kepada sensor gas elektrokimia dan menghasilkan [[Sinyal (elektrik)|sinyal]] listrik. Besarnya nilai sinyal listrik yang dikirim sebanding dengan [[Konsentrasi Massa|konsentrasi]] gas. Sensor gas elektrokimia terdiri dari dua buah elektroda yang masing-masing berfungsi sebagai penginderaan dan pencacah kuantitas gas. Kedua elektroda ini dipisahkan oleh lapisan elektrolit yang tipis.{{Sfn|Yusro dan Diamah|2019|p=83}} Sebelum gas bersentuhan dengan sensor, gas melewati bukaan kapiler tipis dan mengalami difusi selama melalui penghalang [[hidrofobik]] hingga mencapai permukaan elektroda. Penghalang hidrofobik mencegah terjadinya kebocoran elektrolit cair dan menghasilkan sinyal listrik yang cukup di elektroda penginderaan.{{Sfn|Yusro dan Diamah|2019|p=83-84}} Sensor gas elektrokimia juga memiliki elektroda referensi yang bertugas mempertahankan reaksi elektrokimia berkelanjutan yang terjadi pada permukaan elektroda. Elektroda referensi ini membuat beda potensial yang stabil dan konstan pada elektroda penginderaan. Gas target yang mengalami reaksi elektrokimia menghasilkan aliran arus antara elektroda penginderaan dan pencacah. Pelintasan [[muatan listrik]] di elektrida dilakukan oleh elektrolit.{{Sfn|Yusro dan Diamah|2019|p=84}} |
|||
=== Pembuatan parasetamol === |
|||
[[Parasetamol]] dapat dibuat dengan menggunakan reduksi elektrokimia yang memanfaatkan bahan baku berupa [[nitrobenzena]]. Pembuatan parasetamol dengan reduksi elektrokimia menghasilkan [[rendemen reaksi]] yang efisien dan memiliki kapasitas [[obat]] yang cukup besar. Proses elektrokimia dalam pembuatan parasetamol memerlukan energi yang sangat besar.<ref>{{Cite book|last=|first=|date=2016|url=http://perpustakaan.bappenas.go.id/lontar/file?file=digital/192263-[_Konten_]-Konten%20E2474.pdf|title=Outlook Teknologi Kesehatan: Teknologi untuk Industri Farmasi dan Alat Kesehatan Nasional Proyeksi 2035|location=Tangerang Selatan|publisher=Pusat Teknologi Farmasi dan Medika|isbn=978-602-95911-2-5|editor-last=Sumaryono, W., Dewi, E. L., dan Paryanto, I.|pages=83|url-status=live|access-date=2021-05-01|archive-date=2021-01-12|archive-url=https://web.archive.org/web/20210112163313/http://perpustakaan.bappenas.go.id/lontar/file?file=digital%2F192263-%5B_Konten_%5D-Konten%20E2474.pdf|dead-url=yes}}</ref> |
|||
=== Potensiometri === |
|||
Pada potensiometri, pengukuran didasarkan pada beda potensial sel elektrokimia saat sedang tidak dialiri oleh arus listrik.{{Sfn|Iyabu|2014|p=5}} Elektrokimia dapat digunakan pada [[elektroda selektif ion]] dalam metode [[elektronalisis]]. Elektroda selektif ion adalah alat ukur yang digunakan untuk melakukan analisis nilai [[ion]] secara kuantitasi. Analisis dilakukan dengan bantuan sensor elektrokimia. Keaktifan rekasi ion akan memberikan perubahan beda potensial terjadi secara berulang-ulang. Elektroda selektif ion memanfaatkan sel elektrokimia sebagai sensor yang menggunakan [[Membran penukar ion|membran]] selektif ion.{{Sfn|Iyabu|2014|p=13}} Proses elektrokimia dalam potensiometri menggunakan elektroda selektif ion dengan [[asam sulfat]] yang memiliki membran Aliquat-336. Elektroda selektif ion terbuat dari suatu [[penghantar listrik]] berupa kawat platina yang dilapisi oleh membran.{{Sfn|Iyabu|2014|p=32}} |
|||
== Lihat pula == |
|||
* [[Kimia fisik]] |
|||
* Redoks |
|||
== Referensi == |
|||
<references /> |
|||
== Daftar pustaka == |
|||
# {{cite book|last=Iyabu|first=Hendri|date=|year=2014|url=https://repository.ung.ac.id/get/karyailmiah/4598/Pengantar-Eletrode-Seletif-Ion.pdf|title=Pengantar Elektrode Selektif Ion|location=Gorontalo|publisher=UNG Press|isbn=978-979-1340-70-0|pages=|ref={{sfnref|Iyabu|2014}}|url-status=live}} |
|||
# {{cite book|last=Ningsih|first=Sherly Kasuma Warda|date=|year=2016|url=http://repository.unp.ac.id/448/1/Buku%20Sintesis%20Anorganik.pdf|title=Sintesis Anorganik|location=Padang|publisher=UNP Press|isbn=978-602-1178-14-0|pages=|ref={{sfnref|Ningsih|2016}}|url-status=live}} |
|||
# {{cite book|last=Yusro, M., dan Diamah, A.|first=|date=|year=2019|url=http://www.myusro.id/wp-content/uploads/2020/06/BUKU-AJAR-SENSOR-TRANSDUSER_WATERMARK.pdf|title=Sensor dan Transduser: Teori dan Aplikasi|location=Jakarta|publisher=Program Studi Pendidikan Teknik Elektronika, Fakultas Teknik, Universitas Negeri Jakarta|isbn=|pages=|ref={{sfnref|Yusro dan Diamah|2019}}|url-status=live}} |
|||
{{CabangKimia}} |
{{CabangKimia}} |
||
{{kimia-stub}} |
|||
{{authority control}} |
|||
[[Kategori:Elektrokimia| {{PAGENAME}}]] |
|||
[[Kategori:Elektrokimia| ]] |
|||
[[ar:كيمياء كهربية]] |
|||
[[be:Электрахімія]] |
|||
[[be-x-old:Электрахімія]] |
|||
{{kimia-stub}} |
|||
[[bg:Електрохимия]] |
|||
[[bs:Elektrohemija]] |
|||
[[ca:Electroquímica]] |
|||
[[cs:Elektrochemie]] |
|||
[[de:Elektrochemie]] |
|||
[[el:Ηλεκτροχημεία]] |
|||
[[en:Electrochemistry]] |
|||
[[eo:Elektrokemio]] |
|||
[[es:Electroquímica]] |
|||
[[et:Elektrokeemia]] |
|||
[[fa:الکتروشیمی]] |
|||
[[fi:Sähkökemia]] |
|||
[[fr:Électrochimie]] |
|||
[[gl:Electroquímica]] |
|||
[[he:אלקטרוכימיה]] |
|||
[[hi:विद्युत्-रसायन]] |
|||
[[hr:Elektrokemija]] |
|||
[[hu:Elektrokémia]] |
|||
[[it:Elettrochimica]] |
|||
[[ja:電気化学]] |
|||
[[kk:Электрохимия]] |
|||
[[ko:전기화학]] |
|||
[[la:Electrochemia]] |
|||
[[lb:Elektrochimie]] |
|||
[[lmo:Eletruchimica]] |
|||
[[nl:Elektrochemie]] |
|||
[[no:Elektrokjemi]] |
|||
[[pl:Elektrochemia]] |
|||
[[pt:Eletroquímica]] |
|||
[[ro:Electrochimie]] |
|||
[[ru:Электрохимия]] |
|||
[[scn:Alittrochìmica]] |
|||
[[simple:Electrochemistry]] |
|||
[[sl:Elektrokemija]] |
|||
[[sq:Elektrokimia]] |
|||
[[su:Éléktrokimia]] |
|||
[[sv:Elektrokemi]] |
|||
[[ta:மின்வேதியியல்]] |
|||
[[th:ไฟฟ้าเคมี]] |
|||
[[tr:Elektrokimya]] |
|||
[[uk:Електрохімія]] |
|||
[[vi:Điện hóa]] |
|||
[[zh:电化学]] |
|||
Revisi terkini sejak 30 Agustus 2023 03.56

Elektrokimia adalah cabang ilmu kimia fisik yang mempelajari aspek kelistrikan dari reaksi kimia. Elemen yang digunakan dalam reaksi elektrokimia dikarakterisasikan dengan banyaknya elektron yang dimiliki. Secara umum elektrokimia terbagi dalam dua kelompok, yaitu sel galvani dan sel elektrolisis. Reaksi elektrokimia dapat berlangsung secara spontan, yaitu ketika dua elektroda yang direndam di dalam cairan elektrolit dihubungkan dengan untai listrik.[1][2] Elektrokimia digunakan untuk pemurnian dan pelapisan logam serta elektrosintesis. [3]
Jenis
[sunting | sunting sumber]Metode elektrokimia didasarkan pada reaksi redoks yang menggabungkan proses oksidasi dan reduksi. Reaksi ini dilakukan pada elektroda yang sama maupun yang berbeda. Sistem elektrokimia terbentuk melalui reaksi elektrokimia yang ditimbulkan oleh sel elektrokimia. Sel elektrokimia terbagi menjadi dua jenis yaitu sel galvani dan sel elektrolisis. Sel galvani menghasilkan listrik karena adanya reaksi spontan, sedangkan sel elektrolisis menghasilkan listrik karena adanya reaksi yang tidak spontan.[3] Reaksi yang terjadi pada sel elektrolisis disebabkan oleh perbedaan potensial yang dipicu dari luar sistem.[4]
Redoks
[sunting | sunting sumber]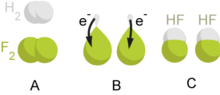
Redoks merupakan istilah yang menjelaskan berubahnya bilangan oksidasi (keadaan oksidasi) atom-atom dalam sebuah reaksi kimia. Istilah redoks berasal dari dua konsep, yaitu reduksi dan oksidasi.[5][6]
- Oksidasi menjelaskan pelepasan elektron oleh sebuah molekul, atom, atau ion
- Reduksi menjelaskan penambahan elektron oleh sebuah molekul, atom, atau ion.
Oksidator dan reduktor
[sunting | sunting sumber]Oksidator adalah zat yang mengoksidasi zat lain dalam suatu reaksi redoks. Sedangkan reduktor adalah zat yang mereduksi zat lain dalam suatu reaksi redoks.[7]
- Oksidator adalah zat yang mengalami reduksi.
- Reduktor adalah zat yang mengalami oksidasi.
Fenomena alam
[sunting | sunting sumber]Korosi
[sunting | sunting sumber]Korosi merupakan kerusakan logam yang terjadi akibat reaksi elektrokimia ataupun reaksi kimia secara langsung. Peristiwa korosi yang paling umum ditemukan adalah karat pada besi, noda pada perak, serta platina hijau yang terbentuk pada tembaga dan kuningan. Medium korosi dapat dalam keadaan kering maupun basah. Contoh korosi yang berlangsung di dalam medium kering yaitu karat logam besi oleh gas oksigen atau oleh gas belerang dioksida. Sedangkan contoh korosi yang berlangsung dalam medium basah yaitu besi yang direndam dalam asam klorida. Kerusakan akibat korosi memberikan kerugian dalam bidang industri maupun ekonomi.[8]
Penerapan
[sunting | sunting sumber]Elektrosintesis
[sunting | sunting sumber]Elektrosintesis adaah salah satu teknik sintesis yang diterapkan pada bahan anorganik. Prinsip dasar elektrosintesis adalah elektrokimia. Peralatan yang digunakan dalam proses elektrosintesis yaitu dua atau tiga batang elektroda yang dihubungkan dengan arus listrik. Pengaturan kecepatan rekasi dilakukan dengan mengatur beda potensial dan tingkat kerapatan arus listrik pada batas-batas yang diinginkan. Sintesis yang menggunakan metode elektrosintesis mudah untuk dikendalikan dan memiliki tingkat polusi yang sangat rendah.[9]
Tranduser gas
[sunting | sunting sumber]Transduser gas merupakan transduser yang berfungsi untuk mengetahui keberadaan atau mengukur kuantitas suatu gas tertentu. Salah satu prinsip kerja yang dapat diterapkan pada transduser gas ialah sensor gas elektrokimia.[10] Gas target akan memberikan reaksi kepada sensor gas elektrokimia dan menghasilkan sinyal listrik. Besarnya nilai sinyal listrik yang dikirim sebanding dengan konsentrasi gas. Sensor gas elektrokimia terdiri dari dua buah elektroda yang masing-masing berfungsi sebagai penginderaan dan pencacah kuantitas gas. Kedua elektroda ini dipisahkan oleh lapisan elektrolit yang tipis.[11] Sebelum gas bersentuhan dengan sensor, gas melewati bukaan kapiler tipis dan mengalami difusi selama melalui penghalang hidrofobik hingga mencapai permukaan elektroda. Penghalang hidrofobik mencegah terjadinya kebocoran elektrolit cair dan menghasilkan sinyal listrik yang cukup di elektroda penginderaan.[12] Sensor gas elektrokimia juga memiliki elektroda referensi yang bertugas mempertahankan reaksi elektrokimia berkelanjutan yang terjadi pada permukaan elektroda. Elektroda referensi ini membuat beda potensial yang stabil dan konstan pada elektroda penginderaan. Gas target yang mengalami reaksi elektrokimia menghasilkan aliran arus antara elektroda penginderaan dan pencacah. Pelintasan muatan listrik di elektrida dilakukan oleh elektrolit.[13]
Pembuatan parasetamol
[sunting | sunting sumber]Parasetamol dapat dibuat dengan menggunakan reduksi elektrokimia yang memanfaatkan bahan baku berupa nitrobenzena. Pembuatan parasetamol dengan reduksi elektrokimia menghasilkan rendemen reaksi yang efisien dan memiliki kapasitas obat yang cukup besar. Proses elektrokimia dalam pembuatan parasetamol memerlukan energi yang sangat besar.[14]
Potensiometri
[sunting | sunting sumber]Pada potensiometri, pengukuran didasarkan pada beda potensial sel elektrokimia saat sedang tidak dialiri oleh arus listrik.[15] Elektrokimia dapat digunakan pada elektroda selektif ion dalam metode elektronalisis. Elektroda selektif ion adalah alat ukur yang digunakan untuk melakukan analisis nilai ion secara kuantitasi. Analisis dilakukan dengan bantuan sensor elektrokimia. Keaktifan rekasi ion akan memberikan perubahan beda potensial terjadi secara berulang-ulang. Elektroda selektif ion memanfaatkan sel elektrokimia sebagai sensor yang menggunakan membran selektif ion.[16] Proses elektrokimia dalam potensiometri menggunakan elektroda selektif ion dengan asam sulfat yang memiliki membran Aliquat-336. Elektroda selektif ion terbuat dari suatu penghantar listrik berupa kawat platina yang dilapisi oleh membran.[17]
Lihat pula
[sunting | sunting sumber]- Kimia fisik
- Redoks
Referensi
[sunting | sunting sumber]- ^ "Electrochemical reaction | chemistry". Encyclopedia Britannica (dalam bahasa Inggris). Diakses tanggal 2020-09-13.
- ^ "Electrochemistry | Encyclopedia.com". www.encyclopedia.com. Diakses tanggal 2020-09-13.
- ^ a b Ningsih 2016, hlm. 99.
- ^ Farandy, Gustav; Suwandi; Fitriyanti, Nurwulan (Desember 2020). "PENGARUH KONSENTRASI DAN TEMPERATUR TERHADAP DAYADAN TEGANGAN KELUARAN LISTRIK PADA BATERAI AIR GARAMDENGAN METODE SEL ELEKTROKIMIA" (PDF). e-Proceeding of Engineering. 7 (3): 9278–9285. ISBN 2355-9365 Periksa nilai: length
|isbn=(bantuan). - ^ "Redox Reactions". www.chemistry.wustl.edu. Diakses tanggal 2020-09-14.
- ^ "Definitions of oxidation and reduction (redox)". www.chemguide.co.uk. Diakses tanggal 2020-09-14.
- ^ "Oxidizing and Reducing Agents". chemed.chem.purdue.edu. Diakses tanggal 2020-09-14.
- ^ Subarkah, C. Z., dan Chusni, M. M. (2018). Nilai Keislaman pada Pembelajaran Elektrokimia (PDF). Bandung: Pusat Penelitian dan Penerbitan, Universitas Islam Negeri Sunan Gunung Djati Bandung. hlm. 69. ISBN 978-602-582-301-5.
Korosi pada umumnya digunakan sebagai istilah untuk kerusakan logam pada proses elektrokimia. Contoh peristiwa korosi sangat banyak dan yang paling umum adalah karat pada besi. Selain itu, noda pada perak, platina hijau yang terbentuk pada tembaga dan kuningan. Korosi mengakibatkan berbagai kerusakan dalam bidang industri maupun perekonomian (...). Dua jenis mekanisme utama dari korosi adalah berdasarkan reaksi kimia secara langsung, dan reaksi elektrokimia. Korosi dapat terjadi didalam medium kering dan juga medium basah. Sebagai contoh korosi yang berlangsung di dalam medium kering adalah penyerangan logam besi oleh gas oksigen (O2) atau oleh gas belerang dioksida (SO2), sedangkan korosi yang berlangsung dalam medium basah contohnya adalah besi yang direndam dalam HCl (...).
- ^ Ningsih 2016, hlm. 100.
- ^ Yusro dan Diamah 2019, hlm. 82.
- ^ Yusro dan Diamah 2019, hlm. 83.
- ^ Yusro dan Diamah 2019, hlm. 83-84.
- ^ Yusro dan Diamah 2019, hlm. 84.
- ^ Sumaryono, W., Dewi, E. L., dan Paryanto, I., ed. (2016). Outlook Teknologi Kesehatan: Teknologi untuk Industri Farmasi dan Alat Kesehatan Nasional Proyeksi 2035 (PDF). Tangerang Selatan: Pusat Teknologi Farmasi dan Medika. hlm. 83. ISBN 978-602-95911-2-5. Diarsipkan dari versi asli (PDF) tanggal 2021-01-12. Diakses tanggal 2021-05-01.
- ^ Iyabu 2014, hlm. 5.
- ^ Iyabu 2014, hlm. 13.
- ^ Iyabu 2014, hlm. 32.
Daftar pustaka
[sunting | sunting sumber]- Iyabu, Hendri (2014). Pengantar Elektrode Selektif Ion (PDF). Gorontalo: UNG Press. ISBN 978-979-1340-70-0.
- Ningsih, Sherly Kasuma Warda (2016). Sintesis Anorganik (PDF). Padang: UNP Press. ISBN 978-602-1178-14-0.
- Yusro, M., dan Diamah, A. (2019). Sensor dan Transduser: Teori dan Aplikasi (PDF). Jakarta: Program Studi Pendidikan Teknik Elektronika, Fakultas Teknik, Universitas Negeri Jakarta.
