Neon: Perbedaan antara revisi
k clean up, added underlinked tag |
FelixJL111 (bicara | kontrib) Tidak ada ringkasan suntingan Tag: Suntingan visualeditor-wikitext |
||
| (8 revisi perantara oleh 4 pengguna tidak ditampilkan) | |||
| Baris 1: | Baris 1: | ||
{{Tentang|unsur kimia}} |
|||
{{Underlinked|date=Januari 2023}} |
|||
{{Kotak info neon}} |
{{Kotak info neon}} |
||
{{Unsur|Neon|Ne|10}} Neon termasuk dalam golongan [[gas mulia]].<ref>Golongan 18 mengacu pada penomoran modern dari tabel periodik. Penomoran yang lebih lama menggambarkan gas mulia sebagai Golongan 0 atau Golongan VIIIA (terkadang disingkat menjadi 8). Lihat pula [[Golongan tabel periodik]].</ref> Neon adalah [[gas monoatomik]] lengai yang nirwarna dan nirbau pada [[temperatur dan tekanan standar|kondisi standar]], dengan massa jenis sekitar dua pertiga udara. Ia ditemukan (bersama dengan [[kripton]] dan [[xenon]]) pada tahun 1898 sebagai salah satu dari tiga unsur lengai sisa yang tersisa di udara kering, setelah [[nitrogen]], [[oksigen]], [[argon]], dan [[karbon dioksida]] dihilangkan. Neon adalah yang kedua dari tiga gas langka ini yang ditemukan dan segera dikenali sebagai unsur baru dari [[spektrum pancar|spektrum emisi]] merah terangnya. Nama neon berasal dari kata Yunani, {{lang|grc|νέον}}, bentuk tunggal netral dari {{lang|grc|νέος}} ({{transl|grc|neos}}), yang berarti 'baru'. Neon bersifat [[gas lengai|lengai]] secara kimiawi, dan tidak ada senyawa neon yang tak bermuatan yang diketahui. [[Senyawa neon]] yang saat ini dikenal meliputi molekul ionik, molekul yang disatukan oleh [[gaya van der Waals]] dan [[Senyawa klatrat|klatrat]]. |
|||
{{unsur|Neon|Ne|10}} '''Neon''' termasuk kelompok [[gas mulia]] yang tak berwarna dan lembam (''inert''). Zat ini memberikan pendar khas kemerahan jika digunakan di tabung hampa (''vacuum discharge tube'') dan lampu neon. Sifat ini membuat neon terutama dipergunakan sebagai bahan pembuatan tanda (''sign''). |
|||
Selama [[Nukleosintesis|nukleogenesis]] kosmik unsur-unsur, sejumlah besar neon dibangun dari proses fusi penangkapan alfa di dalam bintang. Meskipun neon adalah unsur yang sangat umum di alam semesta dan tata surya (berada kelima dalam kelimpahan kosmik setelah [[hidrogen]], [[helium]], [[oksigen]], dan [[karbon]]), neon jarang ditemukan di Bumi. Ia menyusun sekitar 18,2 ppm udara berdasarkan volume (ini hampir sama dengan fraksi molekul atau mol) dan fraksi yang lebih kecil di kerak bumi. Alasan kelangkaan relatif neon di Bumi dan [[planet kebumian|planet bagian dalam (terestrial)]] adalah karena neon sangat [[Volatilitas (kimia)|volatil]] dan tidak membentuk senyawa untuk memperbaikinya menjadi padat. Akibatnya, ia lepas dari [[planetisimal]] di bawah kehangatan Matahari yang baru tersulut di Tata Surya awal. Bahkan atmosfer luar [[Jupiter]] agak kehabisan neon, meski untuk alasan yang berbeda.<ref name="Wilson2010">{{citation | title=Sequestration of Noble Gases in Giant Planet Interiors | last1=Wilson | first1=Hugh F. | last2=Militzer | first2=Burkhard | journal=Physical Review Letters | volume=104 | issue=12 | pages=121101 | id=121101 | date=March 2010 | doi=10.1103/PhysRevLett.104.121101 | pmid=20366523 | bibcode=2010PhRvL.104l1101W | arxiv=1003.5940 | s2cid=9850759 | postscript=. }}</ref> |
|||
== Pranala luar == |
|||
{{Commons|Neon}} |
|||
* {{en}} [http://www.webelements.com/webelements/elements/text/Ne/index.html WebElements.com – Neon] |
|||
* {{en}} [http://education.jlab.org/itselemental/ele010.html It's Elemental – Neon] |
|||
* {{en}} [http://www.compchemwiki.org/index.php?title=Neon Computational Chemistry Wiki] {{Webarchive|url=https://web.archive.org/web/20090430091458/http://www.compchemwiki.org/index.php?title=Neon |date=2009-04-30 }} |
|||
* {{en}} [http://inventors.about.com/library/weekly/aa980107.htm The history of neon signs ] |
|||
Neon memberikan pancaran oranye kemerahan yang berbeda saat digunakan pada [[lampu neon|lampu pijar neon]] [[Volt|bertegangan]] rendah, [[Tabung Geissler tube|tabung lucutan]], dan [[tanda neon|tanda iklan neon]].<ref>{{cite book |title = Project STAR: The Universe in Your Hands|author = Coyle, Harold P. |publisher = Kendall Hunt|date = 2001|isbn = 978-0-7872-6763-6|url = https://books.google.com/books?id=KwTzo4GMlewC&pg=PA127 |pages = 464}}</ref><ref>{{cite book|chapter = Phosphors for lamps |title = Phosphor Handbook|editor = Shionoya, Shigeo|editor2 = Yen, William M. |author = Kohmoto, Kohtaro |publisher = CRC Press|date = 1999|isbn = 978-0-8493-7560-6|chapter-url = https://books.google.com/books?id=lWlcJEDukRIC&pg=PA380|pages = 940}}</ref> Garis emisi merah dari neon juga menyebabkan lampu merah dari [[laser helium–neon]]. Neon digunakan dalam beberapa tabung plasma dan aplikasi pendingin tetapi memiliki beberapa kegunaan komersial lainnya. Ia diekstraksi secara komersial dengan [[distilasi fraksional]] dari [[udara cair]]. Karena udara adalah satu-satunya sumber, ia jauh lebih mahal daripada helium. |
|||
== Referensi == |
|||
==Sejarah== |
|||
{{reflist}} |
|||
[[Berkas:NeTube.jpg|thumb|left|[[Lampu lucutan gas]] neon yang membentuk lambang neon]] |
|||
{{clr}} |
|||
Neon ditemukan pada tahun 1898 oleh kimiawan Inggris Sir [[Sir William Ramsay|William Ramsay]] (1852–1916) dan [[Morris Travers]] (1872–1961) di [[London]].<ref>{{cite journal |title = On the Companions of Argon |author = [[William Ramsay|Ramsay, William]], Travers, Morris W. |journal = Proceedings of the Royal Society of London |volume = 63 |issue = 1 |pages = 437–440 |date = 1898 |doi = 10.1098/rspl.1898.0057|s2cid = 98818445 }}</ref> Neon ditemukan ketika Ramsay mendinginkan sampel udara hingga menjadi cairan, kemudian menghangatkan cairan tersebut dan menangkap gas saat mendidih. Gas [[nitrogen]], [[oksigen]], dan [[argon]] telah diidentifikasi, tetapi gas yang tersisa diisolasi menurut urutan kelimpahannya, dalam periode enam minggu yang dimulai pada akhir Mei 1898. Yang pertama diidentifikasi adalah [[kripton]]. Berikutnya, setelah kripton dihilangkan, adalah gas yang memberikan cahaya merah cemerlang di bawah lucutan spektroskopi. Gas ini, diidentifikasi pada bulan Juni, diberi nama "neon", analog bahasa Yunani dari bahasa Latin ''novum'' ('baru')<ref>{{cite web |url=http://nautilus.fis.uc.pt/st2.5/scenes-e/elem/e01000.html |title=Neon: History |access-date=25 Maret 2023 |publisher=Softciências |url-status=dead |archive-url=https://web.archive.org/web/20070314232318/http://nautilus.fis.uc.pt/st2.5/scenes-e/elem/e01000.html |archive-date=14 Maret 2007 }}</ref> yang disarankan oleh putra Ramsay. Karakteristik warna merah-oranye cemerlang yang dipancarkan oleh gas neon saat dieksitasi secara elektrik segera dicatat. Travers kemudian menulis: "kobaran cahaya merah dari tabung menceritakan kisahnya sendiri dan merupakan pemandangan yang harus diingat dan tidak pernah dilupakan."<ref>{{cite book|url=https://books.google.com/books?id=SJIk9BPdNWcC&pg=PA287|title=Discovery of the Elements: Third Edition (reprint)|last=Weeks|first=Mary Elvira|date=2003|publisher=Kessinger Publishing|isbn=978-0-7661-3872-8|page=287|author-link=Mary Elvira Weeks|archive-url=https://web.archive.org/web/20150322191804/http://books.google.com/books?id=SJIk9BPdNWcC&pg=PA287|archive-date=22 Maret 2015|url-status=live}}<!--Ini adalah kutipan penting. Ia menghilangkan banyak klaim bahwa Claude adalah orang pertama yang mencatat pancaran neon yang cemerlang. Sumber asli yang mungkin adalah buku Travers tahun 1928: {{cite book |title=The Discovery of the Rare Gases |url=https://archive.org/details/discoveryofrareg0000trav |url-access=registration |last=Travers |first=Morris W. |publisher=Edward Arnold & Co. |location=London |year=1928}}--></ref> |
|||
{{Portal|kimia}} |
|||
{{Compact periodic table}} |
|||
Gas kedua juga dilaporkan bersama dengan neon, memiliki massa jenis yang kira-kira sama dengan argon tetapi dengan spektrum yang berbeda – Ramsay dan Travers menamainya ''metargon''.<ref name="Nobel"> |
|||
[[Kategori:Unsur kimia]] |
|||
{{cite web |
|||
[[Kategori:Gas mulia]] |
|||
|url = https://www.nobelprize.org/nobel_prizes/chemistry/laureates/1904/ramsay-lecture.html |
|||
|title = Nobel Lecture – The Rare Gases of the Atmosphere |
|||
|last = Ramsay |
|||
|first = Sir William |
|||
|date = 12 Desember 1904 |
|||
|website = nobelprize.org |
|||
|publisher = Nobel Media AB |
|||
|access-date = 25 Maret 2023 |
|||
|url-status = live |
|||
|archive-url = https://web.archive.org/web/20151113111406/http://www.nobelprize.org/nobel_prizes/chemistry/laureates/1904/ramsay-lecture.html |
|||
|archive-date = 13 November 2015 |
|||
}} |
|||
</ref><ref name="RamsayTravers1898">{{cite journal |last1=Ramsay |first1=William |last2=Travers |first2=Morris W. |title=On the Companions of Argon |journal=Proceedings of the Royal Society of London |volume=63 |issue=1 |year=1898 |pages=437–440 |issn=0370-1662 |doi=10.1098/rspl.1898.0057|s2cid=98818445 }}</ref> Namun, analisis spektroskopi selanjutnya mengungkapkan bahwa itu adalah argon yang terkontaminasi [[karbon monoksida]]. Akhirnya, tim yang sama menemukan [[xenon]] dengan proses yang sama, pada bulan September 1898.<ref name="Nobel" /> |
|||
Kelangkaan neon menghalangi aplikasi cepatnya untuk penerangan di sepanjang garis [[Daniel McFarlan Moore|tabung Moore]], yang menggunakan [[nitrogen]] dan dikomersialkan pada awal 1900-an. Setelah 1902, perusahaan [[Air Liquide]] milik [[Georges Claude]] memproduksi neon dalam jumlah industri sebagai produk sampingan dari bisnis pencairan udaranya. Pada bulan Desember 1910, Claude mendemonstrasikan [[pencahayaan neon]] berdasarkan tabung neon yang disegel. Claude mencoba untuk menjual tabung neon untuk penerangan rumah dalam ruangan, karena intensitasnya, tetapi pasarnya gagal karena pemilik rumah keberatan dengan warnanya. Pada tahun 1912, rekanan Claude mulai menjual tabung neon sebagai [[tanda neon|tanda iklan]] yang menarik perhatian dan langsung menjadi lebih sukses. Tabung neon diperkenalkan ke AS pada tahun 1923 dengan dua lampu neon besar yang dibeli oleh pedagang mobil Los Angeles Packard. Cahaya dan warna merah yang menawan membuat iklan neon benar-benar berbeda dari kompetisi.<ref>{{cite news |
|||
|url = http://nymag.com/shopping/features/41814/ |
|||
|title = Neon: A Brief History |
|||
|last = Mangum |
|||
|first = Aja |
|||
|access-date = 25 Maret 2023 |
|||
|date = 8 Desember 2007 |
|||
|newspaper = New York Magazine |
|||
|url-status = live |
|||
|archive-url = https://web.archive.org/web/20080415165748/http://nymag.com/shopping/features/41814/ |
|||
|archive-date = 15 April 2008 |
|||
}}</ref> Warna intens dan semangat neon disamakan dengan masyarakat Amerika pada saat itu, menunjukkan "abad kemajuan" dan mengubah kota menjadi lingkungan baru yang sensasional yang dipenuhi dengan iklan yang memancar dan "arsitektur elektro-grafis".<ref>{{Cite journal |last=Golec |first=Michael J. |year=2010 |title=Logo/Local Intensities: Lacan, the Discourse of the Other, and the Solicitation to "Enjoy" |journal=Design and Culture |volume=2 |issue=2|pages=167–181 |doi=10.2752/175470710X12696138525622 |s2cid=144257608 }}</ref><ref>{{Cite news |title=Electro-Graphic Architecture |last=Wolfe |first=Tom |date=Oktober 1968 |work=Architecture Canada }}</ref> |
|||
Neon berperan dalam pemahaman dasar tentang sifat atom pada tahun 1913, ketika [[Joseph John Thomson|J. J. Thomson]], sebagai bagian dari penjelajahannya ke dalam komposisi [[sinar anode|sinar kanal]], menyalurkan aliran ion neon melalui medan magnet dan listrik dan mengukur defleksi dari aliran dengan pelat fotografi. Thomson mengamati dua petak cahaya terpisah pada pelat fotografi (lihat gambar), yang memperkirakan dua defleksi parabola yang berbeda. Thomson akhirnya menyimpulkan bahwa beberapa [[atom]] dalam [[gas]] neon memiliki massa yang lebih tinggi daripada yang lain. Meskipun pada saat itu tidak dipahami oleh Thomson, ini adalah penemuan pertama dari [[isotop]] atom [[Nuklida stabil|stabil]]. Perangkat Thomson adalah versi mentah dari instrumen yang sekarang kita sebut sebagai [[Spektrometri massa|spektrometer massa]]. |
|||
{{kimia-stub}} |
|||
==Isotop== |
|||
{{Utama|Isotop neon}} |
|||
[[Berkas:Discovery of neon isotopes.JPG|thumb|left|Bukti pertama untuk isotop unsur stabil diberikan pada tahun 1913 melalui percobaan pada plasma neon. Di pojok kanan bawah pelat foto [[Joseph John Thomson|J. J. Thomson]] terdapat tanda tumbukan terpisah untuk dua isotop neon-20 dan neon-22.]] |
|||
Neon memiliki tiga [[Nuklida stabil|isotop stabil]]: <sup>20</sup>Ne (90,48%), <sup>21</sup>Ne (0,27%) dan <sup>22</sup>Ne (9,25%).<ref>{{NUBASE2020}}</ref> |
|||
<sup>21</sup>Ne dan <sup>22</sup>Ne bersifat sebagian [[Nuklida primordial|primordial]] dan sebagian [[nukleogenik]] (yaitu dibuat oleh reaksi nuklir nuklida lain dengan neutron atau partikel lain di lingkungan) dan variasinya dalam [[Kelimpahan alami unsur|kelimpahan alami]] telah dipahami dengan baik. Sebaliknya, <sup>20</sup>Ne ([[Nuklida primordial|isotop primordial]] utama yang dibuat dalam [[nukleosintesis]] bintang) tidak diketahui bersifat nukleogenik atau [[Nuklida radiogenik|radiogenik]], kecuali dari peluruhan [[Isotop oksigen|oksigen-20]], yang dihasilkan dalam kasus [[peluruhan gugus]] yang sangat jarang oleh [[Isotop torium#Torium-228|torium-228]]. Dengan demikian, penyebab variasi <sup>20</sup>Ne di Bumi telah diperdebatkan dengan hangat.<ref>{{cite book|isbn = 978-0-521-82316-6|chapter = Neon|page = 303|chapter-url = https://books.google.com/books?id=z8ZCg2HRvWsC&pg=PA303|title = Radiogenic isotope geology|author1 = Dickin, Alan P|date = 2005}}{{Pranala mati|date=Mei 2023 |bot=InternetArchiveBot |fix-attempted=yes }}</ref><ref name="wwwrcanml"/> |
|||
[[Reaksi nuklir]] utama yang menghasilkan [[isotop]] neon nukleogenik dimulai dari <sup>24</sup>Mg dan <sup>25</sup>Mg, yang masing-masing menghasilkan <sup>21</sup>Ne dan <sup>22</sup>Ne, setelah [[Tangkapan neutron|penangkapan neutron]] dan emisi langsung [[partikel alfa]]. [[Neutron]] yang menghasilkan reaksi sebagian besar dihasilkan oleh reaksi spalasi sekunder dari partikel alfa, yang pada gilirannya berasal dari [[Deret radioaktif|rantai peluruhan]] deret [[uranium]]. Hasil bersih menghasilkan kecenderungan rasio <sup>20</sup>Ne/<sup>22</sup>Ne yang lebih rendah dan <sup>21</sup>Ne/<sup>22</sup>Ne yang lebih tinggi yang teramati pada batuan kaya uranium seperti [[granit]].<ref name="wwwrcanml">[http://wwwrcamnl.wr.usgs.gov/isoig/period/ne_iig.html Resources on Isotopes Periodic Table--Neon] di [[Survei Geologi Amerika Serikat|U.S. Geological Survey]], oleh Eric Caldwell, dikirim pada Januari 2004, diakses tanggal 25 Maret 2023</ref> |
|||
Selain itu, analisis isotop batuan terestrial telah menunjukkan produksi [[Nuklida kosmogenik|kosmogenik]] (sinar kosmik) <sup>21</sup>Ne. Isotop ini dihasilkan melalui reaksi [[spalasi]] pada [[magnesium]], [[natrium]], [[silikon]], dan [[aluminium]]. Dengan menganalisis ketiga isotop tersebut, komponen kosmogenik dapat diselesaikan dari neon [[magma]]tik dan neon nukleogenik. Hal ini menunjukkan bahwa neon akan menjadi alat yang berguna dalam menentukan usia paparan kosmik dari batuan permukaan dan [[meteorit]].<ref>{{cite web |url=http://nautilus.fis.uc.pt/st2.5/scenes-e/elem/e01093.html |title=Neon: Isotopes |access-date=25 Maret 2023 |publisher=Softciências |url-status=dead |archive-url=https://web.archive.org/web/20121115190653/http://nautilus.fis.uc.pt/st2.5/scenes-e/elem/e01093.html |archive-date=15 November 2011 }}</ref> |
|||
Neon dalam [[angin surya|angin matahari]] mengandung proporsi <sup>20</sup>Ne yang lebih tinggi daripada sumber nukleogenik dan kosmogenik.<ref name="wwwrcanml"/> Kandungan neon yang teramati dalam sampel [[gas]] [[gunung berapi|vulkanik]] dan [[intan]] juga diperkaya dengan <sup>20</sup>Ne, yang menunjukkan kemungkinan berasal dari matahari purba.<ref>{{cite web |url=http://www.mantleplumes.org/Ne.html |title=Helium, Neon & Argon |access-date=25 Maret 2023 |author=Anderson, Don L. |publisher=Mantleplumes.org |url-status=live |archive-url=https://web.archive.org/web/20060528113659/http://www.mantleplumes.org/Ne.html |archive-date=28 Mei 2006 }}</ref> |
|||
==Karateristik== |
|||
Neon adalah [[gas mulia]] paling ringan kedua setelah [[helium]]. Ia bersinar dengan warna oranye kemerahan dalam [[tabung lucutan|tabung lucutan vakum]]. Ia memiliki lebih dari 40 kali lipat kapasitas pendinginan (per satuan volume) dari helium cair dan tiga kali lipat dari [[hidrogen]] cair.<ref name="CRC" /> Dalam sebagian besar aplikasi, ia adalah [[refrigeran|pendingin]] yang lebih murah daripada helium.<ref>{{cite web |url=http://www.nassmc.org/bulletin/dec05bulletin.html#table |title=NASSMC: News Bulletin |access-date=25 Maret 2023 |date=30 Desember 2005 |url-status=dead |archive-url=https://web.archive.org/web/20070213072031/http://www.nassmc.org/bulletin/dec05bulletin.html |archive-date=13 Februari 2007 }}</ref><ref>{{cite book |url=https://books.google.com/books?id=nhVEI52-VE8C&pg=PA195 |page=195|title=Fundamentals of Cryogenic Engineering |isbn=9788120330573 |last1=Mukhopadhyay |first1=Mamata |date=2012 |url-status=live |archive-url=https://web.archive.org/web/20171116145946/https://books.google.com/books?id=nhVEI52-VE8C&pg=PA195 |archive-date=16 November 2017}}</ref> |
|||
[[Berkas:Neon emission.png|thumb|Spektrum neon dengan garis ultraungu (kiri) dan inframerah (kanan) ditampilkan dalam warna putih|center|600x600px]] |
|||
Plasma neon memiliki pelepasan cahaya paling intens pada tegangan dan arus normal dari semua gas mulia. Warna rata-rata cahaya ini bagi mata manusia adalah merah-oranye karena banyaknya garis dalam kisaran ini; ia juga mengandung garis hijau yang kuat, yang tersembunyi, kecuali komponen visualnya didispersi oleh spektroskop.<ref>{{cite web |url=http://www.electricalfun.com/plasma.htm |title=Plasma |access-date=25 Maret 2023 |url-status=dead |archive-url=https://web.archive.org/web/20070307005259/http://www.electricalfun.com/plasma.htm |archive-date=7 Maret 2007 }}</ref> |
|||
Dua jenis [[pencahayaan neon]] yang sangat berbeda digunakan secara umum. [[Lampu neon]] umumnya kecil, dengan sebagian besar beroperasi antara 100 dan 250 [[volt]].<ref name="Baumann">{{cite book |last=Baumann |first=Edward |title=Applications of Neon Lamps and Gas Discharge Tubes |publisher=Carlton Press |date=1966}}</ref> Mereka telah banyak digunakan sebagai indikator daya dan peralatan pengujian sirkuit, tetapi [[dioda pemancar cahaya]] (LED) sekarang mendominasi dalam aplikasi tersebut. Perangkat neon sederhana ini adalah pelopor [[tampilan plasma|layar plasma dan layar televisi plasma]].<ref name="Myers">{{cite book |title=Display interfaces: fundamentals and standards |last1=Myers |first1=Robert L. |publisher=John Wiley and Sons |date=2002 |pages=69–71 |url=https://books.google.com/books?id=ilHvFwoAZDMC&pg=PA69 |isbn=978-0-471-49946-6 |quote=Tampilan plasma terkait erat dengan lampu neon sederhana. |url-status=live |archive-url=https://web.archive.org/web/20160629141148/https://books.google.com/books?id=ilHvFwoAZDMC&pg=PA69 |archive-date=29 Juni 2016 }}</ref><ref name="Weber">{{cite journal |last=Weber |first=Larry F. |author-link=Larry F. Weber |title=History of the plasma display panel |journal=IEEE Transactions on Plasma Science |volume=34 |issue=2 |date=April 2006 |pages=268–278 |doi=10.1109/TPS.2006.872440 |bibcode=2006ITPS...34..268W|s2cid=20290119 }} Akses berbayar.</ref> [[Tanda neon]] biasanya beroperasi pada voltase yang jauh lebih tinggi (2–15 [[volt|kilovolt]]), dan tabung bercahaya biasanya memiliki panjang beberapa meter.<ref>{{cite web |title=ANSI Luminous Tube Footage Chart |url=http://www.allanson.com/wp-content/uploads/Product_PDFs/ANSI_Luminous_footage.pdf |publisher=[[American National Standards Institute|Institut Standar Nasional Amerika]] (ANSI) |access-date=25 Maret 2023 |url-status=live |archive-url=https://web.archive.org/web/20110206163356/http://www.allanson.com/wp-content/uploads/Product_PDFs/ANSI_Luminous_footage.pdf |archive-date=26 Februari 2011 }} Reproduksi bagan dalam katalog perusahaan penerangan di Toronto; spesifikasi ANSI asli tidak diberikan.</ref> Tabung kaca sering dibentuk menjadi bentuk dan huruf untuk papan nama, serta aplikasi arsitektur dan artistik. |
|||
==Keterjadian== |
|||
Isotop stabil neon diproduksi di dalam bintang. Isotop neon yang paling melimpah <sup>20</sup>Ne (90,48%) diciptakan oleh [[fusi nuklir]] [[karbon]] dan karbon dalam [[proses pembakaran karbon]] [[nukleosintesis bintang]]. Proses ini membutuhkan suhu di atas 500 [[Kelvin|megakelvin]], yang terjadi pada inti bintang dengan massa lebih dari 8 [[Massa Matahari|matahari]].<ref>{{Cite book|url=https://books.google.com/books?id=fXcdHyLUVnEC&q=neon+cosmic+nucleosynthesis&pg=PA106|title=Handbook of Isotopes in the Cosmos: Hydrogen to Gallium|last=Clayton|first=Donald|publisher=Cambridge University Press|year=2003|isbn=978-0521823814|pages=106–107}}</ref><ref>{{cite book|author1=Ryan, Sean G. |author2=Norton, Andrew J. | title=Stellar Evolution and Nucleosynthesis | year=2010 | page=135| isbn=978-0-521-13320-3|publisher=[[Cambridge University Press]]|url=https://books.google.com/books?id=PE4yGiU-JyEC&q=carbong+burning}}</ref> |
|||
Neon berlimpah dalam skala universal; ia adalah [[Kelimpahan unsur|unsur kimia paling melimpah kelima]] di alam semesta berdasarkan massa, setelah hidrogen, helium, oksigen, dan karbon (lihat [[unsur kimia]]).<ref>{{cite journal |bibcode=2009ARA&A..47..481A |doi=10.1146/annurev.astro.46.060407.145222 |title=The Chemical Composition of the Sun |journal=Annual Review of Astronomy and Astrophysics |volume=47 |issue=1 |pages=481–522 |year=2009 |last1=Asplund |first1=Martin |last2=Grevesse |first2=Nicolas |last3=Sauval |first3=A. Jacques |last4=Scott |first4=Pat |arxiv=0909.0948|s2cid=17921922 }}</ref> Kelangkaannya yang relatif di Bumi, seperti helium, adalah karena sifatnya yang relatif ringan, tekanan uapnya yang tinggi pada suhu yang sangat rendah, dan kelengaian kimiawinya, semua sifat yang cenderung mencegahnya terperangkap dalam gas kondensasi dan awan debu yang membentuk planet padat yang lebih kecil dan lebih hangat seperti Bumi. |
|||
Neon bersifat monoatomik, membuatnya lebih ringan daripada molekul nitrogen dan oksigen diatomik yang membentuk sebagian besar atmosfer bumi; balon berisi neon akan naik di udara, meski lebih lambat dari balon helium.<ref>{{cite book |title = Chemistry for Higher Tier |author = Gallagher, R. |author2 = Ingram, P. |publisher = University Press |isbn = 978-0-19-914817-2 |url = https://books.google.com/books?id=SJtWSy69eVsC&pg=PA96 |pages = 282 |date = 19 Juli 2001}}</ref> |
|||
Kelimpahan neon di alam semesta adalah sekitar 1 bagian dalam 750; di Matahari dan mungkin di nebula sistem proto-surya, sekitar 1 bagian dalam 600. Prob atmosfer [[Galileo (wahana antariksa)|wahana antariksa Galileo]] menemukan bahwa bahkan pada atmosfer Jupiter bagian atas, kelimpahan neon berkurang (habis) sekitar faktor 10, ke tingkat 1 bagian dalam 6.000 berdasarkan massa. Hal ini mungkin menunjukkan bahwa [[planetisimal]]-es, yang membawa neon ke Jupiter dari luar tata surya, terbentuk di wilayah yang terlalu hangat untuk mempertahankan komponen atmosfer neon (kelimpahan gas lengai yang lebih berat di Jupiter beberapa kali lebih banyak daripada yang ditemukan di Bumi).<ref>{{cite web |url=http://www2.jpl.nasa.gov/sl9/gll38.html |title=Galileo Probe Science Result |access-date=25 Maret 2023 |last=Morse |first=David |date=26 Januari 1996 |publisher=Galileo Project |url-status=live |archive-url=https://web.archive.org/web/20070224232055/http://www2.jpl.nasa.gov/sl9/gll38.html |archive-date=24 Februari 2007 }}</ref> |
|||
Neon terdiri dari 1 bagian dalam 55.000 di [[atmosfer Bumi]], atau 18,2 ppm berdasarkan volume (ini hampir sama dengan fraksi mol atau molekul), atau 1 bagian dalam 79.000 udara berdasarkan massa. Ia terdiri dari fraksi yang lebih kecil di kerak Bumi. Ia diproduksi secara industri dengan [[distilasi fraksional]]kriogenik dari udara yang telah dicairkan.<ref name="CRC" /> |
|||
Pada 17 Agustus 2015, berdasarkan studi dengan wahana antariksa [[Lunar Atmosphere and Dust Environment Explorer]] (LADEE), ilmuwan NASA melaporkan deteksi neon pada [[eksosfer]] [[Bulan]].<ref name="NASA-20150817">{{cite web |last=Steigerwald |first=William |title=NASA's LADEE Spacecraft Finds Neon in Lunar Atmosphere |url=http://www.nasa.gov/content/goddard/ladee-lunar-neon |date=17 Agustus 2015 |work=[[Badan Penerbangan dan Antariksa|NASA]] |access-date=25 Maret 2023 |url-status=live |archive-url=https://web.archive.org/web/20150819035151/http://www.nasa.gov/content/goddard/ladee-lunar-neon/ |archive-date=19 Agustus 2015 }}</ref> |
|||
==Kimia== |
|||
[[Berkas:Ne-water clathrate.png|thumb|Struktur kristal dari [[klatrat hidrat]] neon<ref name="hydrate" />|300x300px]] |
|||
{{Utama|Senyawa neon}} |
|||
Neon adalah gas mulia [[Blok tabel periodik#Blok-p|blok-p]] pertama, dan unsur pertama dengan oktet elektron yang sebenarnya. Ia bersifat [[lengai]]: seperti analognya yang lebih ringan, [[helium]], tidak ada molekul netral yang terikat kuat yang [[Senyawa neon|mengandung neon]] yang telah diidentifikasi. [[Ion]] [Ne[[argon|Ar]]]<sup>+</sup>, [Ne[[hydrogen|H]]]<sup>+</sup>, dan [HeNe]<sup>+</sup> telah diamati dari studi optik dan [[spektrometri massa]].<ref name="CRC" /> [[Klatrat hidrat]] neon padat diproduksi dari es air dan gas neon pada tekanan 350–480 MPa dan suhu sekitar −30 °C.<ref>{{cite journal |doi=10.1073/pnas.1410690111 |pmid=25002464 |pmc=4115495 |year=2014 |last1=Yu |first1=X. |title=Crystal structure and encapsulation dynamics of ice II-structured neon hydrate |journal=Proceedings of the National Academy of Sciences of the United States of America |volume=111 |issue=29 |pages=10456–61 |last2=Zhu |first2=J. |last3=Du |first3=S. |last4=Xu |first4=H. |last5=Vogel |first5=S. C. |last6=Han |first6=J. |last7=Germann |first7=T. C. |last8=Zhang |first8=J. |last9=Jin |first9=C. |last10=Francisco |first10=J. S. |last11=Zhao |first11=Y. |bibcode=2014PNAS..11110456Y|doi-access=free }}</ref> Atom Ne tidak terikat pada air dan dapat bergerak bebas melalui bahan ini. Mereka dapat diekstraksi dengan menempatkan klatrat ke dalam ruang vakum selama beberapa hari, menghasilkan [[es XVI]], bentuk kristal air yang paling tidak padat.<ref name="hydrate">{{cite journal |doi=10.1038/nature14014 |pmid=25503235 |title=Formation and properties of ice XVI obtained by emptying a type sII clathrate hydrate |journal=Nature |volume=516 |issue=7530 |pages=231–3 |year=2014 |last1=Falenty |first1=Andrzej |last2=Hansen |first2=Thomas C. |last3=Kuhs |first3=Werner F. |bibcode=2014Natur.516..231F|s2cid=4464711 }}</ref> |
|||
[[Elektronegativitas#Elektronegativitas Pauling|Skala keelektronegatifan Pauling]] bergantung pada energi ikatan kimia, tetapi nilai tersebut jelas belum diukur untuk helium dan neon yang lengai. [[Elektronegativitas#Elektronegativitas Allen|Skala keelektronegatifan Allen]], yang hanya bergantung pada energi atom (terukur), mengidentifikasi neon sebagai unsur yang paling elektronegatif, diikuti oleh fluorin dan helium.<ref>{{cite journal |doi=10.1021/ja00207a003 |title=Electronegativity is the average one-electron energy of the valence-shell electrons in ground-state free atoms|year=1989|author=Allen, Leland C.|journal=Journal of the American Chemical Society |volume=111|pages=9003–9014 |issue=25}}</ref> |
|||
Suhu [[titik tripel]] neon (24,5561 K) adalah titik tetap yang ditentukan dalam [[Skala Suhu Internasional 1990]].<ref name="ITS90-1">{{cite web |url=http://www.its-90.com/ |title=The Internet resource for the International Temperature Scale of 1990 |access-date=25 Maret 2023 |url-status=dead |archive-url=https://web.archive.org/web/20090815110916/http://www.its-90.com/ |archive-date=15 Agustus 2009}}</ref> |
|||
==Produksi== |
|||
Neon dihasilkan dari udara di pabrik [[pemisahan udara]] [[kriogenik]]. Campuran fase gas yang terutama terdiri dari nitrogen, neon, dan helium ditarik dari kondensor utama di bagian atas kolom pemisah udara bertekanan tinggi dan diumpankan ke bagian bawah kolom samping untuk [[distilasi]] neon.<ref>{{cite book|author1=[[R. Norris Shreve]]|author2=[[Joseph Brink]]|title=Chemical Process Industries|url=https://archive.org/details/chemicalprocessi0000shre_s8m7|date=1977|isbn=0-07-057145-7|page=[https://archive.org/details/chemicalprocessi0000shre_s8m7/page/113 113]|edition=4}}</ref> Ia kemudian dapat dimurnikan lebih lanjut dari helium. |
|||
Sekitar 70% pasokan neon global diproduksi di [[Ukraina]]<ref>{{cite news |title=Explained: Why the Russia-Ukraine crisis may lead to a shortage in semiconductors |url=https://www.msn.com/en-in/news/in-depth/explained-why-the-russia-ukraine-crisis-may-lead-to-a-shortage-in-semiconductors/ar-AAUZRlP |work=MSN |publisher=[[The Indian Express]] |language=en-IN}}</ref> sebagai produk sampingan dari produksi baja di [[Rusia]].<ref>{{Cite news |last=Alper |first=Alexandra |date=11 Maret 2022 |title=Exclusive: Russia's attack on Ukraine halts half of world's neon output for chips |language=en |work=Reuters |url=https://www.reuters.com/technology/exclusive-ukraine-halts-half-worlds-neon-output-chips-clouding-outlook-2022-03-11/ |access-date=25 Maret 2023}}</ref> {{Hingga|2020}}, perusahaan [[Iceblick]], dengan pabrik di [[Odesa]] dan [[Moskow]], memasok 65% produksi neon dunia, serta 15% [[kripton]] dan [[xenon]].<ref name=Newshour>{{cite web |title=Rare Gasses Supplier Known for Innovation |url=https://the-european-times.com/iceblick/ |website=The European Times |date=2020}}</ref><ref name="2022-02-25_Reuters"/> |
|||
===Kelangkaan 2022=== |
|||
Harga neon global melonjak sekitar 600% setelah [[Aneksasi Krimea 2014|pencaplokan Krimea oleh Rusia pada tahun 2014]],<ref name="arstechnica" /> mendorong beberapa produsen cip untuk mulai beralih dari pemasok Rusia dan Ukraina<ref name="cnbc">{{cite news |title=Chipmakers see limited impact for now, as Russia invades Ukraine |url=https://www.cnbc.com/2022/02/24/chipmakers-see-limited-impact-russia-invasion-ukraine.html |work=CNBC |date=24 Februari 2022 |language=en}}</ref> ke pemasok di [[Tiongkok]].<ref name="2022-02-25_Reuters" /> [[Invasi Rusia ke Ukraina 2022|Invasi Rusia ke Ukraina tahun 2022]] juga menutup dua perusahaan di Ukraina: LLC «Cryoin engineering» ({{Lang-uk|ТОВ «Кріоін Інжинірінг»}}) dan LLC «Inhaz» ({{Lang-uk|ТОВ «ІНГАЗ»}}), masing-masing berlokasi di [[Odesa]] dan [[Mariupol]]; yang menghasilkan sekitar setengah dari pasokan global.<ref name="arstechnica">{{cite news |last1=Times |first1=Financial |title=Low on gas: Ukraine invasion chokes supply of neon needed for chipmaking |url=https://arstechnica.com/gadgets/2022/03/low-on-gas-ukraine-invasion-chokes-supply-of-neon-needed-for-chipmaking/ |access-date=25 Maret 2023 |work=Ars Technica |date=4 Maret 2022 |language=en-us}}</ref> Penutupan ini diperkirakan akan memperburuk [[Kelangkaan sirkuit terpadu global 2020|kelangkaan cip COVID-19]],<ref name="Newshour" /><ref name="2022-02-25_Reuters">[https://www.reuters.com/breakingviews/ukraine-war-flashes-neon-warning-lights-chips-2022-02-24/ Ukraine war flashes neon warning lights for chips], [[Reuters]], 25 Februari 2022</ref> yang selanjutnya dapat mengalihkan produksi neon ke Tiongkok.<ref name="cnbc" /> |
|||
==Aplikasi== |
|||
[[Berkas:Neon sign, "CHANGE".jpg|thumb|Sebuah contoh tanda neon|300x300px]] |
|||
Neon sering digunakan dalam [[tanda neon|tanda]] dan menghasilkan cahaya oranye kemerahan yang jelas. Meskipun lampu tabung dengan warna lain sering disebut "neon", mereka menggunakan [[gas mulia]] yang berbeda atau warna lampu [[lampu pendar|fluoresen]] yang bervariasi. |
|||
Neon digunakan dalam [[tabung elektron|tabung vakum]], indikator tegangan tinggi, [[penangkap petir]], tabung [[Pengukur gelombang serapan|pengukur gelombang]], tabung [[televisi]], dan [[laser helium–neon]]. Neon cair secara komersial digunakan sebagai [[refrigeran|pendingin]] [[kriogenik]] dalam aplikasi yang tidak memerlukan rentang suhu lebih rendah yang dapat dicapai dengan pendinginan helium cair yang lebih ekstrem. |
|||
Neon, sebagai cairan atau gas, relatif mahal – untuk jumlah kecil, harga neon cair bisa lebih dari 55 kali lipat dari helium cair. Penyebab mahalnya neon adalah kelangkaannya, yang, tidak seperti helium, hanya dapat diperoleh dalam jumlah yang dapat digunakan dengan menyaringnya dari atmosfer. |
|||
===Industri semikonduktor=== |
|||
{{Hingga|2022}}, campuran gas yang mencakup neon digunakan untuk menggerakkan laser untuk [[litografi ultraungu ekstrem|litografi EUV]].<ref name="arstechnica" /> |
|||
Laser dalam kelas ini dikenal karena pancaran denyutnya yang berintensitas tinggi dalam ultraviolet nanodetik dengan kedalaman panjang gelombang 193 nm, dan ukuran titiknya yang sangat kecil yang dibatasi oleh difraksi, yang sangat penting untuk fotolitografi modern dengan resolusi spasial 7 nm.<ref>{{cite web|title=Understanding the science behind the neon shortage|url=https://www.advancedsciencenews.com/understanding-the-science-behind-the-neon-shortage/|accessdate=2023-10-25|work=www.advancedsciencenews.com}}</ref><ref>{{cite web|title=Laser Classification Explanation|url=https://ehs.lbl.gov/resource/documents/radiation-protection/laser-safety/laser-classification-explanation/|accessdate=2023-10-25|work=ehs.lbl.gov}}</ref><ref>{{cite web|title=Laser|url=https://www.physics-and-radio-electronics.com/physics/laser/applicationsoflasers.html|accessdate=2023-10-25|work=www.physics-and-radio-electronics.com}}</ref> Mereka terutama digunakan dalam pembuatan chip komputer dalam proses etsa sirkuit pada kristal<ref>{{cite web|title=Everything You Need to Know About the Semiconductor Neon Shortage|url=https://partstack.com/blog/everything-you-need-to-know-about-the-semiconductor-neon-shortage/|accessdate=2023-10-25|work=partstack.com}}</ref>, tetapi memiliki banyak aplikasi lain, termasuk senjata laser, fusi nuklir, pemrosesan submikron, pemisahan isotop, dan operasi mata.<ref>{{cite web|title=EUV Lithography: State-of-the-Art Review|url=https://www.researchgate.net/publication/334136595_EUV_Lithography_State-of-the-Art_Review|accessdate=2023-10-25|work=www.researchgate.net}}</ref><ref>{{cite web|title=EUV lithography systems|url=https://www.asml.com/en/products/euv-lithography-systems|accessdate=2023-10-25|work=www.asml.com}}</ref> |
|||
Untuk mencapai daya emisi berdenyut tinggi, konsistensi dan keandalan laser excimer argon-fluoride-neon yang diperlukan untuk jenis fotolitografi ini, neon, yang terdiri atas 95% campuran gas argon dan fluor, harus sangat murni (99,999%) supaya tidak menurunkan performa laser. |
|||
==Lihat pula== |
|||
* [[Rasio ekspansi]] |
|||
* [[Tanda neon]] |
|||
* [[Lampu neon]] |
|||
{{Subject bar |
|||
|portal=Kimia |
|||
|commons=y |
|||
|wikt=y |
|||
|wikt-search=neon |
|||
|v=y |
|||
|v-search=Atom neon |
|||
|b=y |
|||
|b-search=Wikijunior:The Elements/Neon |
|||
}} |
|||
==Referensi== |
|||
{{Reflist|30em}} |
|||
==Pranala luar== |
|||
* {{en}} [http://www.periodicvideos.com/videos/010.htm Neon] di ''[[The Periodic Table of Videos]]'' (Universitas Nottingham) |
|||
* {{en}} [http://www.webelements.com/neon/ WebElements.com – Neon]. |
|||
* {{en}} [http://education.jlab.org/itselemental/ele010.html It's Elemental – Neon] |
|||
* {{en}} [http://wwwrcamnl.wr.usgs.gov/isoig/period/ne_iig.html USGS Periodic Table – Neon] |
|||
* {{en}} [http://hyperphysics.phy-astr.gsu.edu/Hbase/quantum/atspect2.html Atomic Spectrum of Neon] |
|||
* {{en}} [http://www.neonmuseum.org/ Neon Museum, Las Vegas] |
|||
{{Tabel periodik unsur kimia}} |
|||
{{Authority control}} |
|||
[[Kategori:Neon| ]] |
|||
[[Kategori:Unsur kimia]] |
|||
[[Kategori:Gas mulia]] |
|||
[[Kategori:Pendingin]] |
|||
[[Kategori:Refrigeran]] |
|||
[[Kategori:Media penguat laser]] |
|||
[[Kategori:Gas industri]] |
|||
[[Kategori:Tabel periodik]] |
|||
Revisi terkini sejak 15 Juni 2024 16.55
10Ne Neon | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Gas neon dalam tabung lucutan, yang disebut lampu neon. | |||||||||||||||||||||
Garis spektrum neon | |||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||
| Pengucapan | /nèon/[1] | ||||||||||||||||||||
| Penampilan | gas tak berwarna, akan menjadi merah-jingga jika diletakkan pada medan listrik bertegangan tinggi | ||||||||||||||||||||
| Neon dalam tabel periodik | |||||||||||||||||||||
| |||||||||||||||||||||
| Nomor atom (Z) | 10 | ||||||||||||||||||||
| Golongan | golongan 18 (gas mulia) | ||||||||||||||||||||
| Periode | periode 2 | ||||||||||||||||||||
| Blok | blok-p | ||||||||||||||||||||
| Kategori unsur | gas mulia | ||||||||||||||||||||
| Berat atom standar (Ar) |
| ||||||||||||||||||||
| Konfigurasi elektron | 1s2 2s2 2p6 | ||||||||||||||||||||
| Elektron per kelopak | 2, 8 | ||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | gas | ||||||||||||||||||||
| Titik lebur | 24,56 K (−248,59 °C, −415,46 °F) | ||||||||||||||||||||
| Titik didih | 27,104 K (−246,046 °C, −410,883 °F) | ||||||||||||||||||||
| Kerapatan (pada STS) | 0,9002 g/L | ||||||||||||||||||||
| saat cair, pada t.d. | 1,207 g/cm3[2] | ||||||||||||||||||||
| Titik tripel | 24,556 K, 43 kPa[3][4] | ||||||||||||||||||||
| Titik kritis | 44,4918 K, 2,7686 MPa[5] | ||||||||||||||||||||
| Kalor peleburan | 0,335 kJ/mol | ||||||||||||||||||||
| Kalor penguapan | 1,71 kJ/mol | ||||||||||||||||||||
| Kapasitas kalor molar | 5R/2 = 20,79[6] J/(mol·K) | ||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||
| Bilangan oksidasi | 0 | ||||||||||||||||||||
| Energi ionisasi | ke-1: 2080,7 kJ/mol ke-2: 3952,3 kJ/mol ke-3: 6122 kJ/mol (artikel) | ||||||||||||||||||||
| Jari-jari kovalen | 58 pm | ||||||||||||||||||||
| Jari-jari van der Waals | 154 pm | ||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||
| Kelimpahan alami | primordial | ||||||||||||||||||||
| Struktur kristal | kubus berpusat muka (fcc) | ||||||||||||||||||||
| Kecepatan suara | 435 m/s (gas, pada 0 °C) | ||||||||||||||||||||
| Konduktivitas termal | 49,1×10−3 W/(m·K) | ||||||||||||||||||||
| Arah magnet | diamagnetik[7] | ||||||||||||||||||||
| Suseptibilitas magnetik molar | −6,74×10−6 cm3/mol (298 K)[8] | ||||||||||||||||||||
| Modulus curah | 654 GPa | ||||||||||||||||||||
| Nomor CAS | 7440-01-9 | ||||||||||||||||||||
| Sejarah | |||||||||||||||||||||
| Prediksi | W. Ramsay (1897) | ||||||||||||||||||||
| Penemuan | W. Ramsay dan M. Travers[9] (1898) | ||||||||||||||||||||
| Isolasi pertama | W. Ramsay dan M. Travers[10] | ||||||||||||||||||||
| Penemuan lampu neon | Georges Claude (1910) | ||||||||||||||||||||
| Isotop neon yang utama | |||||||||||||||||||||
| |||||||||||||||||||||
Neon adalah unsur kimia dengan lambang Ne dan nomor atom 10. Neon termasuk dalam golongan gas mulia.[11] Neon adalah gas monoatomik lengai yang nirwarna dan nirbau pada kondisi standar, dengan massa jenis sekitar dua pertiga udara. Ia ditemukan (bersama dengan kripton dan xenon) pada tahun 1898 sebagai salah satu dari tiga unsur lengai sisa yang tersisa di udara kering, setelah nitrogen, oksigen, argon, dan karbon dioksida dihilangkan. Neon adalah yang kedua dari tiga gas langka ini yang ditemukan dan segera dikenali sebagai unsur baru dari spektrum emisi merah terangnya. Nama neon berasal dari kata Yunani, νέον, bentuk tunggal netral dari νέος (neos), yang berarti 'baru'. Neon bersifat lengai secara kimiawi, dan tidak ada senyawa neon yang tak bermuatan yang diketahui. Senyawa neon yang saat ini dikenal meliputi molekul ionik, molekul yang disatukan oleh gaya van der Waals dan klatrat.
Selama nukleogenesis kosmik unsur-unsur, sejumlah besar neon dibangun dari proses fusi penangkapan alfa di dalam bintang. Meskipun neon adalah unsur yang sangat umum di alam semesta dan tata surya (berada kelima dalam kelimpahan kosmik setelah hidrogen, helium, oksigen, dan karbon), neon jarang ditemukan di Bumi. Ia menyusun sekitar 18,2 ppm udara berdasarkan volume (ini hampir sama dengan fraksi molekul atau mol) dan fraksi yang lebih kecil di kerak bumi. Alasan kelangkaan relatif neon di Bumi dan planet bagian dalam (terestrial) adalah karena neon sangat volatil dan tidak membentuk senyawa untuk memperbaikinya menjadi padat. Akibatnya, ia lepas dari planetisimal di bawah kehangatan Matahari yang baru tersulut di Tata Surya awal. Bahkan atmosfer luar Jupiter agak kehabisan neon, meski untuk alasan yang berbeda.[12]
Neon memberikan pancaran oranye kemerahan yang berbeda saat digunakan pada lampu pijar neon bertegangan rendah, tabung lucutan, dan tanda iklan neon.[13][14] Garis emisi merah dari neon juga menyebabkan lampu merah dari laser helium–neon. Neon digunakan dalam beberapa tabung plasma dan aplikasi pendingin tetapi memiliki beberapa kegunaan komersial lainnya. Ia diekstraksi secara komersial dengan distilasi fraksional dari udara cair. Karena udara adalah satu-satunya sumber, ia jauh lebih mahal daripada helium.
Sejarah
[sunting | sunting sumber]
Neon ditemukan pada tahun 1898 oleh kimiawan Inggris Sir William Ramsay (1852–1916) dan Morris Travers (1872–1961) di London.[15] Neon ditemukan ketika Ramsay mendinginkan sampel udara hingga menjadi cairan, kemudian menghangatkan cairan tersebut dan menangkap gas saat mendidih. Gas nitrogen, oksigen, dan argon telah diidentifikasi, tetapi gas yang tersisa diisolasi menurut urutan kelimpahannya, dalam periode enam minggu yang dimulai pada akhir Mei 1898. Yang pertama diidentifikasi adalah kripton. Berikutnya, setelah kripton dihilangkan, adalah gas yang memberikan cahaya merah cemerlang di bawah lucutan spektroskopi. Gas ini, diidentifikasi pada bulan Juni, diberi nama "neon", analog bahasa Yunani dari bahasa Latin novum ('baru')[16] yang disarankan oleh putra Ramsay. Karakteristik warna merah-oranye cemerlang yang dipancarkan oleh gas neon saat dieksitasi secara elektrik segera dicatat. Travers kemudian menulis: "kobaran cahaya merah dari tabung menceritakan kisahnya sendiri dan merupakan pemandangan yang harus diingat dan tidak pernah dilupakan."[17]
Gas kedua juga dilaporkan bersama dengan neon, memiliki massa jenis yang kira-kira sama dengan argon tetapi dengan spektrum yang berbeda – Ramsay dan Travers menamainya metargon.[18][19] Namun, analisis spektroskopi selanjutnya mengungkapkan bahwa itu adalah argon yang terkontaminasi karbon monoksida. Akhirnya, tim yang sama menemukan xenon dengan proses yang sama, pada bulan September 1898.[18]
Kelangkaan neon menghalangi aplikasi cepatnya untuk penerangan di sepanjang garis tabung Moore, yang menggunakan nitrogen dan dikomersialkan pada awal 1900-an. Setelah 1902, perusahaan Air Liquide milik Georges Claude memproduksi neon dalam jumlah industri sebagai produk sampingan dari bisnis pencairan udaranya. Pada bulan Desember 1910, Claude mendemonstrasikan pencahayaan neon berdasarkan tabung neon yang disegel. Claude mencoba untuk menjual tabung neon untuk penerangan rumah dalam ruangan, karena intensitasnya, tetapi pasarnya gagal karena pemilik rumah keberatan dengan warnanya. Pada tahun 1912, rekanan Claude mulai menjual tabung neon sebagai tanda iklan yang menarik perhatian dan langsung menjadi lebih sukses. Tabung neon diperkenalkan ke AS pada tahun 1923 dengan dua lampu neon besar yang dibeli oleh pedagang mobil Los Angeles Packard. Cahaya dan warna merah yang menawan membuat iklan neon benar-benar berbeda dari kompetisi.[20] Warna intens dan semangat neon disamakan dengan masyarakat Amerika pada saat itu, menunjukkan "abad kemajuan" dan mengubah kota menjadi lingkungan baru yang sensasional yang dipenuhi dengan iklan yang memancar dan "arsitektur elektro-grafis".[21][22]
Neon berperan dalam pemahaman dasar tentang sifat atom pada tahun 1913, ketika J. J. Thomson, sebagai bagian dari penjelajahannya ke dalam komposisi sinar kanal, menyalurkan aliran ion neon melalui medan magnet dan listrik dan mengukur defleksi dari aliran dengan pelat fotografi. Thomson mengamati dua petak cahaya terpisah pada pelat fotografi (lihat gambar), yang memperkirakan dua defleksi parabola yang berbeda. Thomson akhirnya menyimpulkan bahwa beberapa atom dalam gas neon memiliki massa yang lebih tinggi daripada yang lain. Meskipun pada saat itu tidak dipahami oleh Thomson, ini adalah penemuan pertama dari isotop atom stabil. Perangkat Thomson adalah versi mentah dari instrumen yang sekarang kita sebut sebagai spektrometer massa.
Isotop
[sunting | sunting sumber]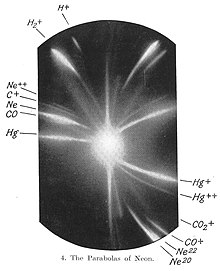
Neon memiliki tiga isotop stabil: 20Ne (90,48%), 21Ne (0,27%) dan 22Ne (9,25%).[23]
21Ne dan 22Ne bersifat sebagian primordial dan sebagian nukleogenik (yaitu dibuat oleh reaksi nuklir nuklida lain dengan neutron atau partikel lain di lingkungan) dan variasinya dalam kelimpahan alami telah dipahami dengan baik. Sebaliknya, 20Ne (isotop primordial utama yang dibuat dalam nukleosintesis bintang) tidak diketahui bersifat nukleogenik atau radiogenik, kecuali dari peluruhan oksigen-20, yang dihasilkan dalam kasus peluruhan gugus yang sangat jarang oleh torium-228. Dengan demikian, penyebab variasi 20Ne di Bumi telah diperdebatkan dengan hangat.[24][25]
Reaksi nuklir utama yang menghasilkan isotop neon nukleogenik dimulai dari 24Mg dan 25Mg, yang masing-masing menghasilkan 21Ne dan 22Ne, setelah penangkapan neutron dan emisi langsung partikel alfa. Neutron yang menghasilkan reaksi sebagian besar dihasilkan oleh reaksi spalasi sekunder dari partikel alfa, yang pada gilirannya berasal dari rantai peluruhan deret uranium. Hasil bersih menghasilkan kecenderungan rasio 20Ne/22Ne yang lebih rendah dan 21Ne/22Ne yang lebih tinggi yang teramati pada batuan kaya uranium seperti granit.[25]
Selain itu, analisis isotop batuan terestrial telah menunjukkan produksi kosmogenik (sinar kosmik) 21Ne. Isotop ini dihasilkan melalui reaksi spalasi pada magnesium, natrium, silikon, dan aluminium. Dengan menganalisis ketiga isotop tersebut, komponen kosmogenik dapat diselesaikan dari neon magmatik dan neon nukleogenik. Hal ini menunjukkan bahwa neon akan menjadi alat yang berguna dalam menentukan usia paparan kosmik dari batuan permukaan dan meteorit.[26]
Neon dalam angin matahari mengandung proporsi 20Ne yang lebih tinggi daripada sumber nukleogenik dan kosmogenik.[25] Kandungan neon yang teramati dalam sampel gas vulkanik dan intan juga diperkaya dengan 20Ne, yang menunjukkan kemungkinan berasal dari matahari purba.[27]
Karateristik
[sunting | sunting sumber]Neon adalah gas mulia paling ringan kedua setelah helium. Ia bersinar dengan warna oranye kemerahan dalam tabung lucutan vakum. Ia memiliki lebih dari 40 kali lipat kapasitas pendinginan (per satuan volume) dari helium cair dan tiga kali lipat dari hidrogen cair.[2] Dalam sebagian besar aplikasi, ia adalah pendingin yang lebih murah daripada helium.[28][29]

Plasma neon memiliki pelepasan cahaya paling intens pada tegangan dan arus normal dari semua gas mulia. Warna rata-rata cahaya ini bagi mata manusia adalah merah-oranye karena banyaknya garis dalam kisaran ini; ia juga mengandung garis hijau yang kuat, yang tersembunyi, kecuali komponen visualnya didispersi oleh spektroskop.[30]
Dua jenis pencahayaan neon yang sangat berbeda digunakan secara umum. Lampu neon umumnya kecil, dengan sebagian besar beroperasi antara 100 dan 250 volt.[31] Mereka telah banyak digunakan sebagai indikator daya dan peralatan pengujian sirkuit, tetapi dioda pemancar cahaya (LED) sekarang mendominasi dalam aplikasi tersebut. Perangkat neon sederhana ini adalah pelopor layar plasma dan layar televisi plasma.[32][33] Tanda neon biasanya beroperasi pada voltase yang jauh lebih tinggi (2–15 kilovolt), dan tabung bercahaya biasanya memiliki panjang beberapa meter.[34] Tabung kaca sering dibentuk menjadi bentuk dan huruf untuk papan nama, serta aplikasi arsitektur dan artistik.
Keterjadian
[sunting | sunting sumber]Isotop stabil neon diproduksi di dalam bintang. Isotop neon yang paling melimpah 20Ne (90,48%) diciptakan oleh fusi nuklir karbon dan karbon dalam proses pembakaran karbon nukleosintesis bintang. Proses ini membutuhkan suhu di atas 500 megakelvin, yang terjadi pada inti bintang dengan massa lebih dari 8 matahari.[35][36]
Neon berlimpah dalam skala universal; ia adalah unsur kimia paling melimpah kelima di alam semesta berdasarkan massa, setelah hidrogen, helium, oksigen, dan karbon (lihat unsur kimia).[37] Kelangkaannya yang relatif di Bumi, seperti helium, adalah karena sifatnya yang relatif ringan, tekanan uapnya yang tinggi pada suhu yang sangat rendah, dan kelengaian kimiawinya, semua sifat yang cenderung mencegahnya terperangkap dalam gas kondensasi dan awan debu yang membentuk planet padat yang lebih kecil dan lebih hangat seperti Bumi. Neon bersifat monoatomik, membuatnya lebih ringan daripada molekul nitrogen dan oksigen diatomik yang membentuk sebagian besar atmosfer bumi; balon berisi neon akan naik di udara, meski lebih lambat dari balon helium.[38]
Kelimpahan neon di alam semesta adalah sekitar 1 bagian dalam 750; di Matahari dan mungkin di nebula sistem proto-surya, sekitar 1 bagian dalam 600. Prob atmosfer wahana antariksa Galileo menemukan bahwa bahkan pada atmosfer Jupiter bagian atas, kelimpahan neon berkurang (habis) sekitar faktor 10, ke tingkat 1 bagian dalam 6.000 berdasarkan massa. Hal ini mungkin menunjukkan bahwa planetisimal-es, yang membawa neon ke Jupiter dari luar tata surya, terbentuk di wilayah yang terlalu hangat untuk mempertahankan komponen atmosfer neon (kelimpahan gas lengai yang lebih berat di Jupiter beberapa kali lebih banyak daripada yang ditemukan di Bumi).[39]
Neon terdiri dari 1 bagian dalam 55.000 di atmosfer Bumi, atau 18,2 ppm berdasarkan volume (ini hampir sama dengan fraksi mol atau molekul), atau 1 bagian dalam 79.000 udara berdasarkan massa. Ia terdiri dari fraksi yang lebih kecil di kerak Bumi. Ia diproduksi secara industri dengan distilasi fraksionalkriogenik dari udara yang telah dicairkan.[2]
Pada 17 Agustus 2015, berdasarkan studi dengan wahana antariksa Lunar Atmosphere and Dust Environment Explorer (LADEE), ilmuwan NASA melaporkan deteksi neon pada eksosfer Bulan.[40]
Kimia
[sunting | sunting sumber]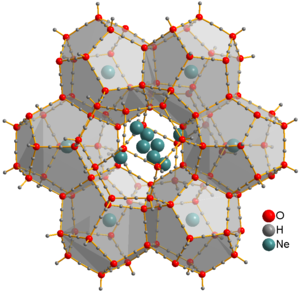
Neon adalah gas mulia blok-p pertama, dan unsur pertama dengan oktet elektron yang sebenarnya. Ia bersifat lengai: seperti analognya yang lebih ringan, helium, tidak ada molekul netral yang terikat kuat yang mengandung neon yang telah diidentifikasi. Ion [NeAr]+, [NeH]+, dan [HeNe]+ telah diamati dari studi optik dan spektrometri massa.[2] Klatrat hidrat neon padat diproduksi dari es air dan gas neon pada tekanan 350–480 MPa dan suhu sekitar −30 °C.[42] Atom Ne tidak terikat pada air dan dapat bergerak bebas melalui bahan ini. Mereka dapat diekstraksi dengan menempatkan klatrat ke dalam ruang vakum selama beberapa hari, menghasilkan es XVI, bentuk kristal air yang paling tidak padat.[41]
Skala keelektronegatifan Pauling bergantung pada energi ikatan kimia, tetapi nilai tersebut jelas belum diukur untuk helium dan neon yang lengai. Skala keelektronegatifan Allen, yang hanya bergantung pada energi atom (terukur), mengidentifikasi neon sebagai unsur yang paling elektronegatif, diikuti oleh fluorin dan helium.[43]
Suhu titik tripel neon (24,5561 K) adalah titik tetap yang ditentukan dalam Skala Suhu Internasional 1990.[44]
Produksi
[sunting | sunting sumber]Neon dihasilkan dari udara di pabrik pemisahan udara kriogenik. Campuran fase gas yang terutama terdiri dari nitrogen, neon, dan helium ditarik dari kondensor utama di bagian atas kolom pemisah udara bertekanan tinggi dan diumpankan ke bagian bawah kolom samping untuk distilasi neon.[45] Ia kemudian dapat dimurnikan lebih lanjut dari helium.
Sekitar 70% pasokan neon global diproduksi di Ukraina[46] sebagai produk sampingan dari produksi baja di Rusia.[47] Hingga 2020[update], perusahaan Iceblick, dengan pabrik di Odesa dan Moskow, memasok 65% produksi neon dunia, serta 15% kripton dan xenon.[48][49]
Kelangkaan 2022
[sunting | sunting sumber]Harga neon global melonjak sekitar 600% setelah pencaplokan Krimea oleh Rusia pada tahun 2014,[50] mendorong beberapa produsen cip untuk mulai beralih dari pemasok Rusia dan Ukraina[51] ke pemasok di Tiongkok.[49] Invasi Rusia ke Ukraina tahun 2022 juga menutup dua perusahaan di Ukraina: LLC «Cryoin engineering» (bahasa Ukraina: ТОВ «Кріоін Інжинірінг») dan LLC «Inhaz» (bahasa Ukraina: ТОВ «ІНГАЗ»), masing-masing berlokasi di Odesa dan Mariupol; yang menghasilkan sekitar setengah dari pasokan global.[50] Penutupan ini diperkirakan akan memperburuk kelangkaan cip COVID-19,[48][49] yang selanjutnya dapat mengalihkan produksi neon ke Tiongkok.[51]
Aplikasi
[sunting | sunting sumber]
Neon sering digunakan dalam tanda dan menghasilkan cahaya oranye kemerahan yang jelas. Meskipun lampu tabung dengan warna lain sering disebut "neon", mereka menggunakan gas mulia yang berbeda atau warna lampu fluoresen yang bervariasi.
Neon digunakan dalam tabung vakum, indikator tegangan tinggi, penangkap petir, tabung pengukur gelombang, tabung televisi, dan laser helium–neon. Neon cair secara komersial digunakan sebagai pendingin kriogenik dalam aplikasi yang tidak memerlukan rentang suhu lebih rendah yang dapat dicapai dengan pendinginan helium cair yang lebih ekstrem.
Neon, sebagai cairan atau gas, relatif mahal – untuk jumlah kecil, harga neon cair bisa lebih dari 55 kali lipat dari helium cair. Penyebab mahalnya neon adalah kelangkaannya, yang, tidak seperti helium, hanya dapat diperoleh dalam jumlah yang dapat digunakan dengan menyaringnya dari atmosfer.
Industri semikonduktor
[sunting | sunting sumber]Hingga 2022[update], campuran gas yang mencakup neon digunakan untuk menggerakkan laser untuk litografi EUV.[50] Laser dalam kelas ini dikenal karena pancaran denyutnya yang berintensitas tinggi dalam ultraviolet nanodetik dengan kedalaman panjang gelombang 193 nm, dan ukuran titiknya yang sangat kecil yang dibatasi oleh difraksi, yang sangat penting untuk fotolitografi modern dengan resolusi spasial 7 nm.[52][53][54] Mereka terutama digunakan dalam pembuatan chip komputer dalam proses etsa sirkuit pada kristal[55], tetapi memiliki banyak aplikasi lain, termasuk senjata laser, fusi nuklir, pemrosesan submikron, pemisahan isotop, dan operasi mata.[56][57]
Untuk mencapai daya emisi berdenyut tinggi, konsistensi dan keandalan laser excimer argon-fluoride-neon yang diperlukan untuk jenis fotolitografi ini, neon, yang terdiri atas 95% campuran gas argon dan fluor, harus sangat murni (99,999%) supaya tidak menurunkan performa laser.
Lihat pula
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ (Indonesia) "Neon". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ a b c d Hammond, C.R. (2000). The Elements, in Handbook of Chemistry and Physics 81st edition (PDF). CRC press. hlm. 19. ISBN 0849304814.
- ^ Preston-Thomas, H. (1990). "The International Temperature Scale of 1990 (ITS-90)". Metrologia. 27: 3–10. Bibcode:1990Metro..27....3P. doi:10.1088/0026-1394/27/1/002.
- ^ "Section 4, Properties of the Elements and Inorganic Compounds; Melting, boiling, triple, and critical temperatures of the elements". CRC Handbook of Chemistry and Physics (edisi ke-85th edition). Boca Raton, Florida: CRC Press. 2005.
- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamab92 - ^ Shuen-Chen Hwang, Robert D. Lein, Daniel A. Morgan (2005). "Noble Gases". in Kirk Othmer Encyclopedia of Chemical Technology, pages 343–383. Wiley. DOI:10.1002/0471238961.0701190508230114.a01.pub2
- ^ Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. hlm. E110. ISBN 0-8493-0464-4.
- ^ Ramsay, William, Travers, Morris W. (1898). "On the Companions of Argon". Proceedings of the Royal Society of London. 63 (1): 437–440. doi:10.1098/rspl.1898.0057.
- ^ "Neon: History". Softciências. Diakses tanggal 18 Juli 2022.
- ^ Golongan 18 mengacu pada penomoran modern dari tabel periodik. Penomoran yang lebih lama menggambarkan gas mulia sebagai Golongan 0 atau Golongan VIIIA (terkadang disingkat menjadi 8). Lihat pula Golongan tabel periodik.
- ^ Wilson, Hugh F.; Militzer, Burkhard (March 2010), "Sequestration of Noble Gases in Giant Planet Interiors", Physical Review Letters, 104 (12): 121101, arXiv:1003.5940
 , Bibcode:2010PhRvL.104l1101W, doi:10.1103/PhysRevLett.104.121101, PMID 20366523, 121101.
, Bibcode:2010PhRvL.104l1101W, doi:10.1103/PhysRevLett.104.121101, PMID 20366523, 121101.
- ^ Coyle, Harold P. (2001). Project STAR: The Universe in Your Hands. Kendall Hunt. hlm. 464. ISBN 978-0-7872-6763-6.
- ^ Kohmoto, Kohtaro (1999). "Phosphors for lamps". Dalam Shionoya, Shigeo; Yen, William M. Phosphor Handbook. CRC Press. hlm. 940. ISBN 978-0-8493-7560-6.
- ^ Ramsay, William, Travers, Morris W. (1898). "On the Companions of Argon". Proceedings of the Royal Society of London. 63 (1): 437–440. doi:10.1098/rspl.1898.0057.
- ^ "Neon: History". Softciências. Diarsipkan dari versi asli tanggal 14 Maret 2007. Diakses tanggal 25 Maret 2023.
- ^ Weeks, Mary Elvira (2003). Discovery of the Elements: Third Edition (reprint). Kessinger Publishing. hlm. 287. ISBN 978-0-7661-3872-8. Diarsipkan dari versi asli tanggal 22 Maret 2015.
- ^ a b Ramsay, Sir William (12 Desember 1904). "Nobel Lecture – The Rare Gases of the Atmosphere". nobelprize.org. Nobel Media AB. Diarsipkan dari versi asli tanggal 13 November 2015. Diakses tanggal 25 Maret 2023.
- ^ Ramsay, William; Travers, Morris W. (1898). "On the Companions of Argon". Proceedings of the Royal Society of London. 63 (1): 437–440. doi:10.1098/rspl.1898.0057. ISSN 0370-1662.
- ^ Mangum, Aja (8 Desember 2007). "Neon: A Brief History". New York Magazine. Diarsipkan dari versi asli tanggal 15 April 2008. Diakses tanggal 25 Maret 2023.
- ^ Golec, Michael J. (2010). "Logo/Local Intensities: Lacan, the Discourse of the Other, and the Solicitation to "Enjoy"". Design and Culture. 2 (2): 167–181. doi:10.2752/175470710X12696138525622.
- ^ Wolfe, Tom (Oktober 1968). "Electro-Graphic Architecture". Architecture Canada.
- ^ Kondev, F.G.; Wang, M.; Huang, W.J.; Naimi, S.; Audi, G. (2021). "The NUBASE2020 evaluation of nuclear properties" (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ^ Dickin, Alan P (2005). "Neon". Radiogenic isotope geology. hlm. 303. ISBN 978-0-521-82316-6.[pranala nonaktif permanen]
- ^ a b c Resources on Isotopes Periodic Table--Neon di U.S. Geological Survey, oleh Eric Caldwell, dikirim pada Januari 2004, diakses tanggal 25 Maret 2023
- ^ "Neon: Isotopes". Softciências. Diarsipkan dari versi asli tanggal 15 November 2011. Diakses tanggal 25 Maret 2023.
- ^ Anderson, Don L. "Helium, Neon & Argon". Mantleplumes.org. Diarsipkan dari versi asli tanggal 28 Mei 2006. Diakses tanggal 25 Maret 2023.
- ^ "NASSMC: News Bulletin". 30 Desember 2005. Diarsipkan dari versi asli tanggal 13 Februari 2007. Diakses tanggal 25 Maret 2023.
- ^ Mukhopadhyay, Mamata (2012). Fundamentals of Cryogenic Engineering. hlm. 195. ISBN 9788120330573. Diarsipkan dari versi asli tanggal 16 November 2017.
- ^ "Plasma". Diarsipkan dari versi asli tanggal 7 Maret 2007. Diakses tanggal 25 Maret 2023.
- ^ Baumann, Edward (1966). Applications of Neon Lamps and Gas Discharge Tubes. Carlton Press.
- ^ Myers, Robert L. (2002). Display interfaces: fundamentals and standards. John Wiley and Sons. hlm. 69–71. ISBN 978-0-471-49946-6. Diarsipkan dari versi asli tanggal 29 Juni 2016.
Tampilan plasma terkait erat dengan lampu neon sederhana.
- ^ Weber, Larry F. (April 2006). "History of the plasma display panel". IEEE Transactions on Plasma Science. 34 (2): 268–278. Bibcode:2006ITPS...34..268W. doi:10.1109/TPS.2006.872440. Akses berbayar.
- ^ "ANSI Luminous Tube Footage Chart" (PDF). Institut Standar Nasional Amerika (ANSI). Diarsipkan dari versi asli (PDF) tanggal 26 Februari 2011. Diakses tanggal 25 Maret 2023. Reproduksi bagan dalam katalog perusahaan penerangan di Toronto; spesifikasi ANSI asli tidak diberikan.
- ^ Clayton, Donald (2003). Handbook of Isotopes in the Cosmos: Hydrogen to Gallium. Cambridge University Press. hlm. 106–107. ISBN 978-0521823814.
- ^ Ryan, Sean G.; Norton, Andrew J. (2010). Stellar Evolution and Nucleosynthesis. Cambridge University Press. hlm. 135. ISBN 978-0-521-13320-3.
- ^ Asplund, Martin; Grevesse, Nicolas; Sauval, A. Jacques; Scott, Pat (2009). "The Chemical Composition of the Sun". Annual Review of Astronomy and Astrophysics. 47 (1): 481–522. arXiv:0909.0948
 . Bibcode:2009ARA&A..47..481A. doi:10.1146/annurev.astro.46.060407.145222.
. Bibcode:2009ARA&A..47..481A. doi:10.1146/annurev.astro.46.060407.145222.
- ^ Gallagher, R.; Ingram, P. (19 Juli 2001). Chemistry for Higher Tier. University Press. hlm. 282. ISBN 978-0-19-914817-2.
- ^ Morse, David (26 Januari 1996). "Galileo Probe Science Result". Galileo Project. Diarsipkan dari versi asli tanggal 24 Februari 2007. Diakses tanggal 25 Maret 2023.
- ^ Steigerwald, William (17 Agustus 2015). "NASA's LADEE Spacecraft Finds Neon in Lunar Atmosphere". NASA. Diarsipkan dari versi asli tanggal 19 Agustus 2015. Diakses tanggal 25 Maret 2023.
- ^ a b Falenty, Andrzej; Hansen, Thomas C.; Kuhs, Werner F. (2014). "Formation and properties of ice XVI obtained by emptying a type sII clathrate hydrate". Nature. 516 (7530): 231–3. Bibcode:2014Natur.516..231F. doi:10.1038/nature14014. PMID 25503235.
- ^ Yu, X.; Zhu, J.; Du, S.; Xu, H.; Vogel, S. C.; Han, J.; Germann, T. C.; Zhang, J.; Jin, C.; Francisco, J. S.; Zhao, Y. (2014). "Crystal structure and encapsulation dynamics of ice II-structured neon hydrate". Proceedings of the National Academy of Sciences of the United States of America. 111 (29): 10456–61. Bibcode:2014PNAS..11110456Y. doi:10.1073/pnas.1410690111
 . PMC 4115495
. PMC 4115495  . PMID 25002464.
. PMID 25002464.
- ^ Allen, Leland C. (1989). "Electronegativity is the average one-electron energy of the valence-shell electrons in ground-state free atoms". Journal of the American Chemical Society. 111 (25): 9003–9014. doi:10.1021/ja00207a003.
- ^ "The Internet resource for the International Temperature Scale of 1990". Diarsipkan dari versi asli tanggal 15 Agustus 2009. Diakses tanggal 25 Maret 2023.
- ^ R. Norris Shreve; Joseph Brink (1977). Chemical Process Industries (edisi ke-4). hlm. 113. ISBN 0-07-057145-7.
- ^ "Explained: Why the Russia-Ukraine crisis may lead to a shortage in semiconductors". MSN (dalam bahasa Inggris). The Indian Express.
- ^ Alper, Alexandra (11 Maret 2022). "Exclusive: Russia's attack on Ukraine halts half of world's neon output for chips". Reuters (dalam bahasa Inggris). Diakses tanggal 25 Maret 2023.
- ^ a b "Rare Gasses Supplier Known for Innovation". The European Times. 2020.
- ^ a b c Ukraine war flashes neon warning lights for chips, Reuters, 25 Februari 2022
- ^ a b c Times, Financial (4 Maret 2022). "Low on gas: Ukraine invasion chokes supply of neon needed for chipmaking". Ars Technica (dalam bahasa Inggris). Diakses tanggal 25 Maret 2023.
- ^ a b "Chipmakers see limited impact for now, as Russia invades Ukraine". CNBC (dalam bahasa Inggris). 24 Februari 2022.
- ^ "Understanding the science behind the neon shortage". www.advancedsciencenews.com. Diakses tanggal 2023-10-25.
- ^ "Laser Classification Explanation". ehs.lbl.gov. Diakses tanggal 2023-10-25.
- ^ "Laser". www.physics-and-radio-electronics.com. Diakses tanggal 2023-10-25.
- ^ "Everything You Need to Know About the Semiconductor Neon Shortage". partstack.com. Diakses tanggal 2023-10-25.
- ^ "EUV Lithography: State-of-the-Art Review". www.researchgate.net. Diakses tanggal 2023-10-25.
- ^ "EUV lithography systems". www.asml.com. Diakses tanggal 2023-10-25.
Pranala luar
[sunting | sunting sumber]- (Inggris) Neon di The Periodic Table of Videos (Universitas Nottingham)
- (Inggris) WebElements.com – Neon.
- (Inggris) It's Elemental – Neon
- (Inggris) USGS Periodic Table – Neon
- (Inggris) Atomic Spectrum of Neon
- (Inggris) Neon Museum, Las Vegas
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


