Amonium dikromat

| |
| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Ammonium dichromate
| |
| Nama lain
Amonium bikromat
Amonium pirokromat | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
| Nomor UN | 1439 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| (NH4)2Cr2O7 | |
| Massa molar | 252.07 g/mol |
| Penampilan | Kristal merah-jingga |
| Densitas | 2.115 g/cm3 |
| Titik lebur | 180 °C terdekomposisi |
| 18.2 g/100ml (0 °C) 35.6 g/100ml (20 °C) 40 g/100ml (25 °C) 156 g/100ml (100 °C) | |
| Kelarutan | tidak larut dalam aseton larut dalam alkohol |
| Bahaya | |
| Bahaya utama | Sangat beracun, karsinogenik, mutagenik |
| Lembar data keselamatan | ICSC 1368 |
| Piktogram GHS |        [1] [1]
|
| H272, H301, H312, H314, H317, H330, H334, H340, H350, H360, H372, H410[1] | |
| P201, P220, P260, P273, P280, P284[1] | |
| 190 °C (374 °F; 463 K) | |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
20-250 mg/kg |
| Senyawa terkait | |
Kation lainnya
|
Kalium dikromat Natrium dikromat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
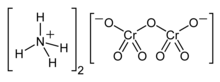
Amonium dikromat adalah senyawa anorganik dengan rumus (NH4)2Cr2O7. Dalam senyawa ini, seperti dalam seluruh kromat dan dikromat, kromium berada pada keadaan oksidasi +6, yang umum dikenal sebagai kromium heksavalen. Senyawa ini adalah suatu garam yang terdiri dari ion amonium dan ion dikromat.
Amonium dikromat kadang dikenal sebagai Api Vesuvius, karena penggunaannya dalam demonstrasi "gunung berapi" di atas meja.[2] Namun, demonstrasi ini tidak lagi populer di kalangan sekolah karena sifatnya yang karsinogenik. Amonium dikromat juga telah digunakan dalam piroteknik dan di awal kemunculan fotografi.
Sifat
[sunting | sunting sumber]Pada suhu dan tekanan ruangan, senyawa ini berwujud kristal asam berwarna jingga yang mudah larut dalam alkohol. Ia terbentuk dari reaksi antara asam kromat dengan amonium hidroksida yang dilanjutkan dengan kristalisasi.[3]
Kristal (NH4)2Cr2O7 (C2/c, z=4) mengandung ion amonium jenis tunggal, pada situs simetri C1(2,3). Masing-masing pusat NH+4 dikelilingi secara tidak tetap oleh delapan atom oksigen dengan jarak N—O berkisar antara 2,83 hingga 3,17Å, sejenis dengan ikatan hidrogen.[4]
Penggunaan
[sunting | sunting sumber]Amonium dikromat telah digunakan dalam piroteknik dan di awal kemunculan fotografi serta dalam litografi, sebagai sumber nitrogen murni di laboratorium, dan sebagai katalis.[5] Senyawa ini juga digunakan sebagai mordan untuk pigmen pewarna, dalam pabrikasi alizarin, krom alum, penyamakan kulit dan pemurnian minyak.[3]
Film fotosensitif mengandung PVA, amonium dikromat, dan fosfor untuk layar televisi dan peranti lainnya. Amonium dikromat bertindak sebagai situs fotoaktif.[6]
Reaksi
[sunting | sunting sumber]Gunung berapi di atas meja dan dekomposisi termal
[sunting | sunting sumber]
Demonstrasi gunung berapi melibatkan penyulutan tumpukan garam, yang menginisiasi konversi eksotermal berikut:[8]
- (NH4)2Cr2O7 (s) → Cr2O3 (s) + N2 (g) + 4 H2O (g) (ΔH = −429.1 ± 3 kcal/mol)
Seperti amonium nitrat, termodinamikanya tidak stabil.[9][10] Reaksi dekomposisinya akan berlangsung setelah dimulai, menghasilkan bubuk berwarna hijau tua yang tebal kromium(III) oksida. Tidak semua amonium dikromat terdekomposisi dalam reaksi ini. Ketika bubuk hijau dicelupkan ke dalam air, larutan kuning/jingga berasal dari amonium dikromat yang tertinggal.
Pengamatan yang diperoleh menggunakan mikroskop dengan pembesaran yang relatif tinggi selama studi kinetik dekomposisi termal amonium dikromat membuktikan, bahwa pemecahan garam berlangsung dengan intervensi zat antara berupa fase cair bukannya fase padat. Karakteristik penghitaman kristal (NH4)2Cr2O7 sebagai konsekuensi dimulainya dekomposisi dapat dijelaskan sebagai kehilangan disosiatif amonia yang menyertai kondensasi progresif anion menjadi Cr3O2−10, Cr4O2−13, dll., yang pada akhirnya menghasilkan CrO3. CrO3 telah diidentifikasi sebagai lelehan zat antara yang memungkinkan pada dekomposisi (NH4)2Cr2O7.[11]
Reaksi oksidasi
[sunting | sunting sumber]Amonium dikromat adalah oksidator kuat dan bereaksi (sering kali dengan hebat) dengan semua reduktor. Semakin kuat reduktornya, semakin hebat reaksinya.[9] Ia juga telah digunakan untuk mempromosi oksidasi alkohol dan tiol. Amonium dikromat, dengan adanya Mg(HSO4)2 dan SiO2 basah dapat bertindak sebagai pereaksi yang sangat efisien untuk penggabungan oksidatif tiol pada kondisi bebas pelarut. Reaksi ini menghasilkan rendemen yang baik pada kondisi ringan.[12] Senyawa ini juga digunakan dalam oksidasi alkohol alifatik menjadi aldehida dan keton terkaitnya, dalam kondisi bebas pelarut dengan adanya ZrCl4/SiO2 basah, dengan rendemen yang relatif tinggi.[13][14]
Keselamatan
[sunting | sunting sumber]Amonium dikromat, seperti seluruh senyawa kromium(VI), sangat beracun dan terbutki karsinogenik.[15] Senyawa ini juga mengiritasi dengan kuat.
Insiden
[sunting | sunting sumber]Dalam wadah tersegel, amonium dikromat dapat meledak jika dipanaskan.[9] Pada 19 Januari 1986, The New York Times melaporkan bahwa dua pekerja tewas dan 14 lainnya luka-luka di Diamond Shamrock Chemicals, Ashtabula, Ohio, ketika 2.000 pon (910 kg) amonium dikromat meledak saat dikeringkan dalam pemanas.[16]
Referensi
[sunting | sunting sumber]- ^ a b c Sigma-Aldrich Co., Ammonium dichromate. Diakses tanggal 2013-07-20.
- ^ "Ammonium Dichromate Volcano". Chemistry Comes Alive!. J. Chem. Educ.
- ^ a b Richard J. Lewis Hawley's Condensed Chemical Dictionary. Wiley & Sons, Inc: New York, 2007 ISBN 978-0-471-76865-4
- ^ Keresztury, G.; Knop, O. (1982). "Infrared spectra of the ammonium ion in crystals. Part XII. Low-temperature transitions in ammonium dichromate, (NH4)2Cr2O7". Can. J. Chem.: 1972–1976.
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ Havard, J. M.; Shim, S. Y.; Fr; eacute; chet, J. M. (1999). "Design of Photoresists with Reduced Environmental Impact. 1. Water-Soluble Resists Based on Photo-Cross-Linking of Poly(vinyl alcohol)". Chem. Mater. 11 (3): 719–725. doi:10.1021/cm980603y.
- ^
Planned and performed by Marina Stojanovska, Miha Bukleski and Vladimir Petruševski, Department of Chemistry, FNSM, Ss. Cyril and Methodius University, Skopje, Macedonia. - ^ Neugebauer, C. A.; Margrave, J. L. (1957). "The Heat Formation of Ammonium Dichromate". J. Phys. Chem. 61 (10): 1429–1430. doi:10.1021/j150556a040.
- ^ a b c Young, A.J. (2005). "CLIP, Chemical Laboratory Information Profile: Ammonium Dichromate". J. Chem. Educ. 82 (11): 1617. doi:10.1021/ed082p1617.
- ^ G. A. P. Dalgaard; A. C. Hazell; R. G. Hazell (1974). "The Crystal Structure of Ammonium Dichromate, (NH4)2Cr2O7". Acta Chemica Scandinavica. A28: 541–545. doi:10.3891/acta.chem.scand.28a-0541.
- ^ Galwey, Andrew K.; Pöppl, Làszlò; Rajam, Sundara (1983). "A Melt Mechanism for the Thermal Decomposition of Ammonium Dichromate". J. Chem. Soc., Faraday Trans. 1. 79 (9): 2143–2151. doi:10.1039/f19837902143.
- ^ Shirini, F.; et al. (2003). "Solvent free oxidation of thiols by (NH4)2Cr2O7 in the presence of Mg(HSO4)2 and wet SiO2". J. Chem. Research (S). 2003: 28–29. doi:10.3184/030823403103172823.
- ^ Shirini, F.; et al. (2001). "ZrCl4/wet SiO2 promoted oxidation of alcohols by (NH4)2Cr2O7 in solution and solvent free condition". J. Chem. Research (S). 2001 (11): 467–477. doi:10.3184/030823401103168541.
- ^ F. Shirini; M. A. Zolfigol; FOO† and M. Khaleghi (2003). "Oxidation of Alcohols Using (NH4)2Cr2O7 in the Presence of Silica Chloride/Wet SiO2 in Solution and under Solvent Free Conditions". Bull. Korean Chem. Soc. 24 (7): 1021–1022. doi:10.5012/bkcs.2003.24.7.1021. Diarsipkan dari versi asli tanggal 2011-07-22. Diakses tanggal 2018-10-02.
- ^ Volkovich, V. A.; Griffiths, T. R. (2000). "Catalytic Oxidation of Ammonia: A Sparkling Experiment". J. Chem. Educ. 77 (2): 177. doi:10.1021/ed077p177.
- ^ Diamond, S. The New York Times, 1986, p. 22.
