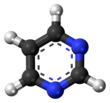
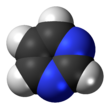
Pirimidina
| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Pyrimidine
| |||
| Nama lain
1,3-Diazine, m-Diazine
| |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
| KEGG | |||
| MeSH | pyrimidine | ||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C4H4N2 | |||
| Massa molar | 80.088 g mol−1 | ||
| Densitas | 1.016 g cm−3 | ||
| Titik lebur | 20 °C (68 °F; 293 K) | ||
| Titik didih | 123 °C (253 °F; 396 K) | ||
| Keasaman (pKa) | 1.10[1] (protonated pyrimidine) | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Pirimidina (bahasa Inggris: Pyrimidine) adalah suatu senyawa organik heterosiklik aromatik yang mirip dengan piridina.[2] Satu dari tiga diazina (senyawa heterosiklik enam karbon dengan dua nitrogen pada cincin), mempunyai nitrogen pada posisi 1 dan 3 dalam cincin.[3] Kedua diazina lain adalah pirazina (nitrogen pada posisi 1 dan 4) dan piridazina ( pada posisi 1 dan 2). Dalam asam nukleat, ketiga tipe nukleobasa merupakan derivat pirimidin yaitu: sitosina (= cytosine) (C), timina (T), dan urasil (U).
Keberadaan dan sejarah

Sistem cincin pirimidina banyak dijumpai dalam alam[4] sebagai senyawa berfusi substitusi dan cincin serta derivatifnya, termasuk nukleotida, tiamina (vitamin B1) dan alloxan. Juga didapati dalam banyak senyawa sintetik seperti barbiturat dan obat HIV, zidovudine. Meskipun derivatif pirimidina seperti asam urat dan alloxan telah dikenal sejak awal abad ke-19, sintesis pirimidina dalam laboratorium baru dilakukan pada tahun 1879,[4] ketika Grimaux melaporkan pembuatan asam barbiturat dari urea Ivy dan asam malonat dengan katalis fosfor oxiklorida.[5] Studi sistematik pirimidina dimulai[6] pada tahun 1884 oleh Pinner,[7] yang melakukan sintesis derivatif melalui kondensasi etil asetoasetat dengan amidina. Pinner pertama kali mengusulkan nama “pyrimidin” pada tahun 1885.[8] Senyawa induk pertama kali dibuat oleh Gabriel & Colman pada tahun 1900,[9] [10] melalui konversi asam barbiturat menjadi 2,4,6-trikloropirimidina diikuti oleh reduksi menggunakan debu seng dalam air panas.
Nomenklatur
Nomenklatur pirimidina tergolong sederhana. Namun, sebagaimana heterosiklik lainnya, gugus hidroksil tautomerik menghasilkan komplikasi karena mereka adanya terutama dalam bentuk amida siklik. Misalnya, 2-hidroksipirimidina lebih tepat dinamai [struktur] 2-pirimidon. Tersedia daftar sebagian nama-nama trivial dari berbagai pirimidina.[11]
Lihat pula
Referensi
- ^ Brown, H.C., et al., in Baude, E.A. and Nachod, F.C., Determination of Organic Structures by Physical Methods, Academic Press, New York, 1955.
- ^ Gilchrist, Thomas Lonsdale; Gilchrist, T. L. (1997). Heterocyclic chemistry. New York: Longman. ISBN 0-582-27843-0.
- ^ Joule, John A.; Mills, Keith, ed. (2010). Heterocyclic Chemistry (edisi ke-5th). Oxford: Wiley. hlm. 250. ISBN 978-1-405-13300-5.
- ^ a b Lagoja, Irene M. (2007). "Pyrimidine as Constituent of Natural Biologically Active Compounds" (PDF). Chemistry and Biodiversity. 2 (1): 1–50. doi:10.1002/cbdv.200490173. PMID 17191918. Kesalahan pengutipan: Tanda
<ref>tidak sah; nama "Lagoja1" didefinisikan berulang dengan isi berbeda - ^ Grimaux, E. (1879). "Synthèse des dérivés uriques de la série de l'alloxane". Comptes rendus hebdomadaires des séances de l'Académie des Sciences. 88: 85–87.
- ^ Kenner, G.W.; Todd, Sir Alexander (1957). Elderfield, R.C., ed. Heterocyclic Compounds, Volume 6. New York: Wiley. hlm. 235.
- ^ Pinner, A. (1884). "Ueber die Einwirkung von Acetessigëther auf die Amidine". Berichte der Deutschen Chemischen Gesellschaft. A17: 2519–2520.
- ^ Pinner, A. (1885). "Ueber die Einwirkung von Acetessigëther auf die Amidine. Pyrimidine". Berichte der Deutschen Chemischen Gesellschaft. A18: 759–760.
- ^ Gabriel, S. (1900). "Pyrimidin aus Barbitursäure". Berichte der Deutschen Chemischen Gesellschaft. A33: 3666.
- ^ Lythgoe, B.; Rayner, L. S. (1951). "Substitution Reactions of Pyrimidine and its 2- and 4-Phenyl Derivatives". Journal of the Chemical Society: 2323–2329. doi:10.1039/JR9510002323.
- ^ Brown, D. J.; Evans, R.F.; Cowden, W. B.; Fenn, M. D. (1994). The Pyrimidines. New York: John Wiley & Sons. hlm. 5–6. ISBN 0-471-50656-7.