Unsur periode 4
| Periode 4 dalam tabel periodik |
Unsur periode 4 adalah unsur-unsur kimia pada baris (atau periode) keempat tabel periodik. Tabel periodik disusun berdasarkan baris untuk menggambarkan tren keberulangan (periodik) perilaku kimia unsur-unsur seiring dengan kenaikan nomor atom: baris baru dimulai ketika perilaku[1] kimia mulai berulang, artinya bahwa unsur-unsur dengan perilaku yang sama jatuh pada kolom yang sama.
Periode 4 mengandung 20 unsur, dimulai dari kalium dan diakhiri oleh kripton. Sesuai kaidah, unsur-unsur periode 4 mengisi terlebih dahulu kulit 4s, disusul kulit 3d dan 4p, urutannya seperti itu. Namun, terdapat perkecualian, misalnya kromium.
Sifat-sifat
[sunting | sunting sumber]Setiap unsur tunggal adalah stabil,[2] dan banyak terdapat dalam kerak dan/atau inti bumi; ini adalah periode terakhir tanpa kehadiran unsur tak stabil. Banyak logam transisi pada periode 4 yang luar biasa kuat, sehingga banyak digunakan dalam industri, terutama besi. Tembaga adalah satu dari tiga logam yang tidak berwarna perak atau abu-abu, dua lainnya adalah emas dan sesium. Tiga unsur yang berurutan dikenal beracun, dengan arsen sebagai salah satu racun yang paling terkenal, selenium yang beracun bagi manusia jika dalam kadar besar, dan bromin, cairan yang sangat beracun. Banyak unsur penting bagi keberlangsungan hidup manusia, seperti kalsium sebagai pembentuk tulang dan gigi.[1]
Tren periodik
[sunting | sunting sumber]Daftar unsur
[sunting | sunting sumber]Unsur kimia Golongan Konfigurasi elektron 19 K Kalium Logam alkali [Ar] 4s1 20 Ca Kalsium Logam alkali tanah [Ar] 4s2 21 Sc Skandium Logam transisi [Ar] 3d1 4s2 22 Ti Titanium Logam transisi [Ar] 3d2 4s2 23 V Vanadium Logam transisi [Ar] 3d3 4s2 24 Cr Kromium Logam transisi [Ar] 3d5 4s1 (*) 25 Mn Mangan Logam transisi [Ar] 3d5 4s2 26 Fe Besi Logam transisi [Ar] 3d6 4s2 27 Co Kobalt Logam transisi [Ar] 3d7 4s2 28 Ni Nikel Logam transisi [Ar] 3d8 4s2 29 Cu Tembaga Logam transisi [Ar] 3d10 4s1 (*) 30 Zn Seng Logam transisi [Ar] 3d10 4s2 31 Ga Galium Logam miskin [Ar] 3d10 4s2 4p1 32 Ge Germanium Metaloid [Ar] 3d10 4s2 4p2 33 As Arsenik Metaloid [Ar] 3d10 4s2 4p3 34 Se Selenium Nonlogam poliatomik [Ar] 3d10 4s2 4p4 35 Br Bromine Nonlogam diatomik [Ar] 3d10 4s2 4p5 36 Kr Kripton Gas mulia [Ar] 3d10 4s2 4p6
(*) Perkecualian pada aturan Madelung
Legenda warna latar belakang
|
Unsur blok-s
[sunting | sunting sumber]Kalium
[sunting | sunting sumber]
Kalium adalah unsur kimia dengan lambang K dan nomor atom 19. Kalium adalah sebuah logam alkali, yang ditempatkan di bawah natrium dan di atas rubidium, dan merupakan unsur pertama dari periode 4.[3] Ia merupakan salah satu unsur palilng reaktif dalam tabel periodik, sehingga biasanya hanya dijumpai dalam bentuk senyawa. Ia cenderung teroksidasi dengan cepat di udara, sehingga bereaksi sangat cepat dengan oksigen ketika baru terpapar udara. Ketika baru terpapar, ia berwarna agak keperakan, tetapi dengan cepat memudar akibat bereaksi dengan udara. Logam ini cukup lunak untuk dipotong menggunakan pisau, dan merupakan unsur kedua dengan massa jenis paling ringan.[4] Kalium mempunyai titik lebur relatif rendah; ia akan meleleh hanya dengan meletakkannya di bawah api kecil.[5] Kalium juga memiliki massa jenis yang lebih kecil daripada air, sehingga dapat mengapung di air.[6]
Kalsium
[sunting | sunting sumber]
Kalsium adalah unsur kimia dengan lambang Ca dan nomor atom 20. Kalsium adalah unsur kedua dalam periode 4, antara kalium dan skandium. Sebagai sebuah logam alkali tanah, kalsium tidak pernah ditemukan di alam karena reaktivitas tingginya antara aku dengan kamu dan kamu dengan air.[7] Unsur tersebut merupakan salah satu unsur yang paling dikenal dan peran biologi paling dikenal dalam seluruh hewan dan beberapa tumbuhan, penyusun tulang dan gigi, dan digunakan dalam beberapa aplikasi sel, seperti sinyal untuk proses seluler. Kalsium dianggap sebagai mineral yang paling melimpah dalam massa tubuh.[8]
Unsur blok-d
[sunting | sunting sumber]Skandium
[sunting | sunting sumber]
Skandium adalah unsur kimia dengan lambang Sc dan nomor atom 21. Skandium adalah unsur ketiga dalam periode 4, antara kalsium dan titanium, dan merupakan logam transisi pertama dalam tabel periodik. Skandium cukup banyak terdapat di alam, tetapi sulit dijumpai karena merupakan yang banyak terdapat dalam senyawa tanah jarang, yang mana sulit diisolasi unsur-unsurnya. Skandium memiliki sedikit aplikasi komersial karena fakta-fakta tersebut di atas, dan aplikasi utama saat ini hanyalah sebagai bahan logam paduan dengan aluminium.
Titanium
[sunting | sunting sumber]
Titanium adalah unsur kimia dengan lambang Ti dan nomor atom 22. Titanium adalah unsur dalam periode 4, antara skandium dan vanadium. Titanium merupakan salah satu logam dengan massa jenis paling ringan sekaligus salah satu logam paling kuat dan paling tahan karat, sehingga banyak memiliki aplikasi, terutama dalam logam paduan dengan unsur lain, seperti besi. Oleh karena sifat-sifat tersebut di atas, ia banyak digunakan dalam pesawat terbang, stik golf, dan objek-objek lain yang memerlukan kekuatan, tetapi sekaligus harus ringan.
Vanadium
[sunting | sunting sumber]
Vanadium adalah unsur kimia dengan lambang V dan nomor atom 23. Vanadium adalah unsur dalam periode 4, antara titanium dan krom. Vanadium tidak pernah dijumpai dalam bentuk murni di alam, tetapi umum ditemukan dalam bentuk senyawa. Vanadium mirip dengan titanium dalam beberapa hal, seperti sangat tahan karat, tetapi, tidak seperti titanium, ia teroksidasi di udara bahkan pada suhu ruang. Seluruh senyawa vanadium memiliki sekurang-kurangnya beberapa tingkat toksisitas, dan beberapa di antaranya sangat toksik.
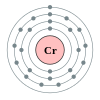
Kromium
[sunting | sunting sumber]
Kromium adalah unsur kimia dengan lambang Cr dan nomor atom 24. Kromium adalah unsur dalam periode 4, antara vanadium dan mangan. Kromium, seperti titanium dan vanadium sebelumnya, sangat tahan terhadap korosi, dan oleh sebab itu menjadi salah satu komponen utama baja nirkarat. Kromium juga memiliki banyak senyawa berwarna, dan oleh karena itu sangat jamak digunakan dalam pigmen, seperti hijau krom.
Mangan
[sunting | sunting sumber]
Mangan adalah unsur kimia dengan lambang Mn dan nomor atom 25. Mangan adalah unsur dalam periode 4, antara kromium dan besi. Mangan sering dijumpai dalam bentuk bebas di alam, tetapi juga ditemukan dalam kombinasi dengan besi. Mangan, seperti kromium sebelumnya, adalah komponen penting dalam baja nirkarat, mencegah besi berkarat. Mangan juga sering digunakan dalam pigmen, lagi-lagi seperti kromium. Mangan juga beracun; jika terhirup dalam kadar yang mencukupi, dapat menyebabkan kerusakan saraf permanen.
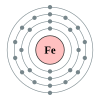
Besi
[sunting | sunting sumber]
Besi adalah unsur kimia dengan lambang Fe dan nomor atom 26. Besi adalah unsur dalam periode 4, antara mangan dan kobalt. Besi mungkin adalah unsur periode 4 yang paling terkenal, menjadikannya unsur yang paling jamak di bumi dan merupakan komponen utama baja. Besi-56 memiliki kerapatan energi terendah di antara isotop semua unsur, artinya bahwa ia adalah unsur paling masif yang dapat dihasilkan dalam bintang raksasa. Besi juga memiliki beberap aplikasi dalam tubuh manusia; sebagian dari hemoglobin adalah besi.
Kobalt
[sunting | sunting sumber]
Kobalt adalah unsur kimia dengan lambang Co dan nomor atom 27. Kobalt adalah unsur dalam periode 4, antara besi dan nikel. Kobalt banyak digunakan dalam pigmen, karena banyak senyawa kobalt berwarna biru. Kobalt juga merupakan komponen inti dari banyak aloy magnetis dan berkekuatan tinggi. Satu-satunya isotop stabil, kobalt-59, merupakan komponen penting vitamin B-12, sementara kobalt-60 adalah komponen limbah nuklir dan dapat berbahaya dalam jumlah besar karena sifat radioaktifnya.
Nikel
[sunting | sunting sumber]
Nikel adalah unsur kimia dengan lambang Ni dan nomor atom 28. Nikel adalah unsur dalam periode 4, antara kobalt dan tembaga. Nikel jarang terdapat dalam kerak bumi, terutama karena kenyataan bahwa ia bereaksi dengan oksigen di udara, dengan sebagian besar nikel di bumi berasal dari meteorit besi nikel. Namun, nikel sangat melimpah di inti bumi; bersama dengan besi ia merupakan salah satu dari dua komponen utama. Nikel adalah komponen utama dalam besi nirkarat, dan dalam banyak superaloy.
Tembaga
[sunting | sunting sumber]
Tembaga adalah unsur kimia dengan lambang Cu dan nomor atom 29. Tembaga adalah unsur dalam periode 4, antara nikel dan seng. Tembaga adalah salah satu dari sedikit logam yang tidak berwarna putih atau abu-abu, lainnya adalah emas dan sesium. Tembaga telah banyak dimanfaatkan oleh manusia selama ribuan tahun untuk memberi warna kemerahan pada banyak objek, dan bahkan merupakan nutrisi penting bagi manusia, meskipun beracun jika terlalu banyak. Tembaga juga banyak digunakan sebagai pengawet kayu atau fungisida.
Seng
[sunting | sunting sumber]
Seng adalah unsur kimia dengan lambang Zn dan nomor atom 30. Seng adalah unsur dalam periode 4, di antara tembaga dan galium. Seng adalah salah satu komponen utama kuningan, yang telah digunakan sejak abad ke-10 sebelum masehi. Seng juga sangat penting bagi manusia; hampir 2 miliar orang di dunia menderita kekurangan seng. Namun, overdosis seng dapat menyebabkan defisiensi tembaga. Seng sering digunakan dalam baterai, sebut saja baterai karbon-seng, dan unsur penting dalam banyak metode pelapisan, karena seng sangat tahan korosi.
Unsur blok-p
[sunting | sunting sumber]Galium
[sunting | sunting sumber]
Galium adalah unsur kimia dengan lambang Ga dan nomor atom 31. Galium adalah unsur dalam periode 4, antar seng dan germanium. Galium adalah unsur penting karena memiliki titik lebur sekitar 303 K, sekitar suhu kamar. Sebagai contoh, ia akan memadat pada musim semi, tetapi akan mencair pada musim panas. Galium merupakan komponen penting dalam logam paduan galinstan, bersama dengan timah. Galium juga dapat dijumpai dalam semikonduktor.
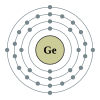
Germanium
[sunting | sunting sumber]
Germanium adalah unsur kimia dengan lambang Ge dan nomor atom 32. Germanium adalah sebuah unsur dalam periode 4, antara gallium dan arsenik. Germanium, seperti silikon di atas, adalah komponen penting dalam semikonduktor dan banyak digunakan dalam dioda dan transistor, sering kali kombinasi dengan arsenik. Germanium jarang ditemukan di bumi, oleh karenanya termasuk yang terakhir ditemukan. Germanium, dalam senyawa, dapat mengiritasi mata, kulit, atau lambung.
Arsenik
[sunting | sunting sumber]
Arsenik adalah unsur kimia dengan lambang As dan nomor atom 33. Arsenik adalah sebuah unsur dalam periode 4, antara germanium dan selenium. Arsenik, seperti telah disinggung sebelumnya, sering digunakan untuk semikonduktor dalam paduannya dengan germanium. Arsenik, dalam bentuk murni dan beberapa aloy, sangat beracun bagi seluruh kehidupan multisel, dan oleh karenanya merupakan komponen yang umum digunakan dalam pestisida. Arsenik juga digunakan dalam beberapa pigmen sebelum toksisitasnya terungkap.
Selenium
[sunting | sunting sumber]
Selenium adalah unsur kimia dengan lambang Se dan nomor atom 34. Selenium adalah sebuah unsur dalam periode 4, antara arsenik dan bromin. Selenium adalah nonlogam pertama dalam periode 4, dengan sifat yang mirip dengan belerang. Selenium cukup jarang dijumpai di alam dalam bentuk murni, kebanyakan ditemukan dalam mineral seperti pirit, dan bahkan inipun cukup jarang. Selenium diperlukan oleh manusia dalam kadar renik, tetapi unsur ini toksik dalam kadar besar.
Bromin
[sunting | sunting sumber]
Bromin adalah unsur kimia dengan lambang Br dan nomor atom 35. Bromin adalah sebuah unsur dalam periode 4, antara selenium dan kripton. Bromin adalah sebuah halogen, tidak pernah ada dalam bentuk murni di alam. Bromin berbentuk cair dalam temperatur kamar, mendidih pada temperatur sekitar 330 K. Bromin juga cukup toksik dan korosif, tetapi ion bromida, yang relatif inert, dapat dijumpai dalam halit, atau garam meja. Bromin sering digunakan sebagai penahan api karena banyak senyawa dapat dibuat untuk membebaskan atom bromin bebas.
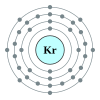
Kripton
[sunting | sunting sumber]
Kripton adalah unsur kimia dengan lambang Kr dan nomor atom 36. Kripton adalah sebuah gas mulia yang ditempatkan di bawah argon dan di atas xenon. Sebagai gas mulia, kripton jarang berinteraksi dengan dirinya sendiri maupun dengan unsur lain; meskipun beberapa senyawa kripton telah terdeteksi, seluruhnya tidak stabil dan meluruh dengan cepat. Oleh karenanya, kripton sering digunakan dalam lampu pendar. Kripton, seperti gas mulia lainnya, juga digunakan dalam penerangan karena ia memiliki banyak garis spektrum dan alasan-alasan di atas.
Peran biologis
[sunting | sunting sumber]Kalium penting bagi kehidupan. Ion kalium dijumpai dalam seluruh sel. Ia diperlukan untuk mempertahankan keseimbangan cairan dan elektrolit. Sel tanaman sangat kaya kalium, yang mereka dapat dari tanah. Lahan pertanian, yang dipanen setiap tahun, perlu dikembalikan kandungan kaliumnya dengan penambahan pupuk berbasis kalium. Rata-rata manusia mengkonsumsi sampai dengan 7 gram kalium per hari, dan menyimpan sekitar 140 gram dalam sel tubuh. Diet sehat normal mengandung kalium, tetapi beberapa makanan seperti kopi instan, sarden, kacang, kismis, kentang, cokelat memiliki kandungan kalium di atas rata-rata. Isotop alami kalium-40 bersifat radioaktif dan, meskipun tingkat radiasinya rendah, merupakan salah satu penyebab alami mutasi genetik pada manusia.[9]
Kalsium penting bagi seluruh bentuk kehidupan, terutama untuk pertumbuhan dan kesehatan tulang dan gigi. Kalsium fosfat adalah komponen utama tulang. Rata-rata manusia mengandung sekitar 1 kilogram kalsium. Anak-anak dan wanita hamil dianjurkan mengonsumsi makanan yang kaya kalsium, seperti susu dan produk susu, sayuran berdaun hijau, ikan dan kacang serta biji-bijian.[10]
Peran biologis skandium tidak diketahui. Unsur ini diduga karsinogen.[11]
Peran biologis titanium tidak diketahui. Unsur ini tak beracun. Debu halus titanium dioksida diduga karsinogen.[12]
Vanadium penting bagi beberapa spesies, termasuk manusia, meskipun kebutuhannya sangat kecil. Manusia hanya mengasup sekitar 0,01 miligram per hari, dan ini sudah melebihi kebutuhan harian tubuh manusia. Dalam beberapa senyawa vanadium dapat bersifat racun.[13]
Krom atau kromium merupakan unsur renik yang penting bagi manusia karena membantu pemanfaatan glukosa tubuh. Namun, unsur ini beracun jika berlebih. Asupan harian sekitar 1 miligram per hari. Makanan seperti ragi bir, wheat germ dan ginjal kaya akan kromium.[14]
Mangan adalah unsur esensial dalam organisme hidup. Banyak jenis enzim mengandung mangan. Sebagai contoh, enzim yang bertindak mengubah molekul air menjadi oksigen selama fotosintesis mengandung empat atom mangan. Beberapa lahan berkadar mangan rendah, sehingga perlu ditambahkan pupuk dan diberikan sebagai suplemen pakan bagi hewan pemakan rumput. Rata-rata tubuh manusia mengandung 12 miligram mangan. Asupan mangan per hari sekitar 4 miligram dari makanan seperti kacang, dedak, sereal utuh (wholegrain cereals), teh dan peterseli. Tanpa mangan, tulang menjadi keropos dan mudah retak. Mangan juga esensial dalam utilisasi vitamin B1.[15]
Besi adalah unsur esensial bagi segala bentuk kehidupan dan tak beracun. Rata-rata manusia mengandung sekitar 4 gram besi. Sebagian besar berada dalam hemoglobin, dalam darah. Hemoglobin mengangkut oksigen dari paru-paru menuju sel, tempat oksigen digunakan untuk respirasi jaringan. Manusia membutuhkan 10–18 miligram besi setiap harinya. Kekurangan besi akan menyebabkan anemia. Makanan seperti hati, ginjal, molases, ragi bir, kokoa dan liquorice mengandung banyak besi.[16]
Kobalt adalah unsur renik esensial, dan pembentuk bagian aktif vitamin B12. Jumlah yang dibutuhkan manusia sangat kecil, dan tubuh hanya mengandung sekitar 1 miligram. Garam kobalt dapat diberikan kepada hewan tertentu dalam dosis kecil untuk mengobati defisiensi mineral. Dalam dosis besar, kobalt bersifat karsinogenik.
Kobalt-60 adalah isotop radioaktif. Ini merupakan sumber sinar-gama yang penting. Ia banyak digunakan dalam pengobatan kanker, sebagai penjejak dan untuk radioterapi.[17]
Peran biologi nikel tidak menentu. Ia dapat mempengaruhi pertumbuhan tanaman tetapi telah menunjukkan bahwa ia penting bagi beberapa spesies. Beberapa senyawa nikel dapat menyebabkan kanker jika debunya terhirup, dan beberapa orang alergi jika kontak dengan logam ini. Nikel tidak dapat sepenuhnya dihindari. Manusia mengkonsumsi senyawa nikel bersamaan dengan makanan. Ini adalah unsur esensial bagi beberapa kacang-kacangan, seperti navy bean yang digunakan untuk kacang panggang.[18]
Tembaga adalah unsur esensial. Manusia dewasa memerlukan sekitar 1,2 miligram tembaga per hari, untuk membantu enzim memindahkan energi dalam sel. Overdosis tembaga bersifat racun. Kelainan genetika, seperti penyakit Wilson dan penyakit Menkes, dapat mempengaruhi kemampuan tubuh untuk menggunakan tembaga secara benar. Tidak seperti mamalia, yang menggunakan besi (dalam hemoglobin) untuk transportasi oksigen ke seluruh tubuh, beberapa krustasea menggunakan kompleks tembaga.[19]
Seng penting untuk seluruh makhluk hidup, membentuk titik-titik aktif dalam lebih dari 20 metalo-enzim. Rata-rata tubuh manusia mengandung sekitar 2,5 gram dan mengasup sekitar 15 miligram per hari. Beberapa makanan memiliki kadar seng di atas rata-rata, di antaranya ikan hering, daging sapi, daging domba, biji bunga matahari dan keju. Seng dapat menjadi karsinogenik jika berlebih. Menghirup seng(II) oksida yang baru terbentuk, dapat mengakibatkan suatu gejala yang disebut ‘gemetar oksida’ (oxide shakes) atau 'menggigil seng' (zinc chills).[20]
Galium tidak diketahui mempunyai peran biologis apapun. Unsur ini tak beracun.[21]
Germanium tidak diketahui mempunyai peran biologis apapun. Unsur ini tak beracun. Senyawa germanium tertentu memiliki efek racun rendah pada mamalia, sementara daya racunnya efektif melawan beberapa bakteri. Ini memicu beberapa ilmuwan meneliti potensi manfaat unsur ini untuk obat-obatan.[22]
Beberapa ilmuwan berpikir bahwa arsen merupakan unsur esensial dalam makanan dalam dosis yang amat sangat kecil. Dalam dosis kecil, arsen bersifat toksik dan diduga karsinogen. Sekali masuk kedalam tubuh, arsen terikat dengan atom-atom dalam rambut, sehingga analisis sampel rambut dapat menunjukkan paparan arsenik pada seseorang. Beberapa makanan, seperti udang, mengandung kadar arsenik yang mengejutkan, tetapi dalam bentuk yang kurang berbahaya yaitu arsen organik.[23]
Selenium adalah unsur renik esensial untuk beberapa spesies, termsuk manusia. Tubuh manusia mengandung sekitar 14 miligram, dan setiap sel dalam tubuh manusia mengandung lebih dari satu juta atom selenium. Kekurangan selenium dapat menyebabkan masalah kesehatan, tetapi terlalu banyak juga berbahaya. Dalam dosis berlebih, selenium bersifat karsinogenik dan teratogenik (mengganggu perkembangan embrio atau janin).[24]
Bromin hadir dalam jumlah kecil, sebagai bromida, dalam semua makhluk hidup. Namun, belum diketahui peran biologisnya bagi manusia. Bromin memiliki efek iritasi pada mata dan tenggorokan, dan menghasilkan rasa nyeri jika terkena kulit.[25]
Kripton tidak diketahui memiliki peran biologis.[26]
Tabel unsur
[sunting | sunting sumber]| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Golongan → | ||||||||||||||||||||||||||||||
| ↓ Periode | ||||||||||||||||||||||||||||||
| 4 | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
Lihat juga
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ a b Gray, Theodore (2009). The Elements: A Visual Exploration of Every Known Atom in the Universe. New York: Black Dog & Leventhal Publishers. ISBN 978-1-57912-814-2.
- ^ "List of Elements of the Periodic Table – Sorted by Abundance in Earth's crust". Science.co.il. Diakses tanggal 2012-08-14.
- ^ "Elements in the Modern Periodic Table, Periodic Classification of Elements". Tutorvista.com. Diarsipkan dari versi asli tanggal 2017-12-22. Diakses tanggal 2012-08-14.
- ^ "It's Elemental – The Element Potassium". Education.jlab.org. Diakses tanggal 2012-08-14.
- ^ "Potassium, Chemical Element – Overview, Discovery and naming, Physical properties, Chemical properties, Occurrence in nature, Isotopes". Chemistryexplained.com. Diakses tanggal 2012-08-14.
- ^ "Potassium (K) – Chemical properties, Health and Environmental effects". Lenntech.com. Diakses tanggal 2012-08-14.
- ^ "Reactions of the Group 2 elements with water". Chemguide.co.uk. Diakses tanggal 2012-08-14.
- ^ "Chapter 11. Calcium", Human Vitamin and Mineral Requirements, Rome, Italy: Report of a joint FAO/WHO expert consultation, 2002, diakses tanggal 2012-08-14
- ^ "Potassium". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Calcium". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Scandium". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Titanium". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Vanadium". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Chromium". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Manganese". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Iron". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Cobalt". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Nickel". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Copper". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Zinc". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Gallium". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Germanium". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Arsenic". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Selenium". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Bromine". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.
- ^ "Krypton". Periodic Table. Royal Society of Chemistry. Diakses tanggal 2016-02-10.