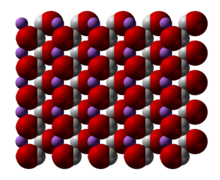
Litium hidroksida
| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Liitium hidroksida
| |
| Nama lain
Litina
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
| Referensi Gmelin | 68415 |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
| Nomor UN | 2680 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| LiOH | |
| Massa molar | 23.95 g/mol (anhidrat) 41.96 g/mol (monohidrat) |
| Penampilan | padatan putih higroskopis tak berbau |
| Densitas | 1.46 g/cm3 (anhidrat) 1.51 g/cm3 (monohidrat) |
| Titik lebur | 462 °C |
| Titik didih | 924 °C terurai |
| anhidrat: 12.7 g/100 mL (0 °C) 12.8 g/100 mL (20 °C) 17.5 g/100 mL (100 °C) monohidrat: 22.3 g/100 mL (10 °C) 26.8 g/100 mL (80 °C)[1] | |
| Kelarutan dalam metanol | anhidrat: 9.76 g/100 g (20 °C, 48 jam pencampuran) monohidrat: 13.69 g/100 g (20 °C, 48 jam pencampuran)[2] |
| Kelarutan dalam etanol | anhidrat: 2.36 g/100 g (20 °C, 48 jam pencampuran) monohidrat: 2.18 g/100 g (20 °C, 48 jam pencampuran)[2] |
| Kelarutan dalam isopropanol | anhidrat: 0 g/100 g (20 °C, 48 jam pencampuran) monohidrat: 0.11 g/100 g (20 °C, 48 jam pencampuran)[2] |
| Kebasaan (pKb) | −0.04[3](LiOH(aq) = Li+ + OH–) |
| −12.3·10−6 cm3/mol | |
| Indeks bias (nD) | 1.464 (anhidrat) 1.460 (monohidrat) |
| Termokimia | |
| Kapasitas kalor (C) | 2.071 J/g K |
| Entalpi pembentukan standar (ΔfH |
-20.36 kJ/g |
| Bahaya | |
| Bahaya utama | Korosif |
| Lembar data keselamatan | ICSC 0913 ICSC 0914 (monohidrat) |
| Titik nyala | Tidak mudah terbakar |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
210 mg/kg (oral, tikus)[4] |
| Senyawa terkait | |
Anion lain
|
Litium amida |
Kation lainnya
|
Natrium hidroksida Kalium hidroksida Rubidium hidroksida Cesium hidroksida |
Senyawa terkait
|
Litium oksida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Litium hidroksida adalah suatu senyawa anorganik dengan rumus kimia LiOH. Senyawa ini adalah material kristalin yang bersifat higroskopis. Senyawa ini larut dalam air dan sedikit larut dalam etanol, dan tersedia secara komersial dalam bentuk anhidrat dan sebagai monohidratnya (LiOH.H2O), keduanya merupakan basa kuat. Senyawa ini adalah basa terlemah di antara hidroksida logam alkali.
Produksi dan reaksi
[sunting | sunting sumber]Litium hidroksida diproduksi dalam suatu reaksi metatesis antara litium karbonat dan kalsium hidroksida:[5]
- Li2CO3 + Ca(OH)2 → 2 LiOH + CaCO3
Hidrat yang diproduksi awalnya didehidrasi dengan pemanasan di bawah vakum hingga 180 °C.
Di laboratorium, litium hidroksida timbul oleh aksi air dalam litium atau litium oksida. Persamaan untuk proses berikut ini:
- 2 Li + 2 H2O → 2 LiOH + H2
- Li2O + H2O → 2 LiOH
Biasanya, reaksi ini dihindari.
Meskipun litium karbonat lebih banyak digunakan, hidroksida adalah prekursor yang efektif untuk garam litium, misalnya
- LiOH + HF → LiF + H2O.
Aplikasi
[sunting | sunting sumber]Litium hidroksida terutama dikonsumsi untuk produksi gemuk litium. Gemuk litium yang populer adalah litium stearat, yang merupakan pelumas umum untuk gemuk karena ketahanannya yang tinggi terhadap air dan kegunaan pada suhu tinggi maupun rendah.
Penghilangan karbon dioksida
[sunting | sunting sumber]Litium hidroksida digunakan dalam sistem pemurnian gas pernapasan untuk pesawat antariksa, kapal selam, dan rebreather untuk menghilangkan karbon dioksida dari gas yang dihembuskan dengan memproduksi litium karbonat dan air:[6]
- 2 LiOH·H2O + CO2 → Li2CO3 + 3 H2O
Atau,
- 2 LiOH + CO2 → Li2CO3 + H2O
Yang terakhir, anhidrat hidroksida, lebih disukai untuk menurunkan massa dan produksi air yang lebih rendah untuk sistem respirator di pesawat ruang angkasa. Satu gram hidroksida litium anhidrat dapat melepas 450 cm3 gas karbon dioksida. Monohidratnya kehilangan air pada suhu 100–110 °C.
Penggunaan lainnya
[sunting | sunting sumber]Senyawa ini digunakan sebagai media perpindahan panas dan sebagai baterai-tempat penyimpanan elektrolit. Senyawa ini juga digunakan dalam formulasi keramik dan beberapa semen Portland. Litium hidroksida (diperkaya secara isotopik dalam litium-7) digunakan untuk mengalkalikan pendingin reaktor dalam reaktor air bertekanan untuk pengendalian korosi.
Pasar
[sunting | sunting sumber]Pada tahun 2012, harga litium hidroksida adalah sekitar $5,000 hingga $6,000 per ton.[7]
Lihat pula
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ Lide, David R., ed. (2006). CRC Handbook of Chemistry and Physics (edisi ke-87). Boca Raton, Florida: CRC Press. ISBN 0-8493-0487-3.
- ^ a b c Khosravi, Javad (2007). "9: Results". PRODUCTION OF LITHIUM PEROXIDE AND LITHIUM OXIDE IN AN ALCOHOL MEDIUM. ISBN 978-0-494-38597-5.
- ^ Popov, K.; et al. (2002). "7Li, 23Na, 39K and 133Cs NMR comparative equilibrium study of alkali metal cation hydroxide complexes in aqueous solutions. First numerical value for CsOH formation". Inorganic Chemistry Communications. 5 (3): 223–225. Diakses tanggal 2017-01-21.
- ^ http://chem.sis.nlm.nih.gov/chemidplus/rn/1310-65-2
- ^ Wietelmann, U; Bauer, RJ (2000). "Lithium and Lithium Compounds". Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a15_393. ISBN 3-527-30673-0.
- ^ Jaunsen, JR (1989). "The Behavior and Capabilities of Lithium Hydroxide Carbon Dioxide Scrubbers in a Deep Sea Environment". US Naval Academy Technical Report. USNA-TSPR-157. Diarsipkan dari versi asli tanggal 2009-08-24. Diakses tanggal 2008-06-17.
- ^ "Salinan arsip". Diarsipkan dari versi asli tanggal 2018-03-11. Diakses tanggal 2017-07-15.
Pranala luar
[sunting | sunting sumber]- International Chemical Safety Card 0913 (anhidrat)
- International Chemical Safety Card 0914 (monohidrat)
