Format (kimia)

| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC (preferensi)
Format | |||
| Nama IUPAC (sistematis)
Metanoat | |||
| Nama lain
Formilat
Metilat Isokarbonit Karbonit(1-) Hidrogenkarboksilat Metakarbonoat Oksokarbinat Ion oksometil oksida Oksometoksida | |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChemSpider | |||
| Nomor EC | |||
| MeSH | Formates | ||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| UNII | |||
| |||
| Sifat | |||
| HCOO− atau HCO−2 | |||
| Massa molar | 45,017 g mol−1 | ||
| Asam konjugat | Asam format | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
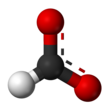
Format (nama IUPAC: metanoat) adalah basa konjugat dari asam format. Format adalah sebuah anion (HCO−
2) atau turunannya seperti ester dari asam format. Garam dan ester format umumnya tidak memiliki warna.[1]
Dasar
[sunting | sunting sumber]Ketika dilarutkan dalam air, asam format berubah menjadi format:
- HCO
2H → HCO−
2 + H+
Format adalah anion planar. Dua atom oksigennya setara dan memiliki muatan negatif parsial. Ikatan C–H yang tersisa tidak bersifat asam.
Biokimia
[sunting | sunting sumber]Format adalah sumber C-1 yang umum dalam sistem kehidupan. Ia terbentuk dari banyak prekursor seperti kolina, serina, dan sarkosina. Ia menyediakan sumber C-1 dalam biosintesis beberapa asam nukleat. Format (atau asam format) digunakan sebagai gugus yang meninggalkan dalam demetilasi beberapa sterol.[2] Konversi ini dikatalisis oleh enzim aromatase menggunakan O2 sebagai oksidan. Konversi spesifik meliputi testosteron menjadi estradiol dan androstenedion menjadi estron.[3]
Format dioksidasi secara reversibel oleh enzim format dehidrogenase dari Desulfovibrio gigas:[4]
- HCO−
2 → CO
2 + H+
+ 2 e−
Ester format
[sunting | sunting sumber]Ester format memiliki rumus HCOOR (cara alternatif untuk menulis rumus ROC(O)H atau RO2CH). Banyak senyawa ester format yang terbentuk secara spontan ketika alkohol larut dalam asam format.
Ester format yang paling penting adalah metil format, yang diproduksi sebagai zat perantara dalam perjalanan menuju asam format. Metanol dan karbon monoksida akan bereaksi dengan adanya basa kuat, seperti natrium metoksida:[1]
- CH
3OH + CO → HCOOCH
3
Hidrolisis metil format menghasilkan asam format dan meregenerasi metanol:
- HCOOCH
3 → HCOOH + CH
3OH
Asam format digunakan untuk banyak aplikasi dalam industri.
Ester format sering kali memiliki bau harum atau bau yang khas. Dibandingkan dengan ester asetat yang lebih umum, ester format lebih jarang digunakan secara komersial karena kurang stabil.[5] Etil format ditemukan di beberapa penganan.[1]
Garam format
[sunting | sunting sumber]Garam format memiliki rumus M(O2CH)(H2O)x. Garam semacam ini rentan terhadap dekarboksilasi. Sebagai contoh, nikel format terhidrasi akan terdekarboksilasi pada suhu sekitar 200 °C dengan reduksi Ni2+ menjadi bubuk logam nikel halus:
- Ni(HCO
2)
2(H
2O)
2 → Ni + 2 CO
2 + 2 H
2O + H
2
Bubuk halus tersebut berguna sebagai katalis hidrogenasi.[1]
Contoh
[sunting | sunting sumber]
- etil format, CH3CH2(HCOO)
- natrium format, Na(HCOO)
- kalium format, K(HCOO)
- sesium format, Cs(HCOO); lihat Sesium: Eksplorasi minyak bumi
- metil format, CH3(HCOO)
- metil kloroformat, CH3OCOCl
- trietil ortoformat
- trimetil ortoformat, C4H10O3
- fenil format HCOOC6H5
- amil format
Referensi
[sunting | sunting sumber]- ^ a b c d Werner Reutemann and Heinz Kieczka "Formic Acid" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a12_013
- ^ Pietzke, Matthias; Meiser, Johannes; Vazquez, Alexei (2020). "Formate Metabolism in Health and Disease". Molecular Metabolism. 33: 23–37. doi:10.1016/j.molmet.2019.05.012. PMC 7056922
 . PMID 31402327.
. PMID 31402327.
- ^ Lephart, E. D. (1996). "A Review of Brain Aromatase Cytochrome P450". Brain Res. Rev. 22 (1): 1–26. doi:10.1016/0165-0173(96)00002-1. PMID 8871783.
- ^ T. Reda, C. M. Plugge, N. J. Abram and J. Hirst, "Reversible interconversion of carbon dioxide and formate by an electroactive enzyme", PNAS 2008 105, 10654–10658. DOI:10.1073/pnas.0801290105
- ^ Johannes Panten dan Horst Surburg "Flavors and Fragrances, 2. Aliphatic Compounds" dalam Ullmann's Encyclopedia of Industrial Chemistry, 2015, Wiley-VCH, Weinheim.DOI:10.1002/14356007.t11_t01