Talium(I) bromida
| |
| Nama | |
|---|---|
| Nama lain
Talium monobromida
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| TlBr | |
| Massa molar | 284,287 g/mol[1] |
| Penampilan | Padatan kristalin kuning[1] |
| Densitas | 7,5 g/cm3[1] |
| Titik lebur | 460 °C (860 °F; 733 K)[1] |
| Titik didih | 819 °C (1.506 °F; 1.092 K)[1] |
| 0,59 g/L (25 °C)[1] | |
| Hasil kali kelarutan, Ksp | 3,71×10−6[2] |
| −63,9·10−6 cm3/mol[3] | |
| Indeks bias (nD) | 2,418 (0,59 µm) 2,350 (0,75 µm) 2,289 (1 µm) 1,984 (5 µm) 2,322 (20 µm)[4] |
| Struktur | |
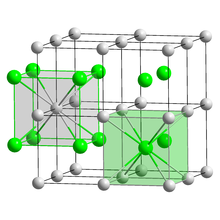
| CsCl, cP2 | |
| Pm3m, No. 221[5] | |
Satuan formula (Z)
|
1 |
| Kubik (Tl+) Kubik (Br−) | |
| Bahaya | |
| Piktogram GHS |   
|
| Keterangan bahaya GHS | {{{value}}} |
| H300, H330, H373, H411 | |
| P260, P264, P270, P271, P273, P284, P301+310, P304+340, P310, P314, P320, P321, P330, P391, P403+233, P405, P501 | |
| Senyawa terkait | |
Anion lain
|
Talium(I) fluorida, Talium(I) klorida, Talium(I) iodida |
Kation lainnya
|
Indium(I) bromida, Timbal(II) bromida Bismut bromida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Talium(I) bromida adalah sebuah senyawa kimia dari talium dan bromin dengan rumus kimia TlBr. Garam ini digunakan dalam detektor suhu kamar untuk sinar-X, sinar gama dan cahaya biru, serta optika inframerah-dekat.
Talium(I) bromida adalah bahan semikonduktor dengan sela pita sebesar 2,68 eV.[6]
Senyawa ini memiliki struktur kristal jenis CsCl kubik pada suhu kamar, tetapi akan berubah menjadi jenis talium iodida ortorombik pada saat didinginkan, dan suhu transisi kemungkinan besar dipengaruhi oleh pengotor.[7] Film TlBr setipis beberapa nanometer yang ditumbuhkan pada substrat LiF, NaCl, atau KBr menunjukkan struktur garam batu.[5]
Talium sangatlah beracun dan merupakan racun kumulatif yang dapat diserap melalui kulit. Efek akut dan kronis dari penelanan senyawa talium meliputi kelelahan, nyeri ekstremitas, neuritis perifer, nyeri sendi, rambut rontok, diare, muntah, kehilangan penglihatan, serta kerusakan pada sistem saraf pusat, hati, dan ginjal.[8]
Referensi[sunting | sunting sumber]
- ^ a b c d e f Haynes, hlm. 4.94
- ^ John Rumble (18 Juni 2018). CRC Handbook of Chemistry and Physics (dalam bahasa English) (edisi ke-99). CRC Press. hlm. 5–189. ISBN 978-1138561632.
- ^ Haynes, hlm. 4.135
- ^ Haynes, hlm. 10.242
- ^ a b Schulz, L. G. (1951). "Polymorphism of cesium and thallium halides". Acta Crystallographica. 4 (6): 487–489. doi:10.1107/S0365110X51001641.
- ^ Temperature Dependence of Spectroscopic Performance of Thallium Bromide X- and Gamma-Ray Detectors
- ^ Blackman, M; Khan, I H (1961). "The Polymorphism of Thallium and Other Halides at Low Temperatures". Proceedings of the Physical Society. 77 (2): 471. Bibcode:1961PPS....77..471B. doi:10.1088/0370-1328/77/2/331.
- ^ Thallium Bromide Material safety data sheet. espimetals.com
Sumber terkutip[sunting | sunting sumber]
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (edisi ke-92). Boca Raton, FL: CRC Press. ISBN 1439855110.
