Mangan: Perbedaan antara revisi
kTidak ada ringkasan suntingan |
Add 1 book for Wikipedia:Pemastian (20240409)) #IABot (v2.0.9.5) (GreenC bot |
||
| (11 revisi perantara oleh 9 pengguna tidak ditampilkan) | |||
| Baris 1: | Baris 1: | ||
{{ |
{{Bedakan|text=[[Magnesium]] ''(Mg)''}} |
||
{{ |
{{Kotak info mangan}} |
||
'''Mangan''', '''batu kawi''', atau '''bekawi''' adalah sebuah [[unsur kimia]] dengan [[Lambang unsur|lambang]] '''Mn''' dan [[nomor atom]] 25. Ia adalah logam yang keras, rapuh, dan berwarna keperakan yang sering ditemukan dalam [[mineral]] yang dikombinasikan dengan [[besi]]. Mangan adalah sebuah [[logam transisi]] dengan beragam penggunaan paduan industri, khususnya [[baja nirkarat]]. Ia dapat meningkatkan kekuatan, kemampuan kerja, dan ketahanan aus. Mangan oksida digunakan sebagai zat pengoksidasi; sebagai aditif karet; serta dalam pembuatan kaca, pupuk, dan keramik. Mangan sulfat dapat digunakan sebagai [[fungisida]]. |
|||
'''Mangan''' adalah [[unsur kimia]] dalam [[tabel periodik]] yang memiliki lambang '''Mn''' dan [[nomor atom]] 25. '''Mangan''' berupa [[logam transisi]] yang berwarna perak metalik. |
|||
Mangan juga merupakan unsur makanan manusia yang penting, penting dalam metabolisme makronutrien, pembentukan tulang, dan sistem pertahanan [[radikal bebas]]. Ia adalah komponen penting dalam lusinan protein dan enzim.<ref name="Erikson-2019" /> Sebagian besar mangan ditemukan di tulang, tetapi juga di hati, ginjal, dan otak.<ref name="Emsley2001" /> Di otak manusia, mangan terikat pada [[metaloprotein]] mangan, terutama [[glutamin sintetase]] dalam [[astrosit]]. |
|||
== Referensi == |
|||
{{reflist}} |
|||
Mangan pertama kali diisolasi pada tahun 1774. Ia dikenal di laboratorium dalam bentuk garam [[kalium permanganat]] berwarna lembayung tua. Ia terjadi di [[sisi aktif]] pada beberapa [[enzim]].<ref>{{cite book|last1=Roth |first1=Jerome |last2=Ponzoni |first2=Silvia |last3=Aschner |first3=Michael|editor1-first=Lucia |editor1-last=Banci |series=Metal Ions in Life Sciences |volume=12|pages=169–201 |chapter=Chapter 6 Manganese Homeostasis and Transport|title=Metallomics and the Cell |date=2013 |publisher=Springer |isbn=978-94-007-5560-4 |doi=10.1007/978-94-007-5561-1_6 |pmid=23595673 |pmc=6542352 }} Buku elektronik {{ISBN|978-94-007-5561-1}}.</ref> Salah satu hal yang menarik adalah penggunaan sebuah [[Gugus nano#Gugus atom|gugus]] Mn–O, [[kompleks yang mengembangkan oksigen]], dalam produksi oksigen oleh tumbuhan. |
|||
{{clr}} |
|||
==Karakteristik== |
|||
===Sifat fisik=== |
|||
Mangan adalah sebuah [[logam]] berwarna abu-abu keperakan yang menyerupai besi. Logam ini keras dan sangat rapuh, sulit melebur, tetapi mudah teroksidasi.<ref name="Holl">{{cite book|publisher=Walter de Gruyter|date=1985|edition=91–100 |pages=1110–1117|isbn=978-3-11-007511-3|title=Lehrbuch der Anorganischen Chemie|first=Arnold F.|last=Holleman|author2=Wiberg, Egon|author3=Wiberg, Nils|language=de|chapter=Mangan}}</ref> Logam mangan dan ionnya yang umum bersifat [[paramagnetisme|paramagnetik]].<ref name="magnet">{{cite book |url=https://archive.org/details/crchandbookofche81lide |url-status=dead |title=Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics |publisher=CRC press |isbn=978-0-8493-0485-9 |first=David R. |last=Lide |date=2004 |url-access=registration |access-date=27 Juni 2023 |archive-url=https://web.archive.org/web/20191217023342/https://archive.org/details/crchandbookofche81lide |archive-date=17 Desember 2019 }}</ref> Mangan akan ternoda perlahan di udara dan teroksidasi ("berkarat") seperti besi dalam air yang mengandung oksigen terlarut.{{Butuh rujukan|date=Juni 2023}} |
|||
===Isotop=== |
|||
{{Utama|Isotop mangan}} |
|||
Mangan alami terdiri dari satu [[isotop]] stabil, <sup>55</sup>Mn. Beberapa [[radionuklida|radioisotop]] telah diisolasi dan dijelaskan, dengan [[massa atom relatif|berat atom]] mulai dari 46 [[Dalton (satuan)|u]] (<sup>46</sup>Mn) hingga 72 u (<sup>72</sup>Mn). Isotop yang paling stabil adalah <sup>53</sup>Mn dengan [[waktu paruh]] 3,7 juta tahun, <sup>54</sup>Mn dengan waktu paruh 312,2 hari, dan <sup>52</sup>Mn dengan waktu paruh 5,591 hari. Semua isotop [[Peluruhan radioaktif|radioaktif]] yang tersisa memiliki waktu paruh kurang dari 3 jam, dan sebagian besar kurang dari 1 menit. [[Peluruhan radioaktif#Mode peluruhan|Mode peluruhan]] utama dari isotop yang lebih ringan daripada isotop stabil yang paling melimpah, <sup>55</sup>Mn, adalah [[tangkapan elektron|penangkapan elektron]] dan mode utama dari isotop yang lebih berat adalah [[peluruhan beta]].<ref name="Audi" /> Mangan juga memiliki tiga [[Isomer nuklir#Isomer metastabil|keadaan meta]].<ref name="Audi">{{NUBASE2016}}</ref> |
|||
Mangan adalah bagian dari unsur-unsur [[gugus besi]], yang diperkirakan disintesis di [[bintang]] besar sesaat sebelum ledakan [[supernova]].<ref>{{cite web |url=https://www.science.org/content/article/galaxy-s-brightest-explosions-go-nuclear-unexpected-trigger-pairs-dead-stars |title=The galaxy's brightest explosions go nuclear with an unexpected trigger: pairs of dead stars |work=Science |last=Clery |first=Daniel |date=4 Juni 2020 |access-date=27 Juni 2023 }}</ref> <sup>53</sup>Mn meluruh menjadi <sup>53</sup>Cr dengan waktu paruh 3,7 juta tahun. Karena waktu paruhnya yang relatif pendek, <sup>53</sup>Mn relatif jarang, dihasilkan oleh tumbukan [[sinar kosmik]] pada [[besi]].<ref>{{cite journal |last1=Schaefer |first1=Jeorg|last2=Faestermann |first2=Thomas |title=Terrestrial manganese-53 – A new monitor of Earth surface processes |journal=Earth and Planetary Science Letters|volume=251|issue=3–4 |pages=334–345|date=2006 |doi=10.1016/j.epsl.2006.09.016 |bibcode=2006E&PSL.251..334S |last3=Herzog |first3=Gregory F. |last4=Knie |first4=Klaus |last5=Korschinek |first5=Gunther |last6=Masarik |first6=Jozef |last7=Meier |first7=Astrid |last8=Poutivtsev |first8=Michail |last9=Rugel |first9=Georg |last10=Schlüchter |first10=Christian |last11=Serifiddin |first11=Feride |last12=Winckler |first12=Gisela}}</ref> Kandungan isotop mangan biasanya digabungkan dengan kandungan isotop [[kromium]] dan telah memiliki aplikasi dalam [[Geokimia isotop|geologi isotop]] dan [[penanggalan radiometrik]]. Rasio isotop Mn–Cr memperkuat bukti dari [[Aluminium-26|<sup>26</sup>Al]] dan [[Isotop paladium#Paladium-107|<sup>107</sup>Pd]] untuk sejarah awal [[Tata Surya]]. Variasi dalam rasio <sup>53</sup>Cr/<sup>52</sup>Cr dan Mn/Cr dari beberapa [[meteorit]] menunjukkan rasio awal <sup>53</sup>Mn/<sup>55</sup>Mn, yang menunjukkan bahwa komposisi isotop Mn–Cr harus dihasilkan dari peluruhan ''in situ'' dari <sup>53</sup>Mn dalam benda planet yang berbeda. Oleh karena itu, <sup>53</sup>Mn memberikan bukti tambahan untuk proses [[nukleosintesis]] segera sebelum penggabungan Tata Surya.<ref>{{cite journal|doi=10.1016/S0016-7037(99)00312-9 |title=53Mn-53Cr evolution of the early solar system|year=1999|last1=Birck|first1=J. |last2=Rotaru|last3=Allègre|journal=Geochimica et Cosmochimica Acta|volume=63|pages=4111–4117|first2=M.|first3=C.|bibcode=1999GeCoA..63.4111B |issue=23–24}}</ref><ref>{{cite journal |doi=10.1016/S0016-7037(98)00189-6|title=Early solar system timescales according to 53Mn-53Cr systematics |url=https://archive.org/details/sim_geochimica-et-cosmochimica-acta_1998-08_62_16/page/2863|year=1998|last1=Lugmair |first1=G.|journal=Geochimica et Cosmochimica Acta|volume=62|pages=2863–2886|bibcode=1998GeCoA..62.2863L|issue=16 |last2=Shukolyukov |first2=A.}}</ref><ref>{{cite journal|doi=10.1023/A:1005243228503|title=On The 53Mn Heterogeneity In The Early Solar System|year=2000|last1=Shukolyukov|first1=Alexander|last2=Lugmair |journal=Space Science Reviews|volume=92|pages=225–236|first2=Günter W.|bibcode=2000SSRv...92..225S}}</ref><ref>{{cite journal |doi=10.1016/j.gca.2008.03.023|title=53Mn–53Cr systematics of the early Solar System revisited|year=2008|last1=Trinquier|first1=A. |last2=Birck|last3=Allègre|last4=Göpel|last5=Ulfbeck |journal=Geochimica et Cosmochimica Acta|volume=72|pages=5146–5163|first2=J.|first3=C. |first4=C.|first5=D.|bibcode=2008GeCoA..72.5146T |issue=20}}</ref> |
|||
{{Compact periodic table}} |
|||
===Alotrop=== |
|||
{{kimia-stub}} |
|||
{|align=right |
|||
| [[Berkas:Alpha-Mn.png|thumb|x160px|Sel unit kristal Mn-α]] |
|||
| [[Berkas:Beta-Mn.png|thumb|x160px|Sel unit kristal Mn-β]] |
|||
|} |
|||
Empat [[alotropi|alotrop]] (bentuk struktural) mangan padat telah diketahui, diberi label α, β, γ dan δ, dan terjadi pada peningkatan suhu secara berturut-turut. Semuanya metalik, stabil pada tekanan standar, dan memiliki kisi kristal kubik, tetapi struktur atomnya sangat bervariasi.<ref name="Young 1975">{{cite journal |last1=Young |first1=D.A. |title=Phase diagrams of the elements |url=https://inis.iaea.org/search/search.aspx?orig_q=RN:7255152 |website=International Nuclear Information System |publisher=LNL |access-date=27 Juni 2023 |page=15 |date=1975}}</ref><ref name="Dhananjayan 1969">{{cite book |last1=Dhananjayan |first1=N. |last2=Banerjee |first2=T. |title=Crystallographic modifications of manganese and their transformation characteristics. ''Chapter 1 of:'' Structure of Electro-Deposited Manganese. |date=1969 |pages=3–28 |publisher=CSIR-NML |url=https://eprints.nmlindia.org/5609/}}</ref><ref name="Kemmitt 1973">{{cite book | last1=Kemmitt | first1=R. D. W. | last2=Peacock | first2=R. D. | title=The Chemistry of Manganese, Technetium and Rhenium. Pergamon Texts in Inorganic Chemistry. | publisher=Elsevier Science | publication-place=Saint Louis | date=1973 | isbn=978-1-4831-3806-0 | oclc=961064866 | page=778}}</ref> |
|||
'''Mangan alfa''' (Mn-α) adalah fase kesetimbangan pada suhu kamar. Ia memiliki kisi [[sistem kristal kubik|kubus berpusat-badan]] dan tidak biasa di antara logam elemental karena memiliki sel unit yang sangat kompleks, dengan 58 atom per sel (29 atom per sel unit sederhana) dalam empat jenis lokasi yang berbeda.<ref name="Young 1975" /><ref name="Bradley 1927">{{cite journal | first1=A.J. | last1=Bradley | first2=J. | last2=Thewlis | title=The crystal structure of α-manganese | journal=Proceedings of the Royal Society of London, Series A | volume=115 | issue=771 | year=1927 | issn=0950-1207 | doi=10.1098/rspa.1927.0103 | pages=456–471| bibcode=1927RSPSA.115..456B }}</ref> Ia bersifat [[paramagnetisme|paramagnetik]] pada suhu kamar dan [[antiferomagnetisme|antiferomagnetik]] pada suhu di bawah {{convert|95|K|C|sigfig=3}}.<ref name="Lawson 1994">{{cite journal | last1=Lawson | first1=A. C. | last2=Larson | first2=Allen C. | last3=Aronson | first3=M. C. | display-authors=etal | title=Magnetic and crystallographic order in α‐manganese | journal=J. Appl. Phys. | volume=76 | issue=10 | date=1994 | pages=7049–7051 | issn=0021-8979 | doi=10.1063/1.358024| bibcode=1994JAP....76.7049L }}</ref> |
|||
{|align=right |
|||
|[[Berkas:Phase diagram of manganese (1975).png|thumb|190px|Diagram fase mangan<ref name="Young 1975" />]] |
|||
|} |
|||
'''Mangan beta''' (Mn-β) terbentuk ketika dipanaskan di atas suhu transisi ({{convert|973|K|C F|sigfig=3}})<!-- Untuk transisi α-β, "Young 1975" memberi nilai sebesar 1000 K; "Kemmitt 1973" memberi nilai sebesar 700±3 C (973 K)-->. Ia memiliki struktur kubus sederhana dengan 20 atom per sel unit di dua jenis lokasi, yang sama rumitnya dengan logam elemental lainnya.<ref name="Prior 2004">{{cite journal | last1=Prior | first1=Timothy J | last2=Nguyen-Manh | first2=Duc | last3=Couper | first3=Victoria J | last4=Battle | first4=Peter D | title=Ferromagnetism in the beta-manganese structure: Fe<sub>1.5</sub>Pd<sub>0.5</sub>Mo<sub>3</sub>N | journal=Journal of Physics: Condensed Matter | volume=16 | issue=13 | date=2004 | issn=0953-8984 | doi=10.1088/0953-8984/16/13/008 | pages=2273–2281| bibcode=2004JPCM...16.2273P | s2cid=250784683 }}</ref> Ia mudah diperoleh sebagai fase metastabil pada suhu kamar melalui pendinginan cepat. Ia tidak menunjukkan [[Magnetisme|pengarahan magnetik]], akan tetap bersifat paramagnetik hingga suhu terendah yang diukur (1,1 K).<ref name="Prior 2004" /><ref name="Funahashi 1984">{{cite journal | last1=Funahashi | first1=S. | last2=Kohara | first2=T. | title=Neutron diffuse scattering in β‐manganese | journal=J. Appl. Phys. | volume=55 | issue=6 | date=1984 | issn=0021-8979 | doi=10.1063/1.333561 | pages=2048–2050| bibcode=1984JAP....55.2048F }}</ref><ref name="Duschanek 1989">{{cite journal | last1=Duschanek | first1=H. | last2=Mohn | first2=P. | last3=Schwarz | first3=K. | title=Antiferromagnetic and ferromagnetic gamma-manganese generalisation of the fixed-spin-moment method | journal=Physica B: Condensed Matter | volume=161 | issue=1–3 | year=1989 | issn=0921-4526 | doi=10.1016/0921-4526(89)90120-8 | pages=139–142}}</ref> |
|||
'''Mangan gama''' (Mn-γ) terbentuk ketika dipanaskan di atas suhu {{convert|1370|K|C F|sigfig=3}}.<!-- Untuk transisi β-γ, "Duschanek 1989" memberi nilai sebesar 1368 K; "Garlen 2015" memberi nilai sebesar 1373 K; keduanya dibulatkan menjadi 1370 K --> Ia memiliki struktur [[sistem kristal kubik|kubus berpusat-muka]] sederhana (empat atom per sel unit). Ketika didinginkan ke suhu kamar, ia akan berubah menjadi Mn-β, tetapi ia dapat distabilkan pada suhu kamar dengan memadukannya dengan setidaknya 5 persen unsur lain (seperti C, Fe, Ni, Cu, Pd atau Au), dan paduan yang distabilkan larutan ini akan terdistorsi menjadi struktur [[Sistem kristal tetragon|tetragon]] berpusat-muka.<ref name="Duschanek 1989"/><ref name="Bacon 1970">{{cite journal | last1=Bacon | first1=G E | last2=Cowlam | first2=N | title=A study of some alloys of gamma -manganese by neutron diffraction | journal=Journal of Physics C: Solid State Physics | volume=3 | issue=3 | date=1970| issn=0022-3719 | doi=10.1088/0022-3719/3/3/023 | pages=675–686| bibcode=1970JPhC....3..675B }}</ref> |
|||
'''Mangan delta''' (Mn-δ) terbentuk ketika dipanaskan di atas suhu {{convert|1406|K|C F|sigfig=3}}<!-- Untuk transisi γ-δ, "Dhananjayan 1969" mengatakan 1134 C (= kira-kira 1407 K); "Duschanek 1989" menunjukkan 1406 K; "Young 1975" menunjukkan sekitar 1400±20 K dalam diagram fase (meskipun teksnya menyatakan "mendekati 1520 K", yang tampaknya salah ketik karena cocok dengan titik lebur, bukan transisi gama-delta). --> dan stabil hingga titik lebur mangan sebesar {{convert|1519|K|C F|sigfig=3}}. Ia memiliki struktur kubus berpusat-badan (dua atom per sel unit kubus).<ref name="Dhananjayan 1969" /><ref name="Duschanek 1989" /> |
|||
==Senyawa== |
|||
[[Berkas:Chlorid manganatý.JPG|thumb|left|upright|Kristal [[mangan(II) klorida]] – warna merah muda pucat dari garam Mn(II) disebabkan oleh transisi 3d [[Reaksi spin-terlarang|spin-terlarang]].<ref>{{cite book|title=Shriver and Atkins' Inorganic Chemistry|url=https://archive.org/details/shriveratkinsino0000unse_m2r9|date=2010|publisher=Oxford University Press|isbn=978-0-19-923617-6|chapter=Ch. 20}}</ref>]] |
|||
[[Bilangan oksidasi|Keadaan oksidasi]] umum mangan adalah +2, +3, +4, +6, dan +7, meskipun semua keadaan oksidasi dari −3 hingga +7 telah diamati. Mangan dalam keadaan oksidasi +7 diwakili oleh garam dari anion permanganat MnO<sub>4</sub><sup>−</sup> yang berwarna sangat ungu. [[Kalium permanganat]] adalah sebuah [[pereaksi kimia|reagen]] laboratorium yang umum digunakan karena sifat pengoksidasinya; ia digunakan sebagai obat topikal (misalnya, dalam pengobatan penyakit ikan). Larutan kalium permanganat adalah salah satu pewarna dan fiksatif pertama yang digunakan dalam persiapan sel dan jaringan biologis untuk mikroskop elektron.<ref>{{cite journal |doi=10.1083/jcb.2.6.799 |last=Luft |first=J. H.|date=1956 |title=Permanganate – a new fixative for electron microscopy |journal=Journal of Biophysical and Biochemical Cytology |volume=2 |pages=799–802 |pmid=13398447 |issue=6 |pmc=2224005}}</ref> |
|||
Selain berbagai garam permanganat, Mn(VII) diwakili oleh turunan Mn<sub>2</sub>O<sub>7</sub> yang tidak stabil dan bersifat volatil. [[Oksihalida]] (MnO<sub>3</sub>F dan MnO<sub>3</sub>Cl) adalah [[oksidator|oksidator kuat]].<ref name="Holl" /> Contoh paling menonjol dari Mn dalam keadaan oksidasi +6 adalah anion [[manganat]] [MnO<sub>4</sub>]<sup>2-</sup> yang berwarna hijau. Garam mangan adalah zat antara dalam ekstraksi mangan dari bijihnya. Senyawa dengan keadaan oksidasi +5 agak sulit dipahami, salah satu contohnya adalah anion [[hipomanganat]] [MnO<sub>4</sub>]<sup>3-</sup> yang berwarna biru. |
|||
Senyawa dengan Mn dalam keadaan oksidasi +5 jarang dijumpai dan sering ditemui berasosiasi dengan ligan oksida (O<sup>2-</sup>) atau [[nitrida]] (N<sup>3-</sup>).<ref>{{cite journal |doi=10.1021/ar400147y|title=Reactivity of Nitrido Complexes of Ruthenium(VI), Osmium(VI), and Manganese(V) Bearing Schiff Base and Simple Anionic Ligands |year=2014 |last1=Man |first1=Wai-Lun |last2=Lam |first2=William W. Y. |last3=Lau |first3=Tai-Chu |journal=Accounts of Chemical Research |volume=47 |issue=2 |pages=427–439 |pmid=24047467 }}</ref><ref>{{cite journal |doi=10.1021/ar700039y|title=Corrolazines: New Frontiers in High-Valent Metalloporphyrinoid Stability and Reactivity |year=2007 |last1=Goldberg |first1=David P. |journal=Accounts of Chemical Research |volume=40 |issue=7 |pages=626–634 |pmid=17580977 }}</ref> |
|||
Mn(IV) agak membingungkan karena ia umum di alam tetapi jauh lebih jarang dalam kimia sintetis. Bijih Mn yang paling umum, [[pirolusit]], adalah MnO<sub>2</sub>. Ia adalah pigmen cokelat tua dari banyak [[lukisan gua]], tetapi juga merupakan bahan umum dalam baterai [[sel kering]]. Kompleks Mn(IV) telah dikenal, tetapi mereka membutuhkan ligan yang rumit. Kompleks Mn(IV)-OH merupakan zat antara dalam beberapa [[enzim]], termasuk pusat evolusi oksigen (OEC) pada tumbuhan.<ref>{{cite journal |doi=10.1021/cr4004874|title=Mn4Ca Cluster in Photosynthesis: Where and How Water is Oxidized to Dioxygen |year=2014 |last1=Yano |first1=Junko |last2=Yachandra |first2=Vittal |journal=Chemical Reviews |volume=114 |issue=8 |pages=4175–4205 |pmid=24684576 |pmc=4002066 }}</ref> |
|||
Turunan sederhana Mn<sup>+3</sup> jarang ditemukan tetapi dapat distabilkan dengan ligan basa yang sesuai. [[Mangan(III) asetat]] adalah oksidan yang berguna dalam [[sintesis organik]]. Senyawa padat mangan(III) dicirikan oleh warna ungu-merah yang kuat dan preferensi untuk koordinasi oktahedron yang terdistorsi akibat [[efek Jahn–Teller]].{{Butuh rujukan|date=Juni 2023}} |
|||
[[Berkas:KMnO4 in H2O.jpg|thumb|left|upright=0.55|Larutan berair KMnO<sub>4</sub>, mengilustrasikan Mn(VII) berwarna ungu tua seperti yang terjadi pada permanganat]] |
|||
Keadaan oksidasi yang sangat umum untuk mangan dalam larutan berair adalah +2, yang memiliki warna merah muda pucat. Banyak senyawa mangan(II) yang diketahui, seperti [[kompleks akuo logam|kompleks akuo]] yang diturunkan dari [[mangan(II) sulfat]] (MnSO<sub>4</sub>) dan [[mangan(II) klorida]] (MnCl<sub>2</sub>). Keadaan oksidasi ini juga terlihat pada mineral rodokrosit ([[mangan(II) karbonat]]). Mangan(II) umumnya eksis dengan spin tinggi, S = 5/2 keadaan dasar karena energi pasangan yang tinggi untuk mangan(II). Tidak ada transisi d–d yang diperbolehkan spin dalam mangan(II), yang menjelaskan warnanya yang redup.<ref>Rayner-Canham, Geoffrey dan Overton, Tina (2003) ''Descriptive Inorganic Chemistry'', Macmillan, hlm. 491, {{ISBN|0-7167-4620-4}}.</ref> |
|||
{| class="wikitable floatright" |
|||
|- |
|||
! colspan=2|Keadaan oksidasi mangan<ref name="Schmidt">{{cite book|title=Anorganische Chemie II.|chapter=VII. Nebengruppe |pages=100–109|first=Max|last=Schmidt|publisher=Wissenschaftsverlag|date=1968|language=de}}</ref> |
|||
|- |
|||
| 0 || [[Dimangan dekakarbonil|{{chem|Mn|2|(CO)|10}}]] |
|||
|- |
|||
| +1 || [[Metilsiklopentadienil mangan trikarbonil|{{chem|MnC|5|H|4|CH|3|(CO)|3}}]] |
|||
|- |
|||
| '''+2''' || [[Mangan(II) klorida|{{chem|MnCl|2}}]], [[Mangan(II) karbonat|{{chem|MnCO|3}}]], [[Mangan(II) oksida|{{chem|MnO}}]] |
|||
|- |
|||
| '''+3''' || [[Mangan(III) fluorida|{{chem|MnF|3}}]], [[Mangan(III) asetat|{{chem|Mn(OAc)|3}}]], [[Mangan(III) oksida|{{chem|Mn|2|O|3}}]] |
|||
|- |
|||
| '''+4''' || [[Mangan dioksida|{{chem|MnO|2}}]] |
|||
|- |
|||
| +5 || [[Kalium hipomanganat|{{chem|K|3|MnO|4}}]] |
|||
|- |
|||
| '''+6''' || [[Kalium manganat|{{chem|K|2|MnO|4}}]] |
|||
|- |
|||
| '''+7''' || [[Kalium permanganat|{{chem|KMnO|4}}]], [[Mangan heptoksida|{{chem|Mn|2|O|7}}]] |
|||
|- |
|||
|colspan=2 style="font-size: smaller; text-align: center"|Keadaan oksidasi yang umum dicetak tebal. |
|||
|} |
|||
===Senyawa organomangan=== |
|||
{{Utama|Kimia organomangan}} |
|||
Mangan membentuk berbagai macam turunan organologam, yaitu senyawa dengan ikatan Mn–C. Turunan organologam mencakup banyak contoh Mn dalam keadaan oksidasi yang lebih rendah, yaitu Mn(-III) hingga Mn(I). Bidang kimia organologam ini dinilai menarik karena Mn tidak mahal dan toksisitasnya relatif rendah.{{Butuh rujukan|date=Juni 2023}} |
|||
Minat komersial terbesar adalah "MMT", [[metilsiklopentadienil mangan trikarbonil]], yang digunakan sebagai sebuah senyawa [[Zat antiketuk|antiketuk]] yang ditambahkan pada bensin di beberapa negara. Ia memiliki Mn(I). Konsisten dengan aspek kimia Mn(II) lainnya, [[manganosena]] ({{chem2|Mn(C5H5)2}}) memiliki spin tinggi. Sebaliknya, logam tetangganya besi membentuk turunan spin rendah yang stabil di udara dalam bentuk [[ferosena]] ({{chem2|Fe(C5H5)2}}). Ketika dilakukan di bawah atmosfer [[karbon monoksida]], reduksi garam Mn(II) akan menghasilkan [[dimangan dekakarbonil]] {{chem2|Mn2(CO)10}}, sebuah padatan berwarna jingga dan volatil. Stabilitas udara dari senyawa Mn(0) ini (dan banyak turunannya) mencerminkan sifat akseptor elektron yang kuat dari karbon monoksida. Banyak [[Kompleks alkena logam transisi|kompleks alkena]] dan [[Kompleks alkuna logam transisi|kompleks alkuna]] diturunkan dari {{chem2|Mn2(CO)10}}.{{Butuh rujukan|date=Juni 2023}} |
|||
Dalam Mn(CH<sub>3</sub>)<sub>2</sub>(dmpe)<sub>2</sub>, Mn(II) memiliki spin rendah, yang kontras dengan karakter spin tinggi dari prekursornya, MnBr<sub>2</sub>(dmpe)<sub>2</sub> ([[1,2-Bis(dimetilfosfino)etana|dmpe]] = (CH<sub>3</sub>)<sub>2</sub>PCH<sub>2</sub>CH<sub>2</sub>P(CH<sub>3</sub>)<sub>2</sub>).<ref>{{cite journal |doi=10.1021/ja00360a054|title=Hydrido, alkyl, and ethylene 1,2-bis(dimethylphosphino)ethane complexes of manganese and the crystal structures of MnBr2(dmpe)2, [Mn(AlH4)(dmpe)2]2 and MnMe2(dmpe)2 |year=1983 |last1=Girolami |first1=Gregory S. |last2=Wilkinson |first2=Geoffrey |last3=Thornton-Pett |first3=Mark |last4=Hursthouse |first4=Michael B. |journal=Journal of the American Chemical Society |volume=105 |issue=22 |pages=6752–6753 }}</ref> Turunan polialkil dan poliaril dari mangan sering berada pada keadaan oksidasi yang lebih tinggi, mencerminkan sifat pelepasan elektron dari ligan alkil dan aril. Salah satu contohnya adalah [Mn(CH<sub>3</sub>)<sub>6</sub>]<sup>2-</sup>.{{Butuh rujukan|date=Juni 2023}} |
|||
==Sejarah== |
|||
Asal usul nama mangan memang kompleks. Pada zaman kuno, dua mineral hitam diidentifikasi dari wilayah [[Magnetes]] (antara [[Magnesia Kuno|Magnesia]], yang terletak di Yunani modern, atau [[Magnesia ad Sipylum]], yang terletak di Turki modern).<ref name="LanguageHAt">{{cite web |last1=languagehat |title=MAGNET. |url=http://languagehat.com/magnet/ |website=languagehat.com |access-date=27 Juni 2023 |language=en |date=28 Mei 2005}}</ref> Keduanya disebut ''magnes'' dari tempat asalnya, tetapi dianggap berbeda jenis kelamin. ''Magnes'' jantan dapat menarik besi, dan bijih besi sekarang dikenal sebagai [[batu magnet]] atau [[magnetit]], dan yang mungkin memberi kita istilah [[magnet]]. Bijih ''magnes'' betina tidak menarik besi, tetapi digunakan untuk menghilangkan warna kaca. ''Magnes'' betina ini kemudian disebut ''magnesia'', yang sekarang dikenal di zaman modern sebagai [[pirolusit]] atau [[mangan dioksida]].{{Butuh rujukan|date=Juni 2023}} Baik mineral maupun mangan elemental ini tidak bersifat magnetis. Pada abad ke-16, mangan dioksida disebut ''manganesum'' (perhatikan adanya dua N, bukan satu) oleh pembuat kaca, mungkin sebagai korupsi dan gabungan dari dua kata, karena ahli alkimia dan pembuat kaca akhirnya harus membedakan ''magnesia nigra'' (bijih hitam) dari ''magnesia alba'' (bijih putih, juga dari Magnesia, yang juga berguna dalam pembuatan kaca). [[Michele Mercati]] menyebut magnesia nigra sebagai ''manganesa'', dan akhirnya logam yang diisolasi darinya dikenal sebagai ''manganese'' (bahasa Indonesia: ''Mangan''). Nama ''magnesia'' akhirnya digunakan untuk merujuk hanya pada [[magnesium oksida|magnesia alba]] (magnesium oksida) putih, yang memberi nama [[magnesium]] untuk unsur bebasnya ketika diisolasi beberapa waktu kemudian.<ref>{{cite web|last=Calvert|first=J. B.|url=http://mysite.du.edu/~jcalvert/phys/chromang.htm|title=Chromium and Manganese|access-date=27 Juni 2023|date=24 Januari 2003|url-status=dead|archive-url=https://web.archive.org/web/20161231161307/http://mysite.du.edu/~jcalvert/phys/chromang.htm|archive-date=31 Desember 2016}}</ref> |
|||
[[Berkas:Lascaux painting.jpg|thumb| left |alt=Sebuah gambar banteng menghadap ke kiri, berwarna hitam, di dinding gua |Beberapa lukisan gua di [[Gua Lascaux|Lascaux]], [[Prancis]], menggunakan pigmen berbasis mangan.<ref name="Lascaux">{{cite journal|doi=10.1088/0957-0233/14/9/310|title=Analysis of rock art painting and technology of Palaeolithic painters|date=2003|last=Chalmin|first=Emilie |author2=Menu, Michel |author3=Vignaud, Colette|journal=Measurement Science and Technology|volume=14|pages=1590–1597|issue=9|s2cid=250842390 }}</ref>]] |
|||
[[Mangan dioksida]] yang melimpah di alam telah lama digunakan sebagai pigmen. Lukisan gua di [[Gargas, Haute-Garonne|Gargas]] yang berusia 30.000 hingga 24.000 tahun terbuat dari mineral berupa pigmen MnO<sub>2</sub>.<ref>{{cite journal|doi=10.1007/s00339-006-3510-7|title=Minerals discovered in paleolithic black pigments by transmission electron microscopy and micro-X-ray absorption near-edge structure|date=2006|last1=Chalmin|first1=E.|last2=Vignaud|first2=C. |last3=Salomon|first3=H.|last4=Farges|first4=F.|last5=Susini|first5=J. |last6= Menu|first6=M.|journal=Applied Physics A|volume=83 |pages=213–218|issue=12|bibcode=2006ApPhA..83..213C|hdl=2268/67458|s2cid=9221234|url=http://orbi.ulg.ac.be/bitstream/2268/67458/1/fulltext.pdf}}</ref> |
|||
Senyawa mangan digunakan oleh pembuat kaca di Mesir dan Romawi, baik untuk menambah, atau menghilangkan, warna dari kaca.<ref>{{cite journal |doi=10.1126/science.133.3467.1824|date=1961|last=Sayre|first=E. V.|author2=Smith, R. W.|title=Compositional Categories of Ancient Glass |volume=133|issue=3467|pages=1824–1826|journal=Science|pmid=17818999|bibcode=1961Sci...133.1824S|s2cid=25198686}}</ref> Penggunaannya sebagai "sabun pembuat kaca" berlanjut hingga [[Abad Pertengahan]] hingga zaman modern dan terbukti dalam kaca abad ke-14 dari [[Venesia]].<ref name="ItGlass" /> |
|||
[[Berkas:Gahn Johan Gottlieb.jpg|thumb|upright|Orang yang pertama kali mengisolasi mangan biasanya dikreditkan kepada [[Johan Gottlieb Gahn|Johan G. Gahn]].]] |
|||
Karena digunakan dalam pembuatan kaca, mangan dioksida tersedia untuk percobaan oleh beberapa ahli alkimia, kimiawan pertama. [[Ignatius Gottfried Kaim|Ignatius G. Kaim]] (1770) dan [[Johann Rudolf Glauber|Johann R. Glauber]] (abad ke-17) menemukan bahwa mangan dioksida dapat diubah menjadi [[permanganat]], sebuah reagen laboratorium yang berguna.<ref>{{cite journal|journal=Centaurus|volume=19|issue=4|title=The Discovery of an Element|first=E.|last=Rancke-Madsen|doi=10.1111/j.1600-0498.1975.tb00329.x|pages=299–313|date=1975|bibcode=1975Cent...19..299R}}</ref> Pada pertengahan abad ke-18, kimiawan Swedia [[Carl Wilhelm Scheele|Carl W. Scheele]] menggunakan mangan dioksida untuk menghasilkan [[klorin]]. Pertama, [[asam klorida]], atau campuran [[asam sulfat]] encer dan [[natrium klorida]] dibuat untuk bereaksi dengan mangan dioksida, dan kemudian asam klorida dari [[proses Leblanc]] digunakan, dan mangan dioksida didaur ulang melalui [[proses Weldon]]. Produksi zat [[pemutih]] klorin dan [[hipoklorit]] merupakan konsumen bijih mangan yang besar.{{Butuh rujukan|date=Juni 2023}} |
|||
Scheele dan yang lainnya menyadari bahwa pirolusit (bentuk mineral mangan dioksida) mengandung sebuah unsur baru. [[Johan Gottlieb Gahn|Johan G. Gahn]] adalah orang pertama yang mengisolasi sampel logam mangan yang tidak murni pada tahun 1774, yang dilakukannya dengan [[Redoks|mereduksi]] mangan dioksida dengan [[karbon]].{{Butuh rujukan|date=Juni 2023}} |
|||
Kandungan mangan dari beberapa bijih besi yang digunakan di Yunani menimbulkan spekulasi bahwa baja yang dihasilkan dari bijih tersebut mengandung mangan tambahan, membuat baja [[Sparta]] sangatlah keras.<ref>{{cite journal|doi=10.1002/ajim.20524|date=2007|title=From lead to manganese through mercury: mythology, science, and lessons for prevention|volume=50|issue=11|pages=779–787 |journal=American Journal of Industrial Medicine|pmid=17918211|last1=Alessio|first1=L.|last2=Campagna|first2=M.|last3=Lucchini|first3=R.}}</ref> Sekitar awal abad ke-19, mangan digunakan dalam pembuatan baja dan beberapa paten diberikan. Pada tahun 1816, didokumentasikan bahwa paduan besi dengan mangan lebih keras tetapi tidak lebih rapuh. Pada tahun 1837, akademisi Inggris [[James Couper (akademisi)|James Couper]] mencatat hubungan antara paparan berat mangan pada penambang dan bentuk [[penyakit Parkinson]].<ref name="Couper 1837 41–42" /> Pada tahun 1912, paten Amerika Serikat diberikan untuk melindungi senjata api dari karat dan korosi dengan pelapisan konversi elektrokimia mangan fosfat, dan proses tersebut telah digunakan secara luas sejak saat itu.<ref>{{cite book|title=Production of Manganese Ferroalloys|publisher=Tapir Academic Press |date=2007|isbn=978-82-519-2191-6|chapter=History of omanganese|pages=11–12|author=Olsen, Sverre E.|author2=Tangstad, Merete |author3=Lindstad, Tor}}</ref> |
|||
Penemuan [[sel Leclanché]] pada tahun 1866 dan perbaikan baterai selanjutnya yang mengandung mangan dioksida sebagai [[depolarisator]] katodik meningkatkan permintaan mangan dioksida. Hingga pengembangan baterai dengan [[Baterai nikel–kadmium|nikel–kadmium]] dan litium, sebagian besar baterai mengandung mangan. [[Baterai seng–karbon]] dan [[baterai alkalin]] biasanya menggunakan mangan dioksida yang diproduksi secara industri karena mangan dioksida alami mengandung kotoran. Pada abad ke-20, mangan dioksida banyak digunakan sebagai katodik untuk [[baterai kering]] sekali pakai komersial baik tipe standar (seng–karbon) maupun alkalin.<ref name="ChiuZMnO2">{{cite journal|doi=10.1002/ciuz.19800140502|title=Moderne Verfahren der Großchemie: Braunstein |date=1980|last=Preisler|first=Eberhard|journal=Chemie in unserer Zeit|language=de|volume=14|pages=137–148|issue=5}}</ref> |
|||
==Keterjadian== |
|||
{{Lihat pula|Kategori:Mineral mangan}} |
|||
Mangan menyusun sekitar 1000 [[Notasi bagian per#Bagian per juta|ppm]] (0,1%) [[kerak Bumi]], menjadi unsur kerak Bumi yang paling melimpah ke-12.<ref name="Emsley2001">{{cite book|title=Nature's Building Blocks: An A-Z Guide to the Elements|last=Emsley|first=John|publisher=Oxford University Press|date=2001|location=Oxford, UK|isbn=978-0-19-850340-8|chapter=Manganese|pages=[https://archive.org/details/naturesbuildingb0000emsl/page/249 249–253]|chapter-url=https://books.google.com/books?id=j-Xu07p3cKwC|url=https://archive.org/details/naturesbuildingb0000emsl/page/249}}</ref> Tanah mengandung 7–9000 ppm mangan dengan rata-rata 440 ppm.<ref name="Emsley2001" /> Atmosfer mengandung 0,01 μg/m<sup>3</sup>.<ref name="Emsley2001" /> Mangan terjadi terutama sebagai [[pirolusit]] ([[mangan dioksida|MnO<sub>2</sub>]]), [[braunit]] (Mn<sup>2+</sup>Mn<sup>3+</sup><sub>6</sub>)SiO<sub>12</sub>),<ref>{{cite journal|pages=65–71 |journal=Contributions to Mineralogy and Petrology|title=Geochemistry of braunite and associated phases in metamorphosed non-calcareous manganese ores of India|url=https://archive.org/details/sim_contributions-to-mineralogy-and-petrology_1984-08_87_1/page/n66 |first=P. K.|last=Bhattacharyya|author2=Dasgupta, Somnath |author3=Fukuoka, M. |author4=Roy Supriya |doi=10.1007/BF00371403|date=1984|volume=87|issue=1|bibcode=1984CoMP...87...65B|s2cid=129495326}}</ref> [[psilomelan]] {{chem2|(Ba,H2O)2Mn5O10}}, dan pada tingkat yang lebih rendah sebagai [[rodokrosit]] ([[mangan(II) karbonat|MnCO<sub>3</sub>]]). |
|||
{|class="wikitable" |
|||
|[[Berkas:ManganeseOreUSGOV.jpg|center|120px]] |
|||
|[[Berkas:Mineraly.sk - psilomelan.jpg|center|140px]] |
|||
|[[Berkas:Spiegeleisen.jpg|center|150px]] |
|||
|[[Berkas:Dendrites01.jpg|center|130px]] |
|||
|[[Berkas:The Searchlight Rhodochrosite Crystal.jpg|center|140px]] |
|||
|- |
|||
|Bijih mangan |
|||
|Psilomelan (bijih mangan) |
|||
|[[Spiegeleisen]] adalah sebuah paduan besi dengan kandungan mangan sekitar 15% |
|||
|Dendrit mangan oksida pada batu gamping dari [[Solnhofen]], Jerman – sejenis [[pseudofosil]]. Skala dalam mm |
|||
|Mineral rodokrosit ([[mangan(II) karbonat]]) |
|||
|} |
|||
[[Berkas:World Manganese Production 2006.svg|thumb|upright=1.6|Persentase keluaran mangan pada tahun 2006 menurut negara<ref name="USGSMCS2009">USGS Mineral Commodity Summaries 2009</ref>]] |
|||
Bijih mangan yang paling penting adalah pirolusit (MnO<sub>2</sub>). Bijih mangan lain yang penting secara ekonomi biasanya menunjukkan hubungan spasial yang dekat dengan bijih besi, seperti [[sfalerit]].<ref name="Holl" /><ref>{{Cite journal|last1=Cook|first1=Nigel J.|last2=Ciobanu|first2=Cristiana L.|last3=Pring|first3=Allan|last4=Skinner|first4=William|last5=Shimizu|first5=Masaaki|last6=Danyushevsky|first6=Leonid|last7=Saini-Eidukat|first7=Bernhardt|last8=Melcher|first8=Frank|date=2009|title=Trace and minor elements in sphalerite: A LA-ICPMS study|url=https://linkinghub.elsevier.com/retrieve/pii/S0016703709003263|journal=Geochimica et Cosmochimica Acta|language=en|volume=73|issue=16|pages=4761–4791|doi=10.1016/j.gca.2009.05.045|bibcode=2009GeCoA..73.4761C}}</ref> Sumber daya berbasis lahan berjumlah besar tetapi didistribusikan secara tidak teratur. Sekitar 80% dari sumber mangan dunia yang diketahui terdapat di Afrika Selatan; endapan mangan penting lainnya terdapat di Ukraina, Australia, India, Tiongkok, [[Gabon]], dan Brasil.<ref name="USGSMCS2009" /> Menurut perkiraan tahun 1978, [[dasar laut]]an memiliki 500 miliar ton [[nodul mangan]].<ref>{{cite journal|doi=10.1016/j.micron.2008.10.005|pages=350–358|date=2009|title=Manganese/polymetallic nodules: micro-structural characterization of exolithobiontic- and endolithobiontic microbial biofilms by scanning electron microscopy|volume=40 |issue=3|pmid=19027306|journal=Micron |author1=Wang, X|author2=Schröder, HC|author3=Wiens, M|author4=Schlossmacher, U|author5=Müller, WEG}}</ref> Upaya untuk menemukan metode pemanenan nodul mangan yang layak secara ekonomi ditinggalkan pada tahun 1970-an.<ref>{{cite book |title=Manganese Nodules: Dimensions and Perspectives|journal=Marine Geology|volume=41|issue=3–4|pages=343|publisher=Springer|date=1978|isbn=978-90-277-0500-6|author=United Nations|bibcode=1981MGeol..41..343C|doi=10.1016/0025-3227(81)90092-X|oclc=4515098|series=Natural Resources Forum Library}}</ref> |
|||
Di Afrika Selatan, endapan yang paling teridentifikasi terletak di dekat [[Hotazel]] di [[Northern Cape|Provinsi Northern Cape]] ([[ladang mangan Kalahari]]), dengan perkiraan tahun 2011 sebesar 15 miliar ton. Pada tahun 2011, Afrika Selatan menghasilkan 3,4 juta ton, melampaui semua negara lain.<ref name="Mbendi">{{cite web |url=http://www.mbendi.com/indy/ming/mang/af/sa/p0005.htm |title=Manganese Mining in South Africa – Overview |publisher=MBendi Information Services |access-date=27 Juni 2023 |url-status=dead |archive-url=https://web.archive.org/web/20160205194737/http://www.mbendi.com/indy/ming/mang/af/sa/p0005.htm |archive-date=5 Februari 2016}}</ref> |
|||
Mangan ditambang terutama di Afrika Selatan, Australia, Tiongkok, Gabon, Brasil, India, Kazakhstan, Ghana, Ukraina, dan Malaysia.<ref>{{Cite journal|doi = 10.1007/s11837-018-2769-4|title = Review of Manganese Processing for Production of TRIP/TWIP Steels, Part 1: Current Practice and Processing Fundamentals|journal = JOM |volume = 70|issue = 5|pages = 680–690|year = 2018|last1 = Elliott|first1 = R|last2 = Coley|first2 = K|last3 = Mostaghel|first3 = S|last4 = Barati|first4 = M|bibcode = 2018JOM....70e.680E|s2cid = 139950857}}</ref> |
|||
==Produksi== |
|||
Untuk produksi [[feromangan]], bijih mangan dicampur dengan bijih besi dan karbon, dan kemudian direduksi baik dalam tanur tiup atau tanur busur listrik.<ref name="IndMin">{{cite book|title=Industrial Minerals & Rocks: Commodities, Markets, and Uses |edition=7|publisher=SME|date=2006|isbn=978-0-87335-233-8|chapter=Manganese|first=L. A.|last=Corathers |author2=Machamer, J. F. |chapter-url=https://books.google.com/books?id=zNicdkuulE4C&pg=PA631|pages=631–636}}</ref> Feromangan yang dihasilkan memiliki kandungan mangan 30 hingga 80%.<ref name="Holl" /> Mangan murni yang digunakan untuk produksi paduan bebas besi diproduksi dengan [[pelindian (metalurgi)|melindi]] bijih mangan dengan [[asam sulfat]] dan proses [[pengekstrakan elektrolisis|elektrodeposisi]] berikutnya.<ref name="hydrometI">{{cite journal|doi=10.1016/j.hydromet.2007.08.010 |title=Manganese metallurgy review. Part I: Leaching of ores/secondary materials and recovery of electrolytic/chemical manganese dioxide|date=2007|last=Zhang|first=Wensheng|author2=Cheng, Chu Yong|journal=Hydrometallurgy|volume=89 |pages=137–159|issue=3–4}}</ref> |
|||
[[Berkas:Manganese Process Flow Diagram.jpg|thumb|upright=1.75|alt=Berisi reaksi dan suhu, serta menunjukkan proses lanjutan seperti penukar panas dan proses penggilingan.|Diagram alir proses untuk sirkuit pemurnian mangan.]] |
|||
Proses ekstraksi yang lebih progresif melibatkan pereduksian bijih mangan (kadar rendah) secara langsung melalui [[pelindian timbunan]]. Ini dilakukan dengan [[perkolasi|memerkolasi]] gas alam melalui dasar tumpukan; gas alam menyediakan panas (perlu setidaknya 850 °C) dan zat pereduksi (karbon monoksida). Ini akan mereduksi semua bijih mangan menjadi mangan oksida (MnO), yang merupakan bentuk yang dapat dilindi. Bijih kemudian bergerak melalui sebuah sirkuit [[Alat giling|penggilingan]] untuk mengurangi ukuran partikel bijih menjadi antara 150 dan 250 μm, meningkatkan luas permukaan untuk membantu pelindian. Bijih tersebut kemudian ditambahkan ke dalam tangki pelindian asam sulfat dan [[Besi(II)|ion fero]] (Fe<sup>2+</sup>) dengan perbandingan 1,6:1. Besi kemudian bereaksi dengan [[mangan dioksida]] (MnO<sub>2</sub>) untuk membentuk [[besi oksida|besi hidroksida]] (FeO(OH)) dan mangan elemental (Mn).{{Butuh rujukan|date=Juni 2023}} |
|||
Proses ini menghasilkan sekitar 92% pemulihan mangan. Untuk pemurnian lebih lanjut, mangan kemudian dapat dikirim ke sebuah fasilitas elektrodeposisi.<ref name="ManganeseRecovery">{{cite web|url=http://www.americanmanganeseinc.com/wp-content/uploads/2011/08/American-Manganese-Phase-II-August-19-2010-Final-Report-Internet-Version-V2.pdf|title=The Recovery of Manganese from low grade resources: bench scale metallurgical test program completed|date=2010|author=Chow, Norman|author2=Nacu, Anca|author3=Warkentin, Doug|author4=Aksenov, Igor|author5=Teh, Hoe|name-list-style=amp|publisher=Kemetco Research Inc.|url-status=dead|archive-url=https://web.archive.org/web/20120202065633/http://www.americanmanganeseinc.com/wp-content/uploads/2011/08/American-Manganese-Phase-II-August-19-2010-Final-Report-Internet-Version-V2.pdf|archive-date=2 Februari 2012}}</ref> |
|||
Pada tahun 1972, [[Proyek Azorian]] [[Badan Intelijen Pusat|CIA]], melalui miliarder [[Howard Hughes]], menugaskan kapal ''[[GSF Explorer|Hughes Glomar Explorer]]'' dengan "cerita sampul" memanen nodul mangan dari dasar laut.<ref>{{Cite news|url=https://www.bbc.com/news/science-environment-42994812|title=The CIA secret on the ocean floor|date=19 Februari 2018|work=BBC News|access-date=27 Juni 2023|language=en-GB}}</ref> Hal itu memicu kesibukan untuk mengumpulkan nodul mangan, yang sebenarnya tidak praktis. Misi sebenarnya dari ''Hughes Glomar Explorer'' adalah mengangkat kapal selam [[Uni Soviet|Soviet]] yang tenggelam, ''[[Kapal selam Soviet K-129 (1960)|K-129]]'', dengan tujuan mengambil buku kode Soviet.<ref name="azorian">{{cite web |url=http://www2.gwu.edu/~nsarchiv/nukevault/ebb305/index.htm |title=Project Azorian: The CIA's Declassified History of the Glomar Explorer |publisher=National Security Archive at George Washington University |date=12 Februari 2010 |access-date=27 Juni 2023}}</ref> |
|||
Sumber daya mangan yang melimpah berupa nodul mangan yang ditemukan di [[dasar laut]].<ref>{{cite book |last1=Hein |first1=James R. |title=Encyclopedia of Marine Geosciences - Manganese Nodules |date=Januari 2016 |publisher=Springer |pages=408–412 |url=https://www.researchgate.net/publication/306107551 |access-date=27 Juni 2023}}</ref><ref>{{cite journal |last1=Hoseinpour |first1=Vahid |last2=Ghaemi |first2=Nasser |title=Green synthesis of manganese nanoparticles: Applications and future perspective–A review |journal=Journal of Photochemistry and Photobiology B: Biology |date=1 Desember 2018 |volume=189 |pages=234–243 |doi=10.1016/j.jphotobiol.2018.10.022 |pmid=30412855 |s2cid=53248245 |url=https://www.sciencedirect.com/science/article/abs/pii/S101113441830959X |access-date=27 Juni 2023}}</ref> Nodul-nodul ini, yang terdiri dari 29% mangan,<ref>{{cite web |last1=International Seabed Authority |title=Polymetallic Nodules |url=https://isa.org.jm/files/files/documents/eng7.pdf |website=isa.org |publisher=International Seabed Authority |access-date=27 Juni 2023}}</ref> terletak di sepanjang dasar laut dan dampak potensial penambangan nodul-nodul ini sedang diteliti. Dampak lingkungan fisik, kimia, dan biologis dapat terjadi karena penambangan nodul ini mengganggu dasar laut dan menyebabkan terbentuknya gumpalan sedimen. Suspensi ini meliputi logam dan nutrisi anorganik, yang dapat menyebabkan kontaminasi perairan dekat dasar dari senyawa beracun terlarut. Nodul mangan juga merupakan tempat merumput, ruang hidup, dan perlindungan untuk sistem endo- dan epifauna. Ketika nodul ini dihilangkan, sistem ini secara langsung akan terpengaruh. Secara keseluruhan, hal ini dapat menyebabkan spesies meninggalkan area tersebut atau mati total.<ref>{{Cite journal|last1=Oebius|first1=Horst U|last2=Becker|first2=Hermann J|last3=Rolinski|first3=Susanne|last4=Jankowski|first4=Jacek A|date=Januari 2001|title=Parametrization and evaluation of marine environmental impacts produced by deep-sea manganese nodule mining|url=http://dx.doi.org/10.1016/s0967-0645(01)00052-2|journal=Deep Sea Research Part II: Topical Studies in Oceanography|volume=48|issue=17–18|pages=3453–3467|doi=10.1016/s0967-0645(01)00052-2|bibcode=2001DSRII..48.3453O|issn=0967-0645}}</ref> Sebelum dimulainya penambangan itu sendiri, penelitian sedang dilakukan oleh badan-badan afiliasi [[Perserikatan Bangsa-Bangsa]] dan perusahaan yang disponsori negara dalam upaya untuk memahami sepenuhnya [[Masalah lingkungan|dampak lingkungan]] dengan harapan dapat mengurangi dampak tersebut.<ref>{{cite journal |last1=Thompson |first1=Kirsten F. |last2=Miller |first2=Kathryn A. |last3=Currie |first3=Duncan |last4=Johnston |first4=Paul |last5=Santillo |first5=David |title=Seabed Mining and Approaches to Governance of the Deep Seabed |journal=Frontiers in Marine Science |date=2018 |volume=5 |doi=10.3389/fmars.2018.00480 |s2cid=54465407 |doi-access=free }}</ref> |
|||
===Lingkungan lautan=== |
|||
Banyak unsur renik di lautan berasal dari partikel hidrotermal yang kaya logam dari ventilasi hidrotermal.<ref name="Ray-2017">{{Cite journal|last1=Ray|first1=Durbar|last2=Babu|first2=E. V. S. S. K.|last3=Surya Prakash|first3=L.|date=1 Januari 2017|title=Nature of Suspended Particles in Hydrothermal Plume at 3°40'N Carlsberg Ridge:A Comparison with Deep Oceanic Suspended Matter|journal=Current Science|volume=112|issue=1|pages=139|doi=10.18520/cs/v112/i01/139-146|issn=0011-3891|doi-access=free}}</ref> Mangan terlarut (dMn) ditemukan di seluruh lautan dunia, 90% di antaranya berasal dari lubang hidrotermal.<ref name="Hernroth-2020">{{Cite journal|last1=Hernroth|first1=Bodil|last2=Tassidis|first2=Helena|last3=Baden|first3=Susanne P.|date=Maret 2020|title=Immunosuppression of aquatic organisms exposed to elevated levels of manganese: From global to molecular perspective|url=http://dx.doi.org/10.1016/j.dci.2019.103536|journal=Developmental & Comparative Immunology|volume=104|pages=103536|doi=10.1016/j.dci.2019.103536|pmid=31705914|s2cid=207935992|issn=0145-305X}}</ref> Partikulat Mn berkembang dalam gumpalan apung di atas sumber ventilasi aktif, sedangkan dMn berperilaku secara konservatif.<ref name="Ray-2017" /> Konsentrasi Mn bervariasi antara kolom air laut. Di permukaan, dMn terangkat karena masukan dari sumber eksternal seperti sungai, debu, dan sedimen landas. Sedimen pesisir biasanya memiliki konsentrasi Mn yang lebih rendah, tetapi dapat meningkat akibat pembuangan antropogenik dari industri seperti pertambangan dan pabrik baja, yang masuk ke laut dari input sungai. Konsentrasi dMn permukaan juga dapat ditingkatkan secara biologis melalui fotosintesis dan secara fisik dari [[pembalikan massa air]] pantai dan arus permukaan yang digerakkan oleh angin. Siklus internal seperti fotoreduksi dari radiasi UV juga dapat meningkatkan level dengan mempercepat disolusi Mn-oksida dan pemulungan oksidatif, mencegah Mn tenggelam ke perairan yang lebih dalam.<ref name="Sim-2019">{{Cite journal|last1=Sim|first1=Nari|last2=Orians|first2=Kristin J.|date=Oktober 2019|title=Annual variability of dissolved manganese in Northeast Pacific along Line-P: 2010–2013|url=http://dx.doi.org/10.1016/j.marchem.2019.103702|journal=Marine Chemistry|volume=216|pages=103702|doi=10.1016/j.marchem.2019.103702|s2cid=203151735|issn=0304-4203}}</ref> Tingkat yang lebih tinggi di pertengahan kedalaman dapat terjadi di dekat pegunungan tengah laut dan ventilasi hidrotermal. Ventilasi hidrotermal melepaskan cairan yang diperkaya dMn ke dalam air. dMn kemudian dapat melakukan perjalanan hingga 4.000 km karena adanya kapsul mikroba, mencegah pertukaran dengan partikel, menurunkan tingkat penenggelaman. Konsentrasi Mn terlarut bahkan lebih tinggi ketika kadar oksigen rendah. Secara keseluruhan, konsentrasi dMn biasanya lebih tinggi di wilayah pesisir dan akan menurun saat bergerak ke lepas pantai.<ref name="Sim-2019" /> |
|||
===Tanah=== |
|||
Mangan terjadi di tanah dalam tiga keadaan oksidasi: kation divalen, Mn<sup>2+</sup> serta sebagai oksida hitam kecokelatan dan hidroksida yang mengandung Mn(III,IV), seperti MnOOH dan MnO<sub>2</sub>. Kondisi pH tanah dan oksidasi-reduksi akan memengaruhi yang mana dari ketiga bentuk Mn ini yang dominan dalam tanah tertentu. Pada pH kurang dari 6 atau dalam kondisi anaerobik, Mn(II) mendominasi, sedangkan pada kondisi yang lebih basa dan aerobik, Mn(III,IV) oksida dan hidroksida mendominasi. Efek keasaman tanah dan keadaan aerasi pada bentuk Mn ini dapat dimodifikasi atau dikendalikan oleh aktivitas mikroba. Respirasi mikroba dapat menyebabkan oksidasi Mn<sup>2+</sup> menjadi mangan oksida, dan dapat menyebabkan reduksi oksida tersebut menjadi kation divalen.<ref>{{Cite book|last1=Bartlett|first1=Richmond|title=Chemical Processes in Soils|last2=Ross|first2=Donald|publisher=Soil Science Society of America|year=2005|editor-last=Tabatabai|editor-first=M.A.|series=SSSA Book Series, no. 8|location=Madison, Wisconsin|pages=461–487|chapter=Chemistry of Redox Processes in Soils|lccn=2005924447|editor-last2=Sparks|editor-first2=D.L.}}</ref> |
|||
Oksida Mn(III,IV) terdapat sebagai noda hitam kecokelatan dan nodul kecil pada partikel pasir, lanau, dan lempung. Lapisan permukaan pada partikel tanah lainnya ini memiliki luas permukaan yang tinggi dan membawa muatan negatif. Sisi bermuatan dapat menyerap dan mempertahankan berbagai kation, terutama logam berat (misalnya Cr<sup>3+</sup>, Cu<sup>2+</sup>, Zn<sup>2+</sup>, dan Pb<sup>2+</sup>). Selain itu, oksida tersebut dapat menyerap asam organik dan senyawa lainnya. Adsorpsi logam dan senyawa organik kemudian dapat menyebabkannya teroksidasi sedangkan oksida Mn(III,IV) direduksi menjadi Mn<sup>2+</sup> (misalnya Cr<sup>3+</sup> menjadi Cr(VI) dan hidrokuinon tidak berwarna menjadi polimer kuinon berwarna teh).<ref>{{Cite book|last1=Dixon|first1=Joe B.|title=Soil Mineralogy with Environmental Applications|last2=White|first2=G. Norman|publisher=Soil Science Society of America|year=2002|editor-last=Dixon|editor-first=J.B.|series=SSSA Book Series no. 7|location=Madison, Wisconsin|pages=367–386|chapter=Manganese Oxides|lccn=2002100258|editor-last2=Schulze|editor-first2=D.G.}}</ref> |
|||
==Aplikasi== |
|||
Mangan tidak memiliki pengganti yang memuaskan dalam aplikasi utamanya dalam metalurgi.<ref name="USGSMCS2009" /> Dalam aplikasi kecil (misalnya pemfosfatan mangan), [[seng]] dan kadang-kadang [[vanadium]] adalah pengganti yang layak. |
|||
===Baja=== |
|||
[[Berkas:M1917helmet.jpg|thumb|[[Helm tempur]] M1917 A.S., sebuah varian dari [[helm Brodie]], terbuat dari paduan mangan [[mangaloi|baja Hadfield]].]] |
|||
Mangan sangat penting untuk [[pembuatan baja|produksi baja]] dan besi berdasarkan sifat pengikat [[belerang]], [[baja terdeoksidasi|deoksidasi]], dan [[logam paduan|pemaduan]]nya, seperti yang pertama kali diakui oleh ahli metalurgi Inggris [[Robert Forester Mushet|Robert F. Mushet]] (1811–1891) yang, pada tahun 1856, memperkenalkan unsur tersebut, dalam bentuk [[spiegeleisen]], menjadi baja untuk tujuan khusus untuk menghilangkan kelebihan oksigen, belerang, dan fosforus terlarut untuk meningkatkan kelenturannya. [[Pembuatan baja]],<ref>{{cite book|isbn=978-0-87170-858-8|pages=[https://archive.org/details/steelmetallurgyf0000verh/page/56 56]–57|first=John D. |last=Verhoeven |date=2007 |publisher=ASM International |location=Materials Park, Ohio |title=Steel metallurgy for the non-metallurgist|url=https://archive.org/details/steelmetallurgyf0000verh}}</ref> termasuk komponen pembuatan besinya, telah menyumbang sebagian besar permintaan mangan, saat ini berkisar antara 85% sampai 90% dari total permintaan.<ref name="hydrometI" /> Mangan adalah komponen utama dari [[baja nirkarat]] berbiaya rendah.<ref name="MangUSGS2006">Manganese USGS 2006</ref><ref>{{cite journal |doi=10.1007/BF02648339 |title=Mechanism of work hardening in Hadfield manganese steel |date=1981 |last1=Dastur|first1=Y. N. |journal=Metallurgical Transactions A|volume=12|pages=749–759|last2=Leslie|first2=W. C.|issue=5|bibcode=1981MTA....12..749D|s2cid=136550117}}</ref> Seringkali feromangan (biasanya sekitar 80% mangan) menjadi zat antara dalam proses modern. |
|||
Sejumlah kecil mangan dapat meningkatkan kemampuan kerja baja pada suhu tinggi dengan membentuk sulfida dengan titik lebur tinggi dan mencegah pembentukan [[besi sulfida]] cair pada batas butir. Jika kandungan mangan mencapai 4%, kegetasan baja menjadi ciri yang dominan. Penggetasan akan menurun pada konsentrasi mangan yang lebih tinggi dan mencapai tingkat yang dapat diterima pada 8%. Baja yang mengandung 8 hingga 15% mangan memiliki [[kekuatan tarik]] yang tinggi hingga 863 M[[Pascal (satuan)|Pa]].<ref>{{cite book|isbn=978-1-4086-2616-0 |pages=351–352|title=Iron and Steel|first=John Henry |last=Stansbie|publisher=Read Books|url=https://books.google.com/books?id=FyogLqUxW1cC&pg=PA351 |date=2007}}</ref><ref>{{cite book|isbn=978-0-07-136076-0|pages=585–587|last=Brady|first=George S.|author2=Clauser, Henry R. |author3=Vaccari. John A. |date=2002|publisher=McGraw-Hill|location=New York, NY|title=Materials Handbook: an encyclopedia for managers, technical professionals, purchasing and production managers, technicians, and supervisors|url=https://books.google.com/books?id=vIhvSQLhhMEC&pg=PA585}}</ref> Baja dengan mangan 12% ditemukan pada tahun 1882 oleh [[Robert Hadfield]] dan masih dikenal sebagai [[mangaloi|baja Hadfield (mangaloi)]]. Baja ini digunakan untuk [[Helm Brodie|helm baja]] militer Britania Raya dan kemudian oleh militer Amerika Serikat.<ref>{{cite journal|title=Sir Robert Abbott Hadfield F.R.S. (1858–1940), and the Discovery of Manganese Steel Geoffrey Tweedale|journal=Notes and Records of the Royal Society of London|volume=40|issue=1 |date=1985|pages=63–74|doi=10.1098/rsnr.1985.0004|first=Geoffrey|last=Tweedale|jstor=531536|doi-access=free}}</ref> |
|||
===Paduan aluminium=== |
|||
{{Utama|Paduan aluminium}} |
|||
Mangan digunakan dalam produksi beberapa paduan dengan aluminium. Aluminium dengan sekitar 1,5% mangan dapat meningkatkan ketahanan terhadap korosi melalui butiran yang menyerap kotoran yang akan menyebabkan [[korosi galvanik]].<ref>{{cite web |url=http://www.suppliersonline.com/propertypages/2024.asp|title=Chemical properties of 2024 aluminum allow|access-date=27 Juni 2023 |publisher=Metal Suppliers Online, LLC.}}</ref> [[Paduan aluminium]] tahan korosi 3004 dan 3104 (0,8 hingga 1,5% mangan) digunakan untuk sebagian besar [[kaleng minuman]].<ref name="Al3004">{{cite book |title=Introduction to aluminum alloys and tempers|first=John Gilbert |last=Kaufman|publisher=ASM International|date=2000|isbn=978-0-87170-689-8|chapter=Applications for Aluminium Alloys and Tempers |pages=93–94|chapter-url=https://books.google.com/books?id=idmZIDcwCykC&pg=PA93}}</ref> Sebelum tahun 2000, lebih dari 1,6 juta [[ton metrik|ton]] paduan tersebut digunakan; dengan 1% mangan, paduan ini menghabiskan 16.000 ton mangan.{{Gagal diverifikasi|date=Juni 2023}}<ref name="Al3004" /> |
|||
====Baterai==== |
|||
[[Mangan dioksida|Mangan(IV) oksida]] digunakan pada [[baterai listrik|baterai]] sel kering tipe asli sebagai akseptor elektron dari seng, dan merupakan bahan kehitaman pada sel senter tipe karbon–seng. Mangan dioksida akan direduksi menjadi mangan oksida-hidroksida MnO(OH) selama pemakaian, mencegah pembentukan hidrogen pada anoda baterai.<ref name="BattHist" /> |
|||
:MnO<sub>2</sub> + H<sub>2</sub>O + e<sup>−</sup> → MnO(OH) + {{chem|OH|-}} |
|||
Bahan yang sama juga berfungsi pada [[baterai alkalin]] (biasanya sel baterai) yang lebih baru, yang menggunakan reaksi dasar yang sama, tetapi campuran elektrolitnya berbeda. Pada tahun 2002, lebih dari 230.000 ton mangan dioksida digunakan untuk tujuan ini.<ref name="ChiuZMnO2" /><ref name="BattHist">{{cite journal|doi=10.1016/S0167-2738(00)00722-0|title=Batteries fifty years of materials development|date=2000|last=Dell|first=R. M.|journal=Solid State Ionics|volume=134|issue=1–2|pages=139–158}}</ref> |
|||
[[Berkas:1945-P-Jefferson-War-Nickel-Reverse.JPG|upright|thumb|Koin 5 sen era Perang Dunia II (1942-5 diidentifikasi dengan tanda percetakan uang logam P, D atau S di atas kubah) yang terbuat dari paduan 56% tembaga, 35% perak, dan 9% mangan]] |
|||
====Resistor==== |
|||
Paduan tembaga mangan, seperti [[Manganin]], umumnya ditemukan dalam resistor ''shunt'' unsur logam yang digunakan untuk mengukur jumlah arus yang relatif besar. Paduan ini memiliki [[Koefisien suhu#TCR|koefisien ketahanan suhu]] yang sangat rendah dan tahan terhadap belerang. Hal ini membuat paduan ini sangat berguna di lingkungan otomotif dan industri yang keras.<ref name="ShuntDatasheet">{{cite web |title=WSK1216 |url=https://www.vishay.com/docs/30189/wsk1216.pdf |website=vishay |publisher=Vishay Intertechnology |access-date=27 Juni 2023}}</ref> |
|||
====Ceruk==== |
|||
[[Metilsiklopentadienil mangan trikarbonil]] adalah sebuah aditif dalam beberapa [[bensin|bensin tanpa timbal]] untuk meningkatkan [[bilangan oktan|nilai oktan]] dan mengurangi [[detonasi|ketukan mesin]].<ref>{{cite web |title=EPA Comments on the Gasoline Additive MMT |url=https://www.epa.gov/gasoline-standards/epa-comments-gasoline-additive-mmt |website=epa.gov |publisher=[[Badan Perlindungan Lingkungan Amerika Serikat|EPA]] |access-date=27 Juni 2023}}</ref> |
|||
Mangan(IV) oksida (mangan dioksida, MnO<sub>2</sub>) digunakan sebagai reagen dalam [[kimia organik]] untuk [[redoks|oksidasi]] [[alkohol]] benzilik (di mana [[hidroksil|gugus hidroksil]] berdekatan dengan sebuah [[Aromatisitas|cincin aromatik]]). Mangan dioksida telah digunakan sejak zaman dahulu untuk mengoksidasi dan menetralkan semburat kehijauan pada kaca dari sejumlah kecil besi pengotor.<ref name="ItGlass">{{cite journal |doi=10.1007/s11837-998-0024-0|title=Glassmaking in renaissance Italy: The innovation of venetian cristallo|date=1998|last=Mccray |first=W. Patrick|journal=JOM|volume=50|pages=14–19|issue=5|bibcode=1998JOM....50e..14M|s2cid=111314824}}</ref> MnO<sub>2</sub> juga digunakan dalam pembuatan oksigen dan klorin serta dalam pengeringan cat hitam. Dalam beberapa pembuatan, ia adalah [[pigmen]] cokelat untuk [[cat]] dan merupakan penyusun [[serbuk kopi]] alami.<ref name=straightouttathetheumberwikiarticle>{{cite book |title=Shorter Oxford English Dictionary |url=https://archive.org/details/shorteroxfordeng00will_0 |publisher=Oxford University Press |year=2002 |isbn=978-0-19-860457-0 |quote=Tanah berwarna merah kecokelatan yang mengandung besi dan mangan oksida dan lebih gelap dari oker dan sienna, digunakan untuk membuat berbagai pigmen. |edition=5}}</ref> |
|||
Mangan [[Valensi|tetravalen]] digunakan sebagai [[Aktivator (fosfor)|aktivator]] dalam [[fosfor]] pemancar merah. Walaupun banyak senyawa diketahui dapat menunjukkan [[luminesensi]],<ref>{{cite journal|journal=RSC Advances |date=2016|volume=6|issue=89|pages=86285–86296|first=Daquin|last=Chen|author2=Zhou, Yang |author3=Zhong, Jiasong |title=A review on Mn<sup>4+</sup> activators in solids for warm white light-emitting diodes|doi=10.1039/C6RA19584A|bibcode=2016RSCAd...686285C}}</ref> mayoritas dari mereka tidak digunakan dalam aplikasi komersial karena efisiensinya rendah atau pancarannya berwarna merah tua.<ref>{{cite journal|journal=Journal of Luminescence |date=2016|volume=177|pages=354–360|first=Florian|last=Baur|author2=Jüstel, Thomas|title=Dependence of the optical properties of Mn<sup>4+</sup> activated A<sub>2</sub>Ge<sub>4</sub>O<sub>9</sub> (A=K,Rb) on temperature and chemical environment|doi=10.1016/j.jlumin.2016.04.046|bibcode=2016JLum..177..354B}}</ref><ref>{{Cite journal|last1=Jansen|first1=T.|last2=Gorobez|first2=J.|last3=Kirm|first3=M.|last4=Brik|first4=M. G.|last5=Vielhauer|first5=S.|last6=Oja|first6=M.|last7=Khaidukov|first7=N. M.|last8=Makhov|first8=V. N.|last9=Jüstel|first9=T.|date=1 Januari 2018|title=Narrow Band Deep Red Photoluminescence of Y<sub>2</sub>Mg<sub>3</sub>Ge<sub>3</sub>O<sub>12</sub>:Mn<sup>4+</sup>,Li<sup>+</sup> Inverse Garnet for High Power Phosphor Converted LEDs|journal=ECS Journal of Solid State Science and Technology|volume=7|issue=1|pages=R3086–R3092|doi=10.1149/2.0121801jss|s2cid=103724310 }}</ref> Namun, beberapa fluorida teraktivasi Mn<sup>4+</sup> dilaporkan sebagai fosfor pemancar merah potensial untuk [[Dioda pemancar cahaya|LED]] putih-hangat.<ref>{{Cite journal|last1=Jansen|first1=Thomas|last2=Baur|first2=Florian|last3=Jüstel|first3=Thomas|title=Red emitting K<sub>2</sub>NbF<sub>7</sub>:Mn<sup>4+</sup> and K<sub>2</sub>TaF<sub>7</sub>:Mn<sup>4+</sup> for warm-white LED applications|journal=Journal of Luminescence|volume=192|pages=644–652|doi=10.1016/j.jlumin.2017.07.061|year=2017|bibcode=2017JLum..192..644J}}</ref><ref>{{Cite journal|last1=Zhou|first1=Zhi|last2=Zhou|first2=Nan|last3=Xia|first3=Mao|last4=Yokoyama|first4=Meiso|last5=Hintzen|first5=H. T. (Bert)|date=6 Oktober 2016|title=Research progress and application prospects of transition metal Mn<sup>4+</sup>-activated luminescent materials|journal=Journal of Materials Chemistry C|volume=4|issue=39|pages=9143–9161|doi=10.1039/c6tc02496c}}</ref> Namun hingga hari ini, hanya K<sub>2</sub>SiF<sub>6</sub>:Mn<sup>4+</sup> yang tersedia secara komersial untuk digunakan dalam LED putih-hangat.<ref>{{cite web|url=https://energy.gov/sites/prod/files/2015/02/f19/setlur_emitters_2015.pdf|title=TriGain LED phosphor system using red Mn<sup>4+</sup>-doped complex fluorides|publisher=GE Global Research |access-date=10 December 2022}}</ref> |
|||
Logam ini terkadang digunakan dalam koin; hingga tahun 2000, satu-satunya koin Amerika Serikat yang menggunakan mangan adalah [[Jefferson nickel#1938-1945: Awal produksi; perubahan Perang Dunia II|nikel "masa perang"]] dari tahun 1942 hingga 1945.<ref>{{cite journal|journal=Western Journal of Medicine |date=2001|volume=175|issue=2|pages=112–114|first=Raymond T.|last=Kuwahara|author2=Skinner III, Robert B. |author3=Skinner Jr., Robert B. |title=Nickel coinage in the United States|doi=10.1136/ewjm.175.2.112|pmid=11483555|pmc=1071501}}</ref> Sebuah paduan 75% tembaga dan 25% nikel secara tradisional digunakan untuk produksi koin nikel. Namun, karena pasokan logam nikel yang terus berkurang selama perang, ia diganti dengan perak dan mangan yang lebih tersedia, sehingga menghasilkan paduan 56% tembaga, 35% perak, dan 9% mangan. Sejak tahun 2000, [[Koin solar (Amerika Serikat)|koin dolar]], misalnya [[dolar Sacagawea]] dan [[Koin dolar presiden|koin Presiden $1]], dibuat dari kuningan yang mengandung 7% mangan dengan inti tembaga murni.<ref>{{cite web|url=http://www.usmint.gov/mint_programs/golden_dollar_coin/index.cfm?action=sacDesign|title=Design of the Sacagawea dollar|publisher=United States Mint |access-date=27 Juni 2023}}</ref> Dalam kedua kasus nikel dan dolar, penggunaan mangan dalam koin ini adalah untuk menduplikasi sifat elektromagnetik dari koin berukuran dan bernilai identik sebelumnya dalam mekanisme [[mesin jual otomatis|mesin penjual otomatis]]. Dalam kasus koin dolar A.S. selanjutnya, paduan mangan dimaksudkan untuk menduplikasi sifat paduan tembaga/nikel yang digunakan dalam [[dolar Susan B. Anthony]]. |
|||
Senyawa mangan telah digunakan sebagai pigmen dan pewarna keramik dan kaca. Warna cokelat pada keramik terkadang merupakan hasil dari senyawa mangan.<ref>{{cite book|title=Ceramics for the Archaeologist|first=Anna Osler|last=Shepard|publisher=Carnegie Institution of Washington|date=1956|pages=40–42|isbn=978-0-87279-620-1|chapter=Manganese and Iron–Manganese Paints}}</ref> Dalam industri kaca, senyawa mangan digunakan untuk dua efek. [[Mangan(III) oksida|Mangan(III)]] akan bereaksi dengan [[Besi(II) oksida|besi(II)]] untuk mengurangi warna hijau yang kuat pada kaca dengan membentuk besi(III) yang kurang berwarna dan mangan(II) yang berwarna agak merah muda, mengimbangi sisa warna besi(III).<ref name="ItGlass" /> Jumlah mangan yang lebih besar digunakan untuk menghasilkan kaca berwarna merah muda. Pada tahun 2009, Profesor [[Mas Subramanian]] dan rekannya di [[Universitas Negeri Oregon]] menemukan bahwa mangan dapat digabungkan dengan [[itrium]] dan [[indium]] untuk membentuk [[pigmen]] yang sangat [[biru]], tidak beracun, lengai, dan tahan pudar, yaitu [[biru YInMn]], pigmen biru baru pertama yang ditemukan pada tahun 200 terakhir.{{Butuh rujukan|date=Juni 2023}} |
|||
==Peran biologis== |
|||
[[Berkas:Arginase.jpeg|thumb|upright=1.3|Pusat reaktif arginase dengan [[inhibitor enzim|inhibitor]] asam boronat – atom mangan ditunjukkan dengan warna kuning.]]{{Utama|Mangan dalam biologi}} |
|||
===Biokimia=== |
|||
Kelas [[enzim]] yang memiliki [[Kofaktor (biokimia)|kofaktor]] mangan meliputi [[oksidoreduktase]], [[transferase]], [[hidrolase]], [[liase]], [[isomerase]], dan [[ligase]]. Enzim lain yang mengandung mangan adalah [[arginase]] dan [[superoksida dismutase]] yang mengandung Mn ([[SOD2|Mn-SOD]]). Juga, kelas enzim [[transkriptase balik]] dari banyak [[Retroviridae|retrovirus]] (meskipun bukan ''[[lentivirus]]'' seperti [[HIV]]) mengandung mangan. [[Peptida|Polipeptida]] yang mengandung mangan adalah [[toksin difteri]], [[lektin]], dan [[integrin]].<ref name="Mnzym">{{cite journal |doi=10.1021/acs.accounts.7b00343 |title=Manganese–Oxygen Intermediates in O–O Bond Activation and Hydrogen-Atom Transfer Reactions |year=2017 |last1=Rice |first1=Derek B. |last2=Massie |first2=Allyssa A. |last3=Jackson |first3=Timothy A. |journal=Accounts of Chemical Research |volume=50 |issue=11 |pages=2706–2717 |pmid=29064667 }}</ref> |
|||
===Peran biologis pada manusia=== |
|||
Mangan adalah unsur makanan manusia yang penting. Ia hadir sebagai sebuah [[Kofaktor (biokimia)|koenzim]] dalam beberapa proses biologis, yang meliputi metabolisme makronutrien, pembentukan tulang, dan sistem pertahanan [[radikal bebas]]. Ia adalah komponen penting dalam lusinan protein dan enzim.<ref name="Erikson-2019">{{cite book |
|||
|last1=Erikson|first1=Keith M. |last2=Ascher |first2=Michael |
|||
|editor1-last=Sigel|editor1-first=Astrid |
|||
|editor2-last=Freisinger|editor2-first=Eva |
|||
|editor3-last=Sigel|editor3-first=Roland K. O. |
|||
|editor4-last=Carver|editor4-first=Peggy L. |
|||
|title=Essential Metals in Medicine:Therapeutic Use and Toxicity of Metal Ions in the Clinic |
|||
|journal=Metal Ions in Life Sciences |volume=19 |date=2019 |publisher=de Gruyter GmbH|location=Berlin |
|||
|isbn=978-3-11-052691-2 |
|||
|doi=10.1515/9783110527872-016 |
|||
|pmid=30855111 |
|||
|pages=253–266|chapter=Chapter 10. Manganese: Its Role in Disease and Health|s2cid=73725546 }} |
|||
</ref> Tubuh manusia mengandung sekitar 12 mg mangan, kebanyakan di tulang. Sisa jaringan lunak terkonsentrasi di hati dan ginjal.<ref name="Emsley2001" /> Di otak manusia, mangan terikat pada [[metaloprotein]] mangan, terutama [[glutamin sintetase]] dalam [[astrosit]].<ref>{{cite journal|doi=10.1016/S0165-0173(02)00234-5|title=Manganese action in brain function|url=https://archive.org/details/sim_brain-research-reviews_2003-01_41_1/page/79|date=2003 |last=Takeda |first=A.|journal=Brain Research Reviews|volume=41|issue=1|pmid=12505649|pages=79–87|s2cid=1922613}}</ref> |
|||
====Nutrisi==== |
|||
<div style="float: right; margin: 2px; font-size:85%;"> |
|||
{| class="wikitable" |
|||
|+AI mangan saat ini menurut kelompok umur dan jenis kelamin<ref name="MnDRI" /> |
|||
!colspan="2"|Pria |
|||
!colspan="2"|Wanita |
|||
|- |
|||
!Usia |
|||
!AI (mg/hari) |
|||
!Usia |
|||
!AI (mg/hari) |
|||
|- |
|||
|1–3 |
|||
|1,2 |
|||
|1–3 |
|||
|1,2 |
|||
|- |
|||
|4–8 |
|||
|1,5 |
|||
|4–8 |
|||
|1,5 |
|||
|- |
|||
|9–13 |
|||
|1,9 |
|||
|9–13 |
|||
|1,6 |
|||
|- |
|||
|14–18 |
|||
|2,2 |
|||
|14–18 |
|||
|1,6 |
|||
|- |
|||
|rowspan=3|19+ |
|||
|rowspan=3|2,3 |
|||
|rowspan=3|19+ |
|||
|1,8 |
|||
|- |
|||
|hamil: 2 |
|||
|- |
|||
|menyusui: 2,6 |
|||
|}</div> |
|||
[[Akademi Kedokteran Nasional|Institut Kedokteran]] A.S. (IOM) memperbarui Kebutuhan Perkiraan Rata-rata (EAR) dan Angka Kecukupan Gizi (AKG) untuk mineral pada tahun 2001. Untuk mangan, tidak ada informasi yang cukup untuk menetapkan EAR dan AKG, sehingga kebutuhannya digambarkan sebagai perkiraan [[Asupan Referensi Diet#Parameter|Asupan Adekuat]] (AI). Mengenai keamanan, IOM menetapkan [[Asupan Referensi Diet#Parameter|Batas Atas Asupan]] (UL) yang dapat ditoleransi untuk vitamin dan mineral bila bukti cukup. Dalam kasus mangan, UL dewasa ditetapkan pada 11 mg/hari. Secara kolektif EAR, AKG, AI, dan UL disebut sebagai [[Asupan Referensi Diet]] (DRI).<ref name="MnDRI">{{cite book|chapter=Manganese|chapter-url=https://www.nap.edu/read/10026/chapter/12 |title=Dietary Reference Intakes for Vitamin A, Vitamin K, Arsenic, Boron, Chromium, Chromium, Iodine, Iron, Manganese, Molybdenum, Nickel, Silicon, Vanadium, and Chromium|publisher= National Academy Press|year= 2001|pages=394–419|pmid=25057538|isbn=978-0-309-07279-3|author1=Institute of Medicine (US) Panel on Micronutrients }}</ref> Kekurangan mangan jarang terjadi.<ref>''Lihat'' {{cite web|url=http://lpi.oregonstate.edu/mic/minerals/manganese |title=Manganese|work=Micronutrient Information Center|publisher=[[Universitas Negeri Oregon|Oregon State University]] [[Institut Linus Pauling|Linus Pauling Institute]]|date=23 April 2014}}</ref> |
|||
[[Otoritas Keamanan Makanan Eropa]] (EFSA) menyebut kumpulan informasi kolektif tersebut sebagai Nilai Referensi Diet, dengan Asupan Referensi Populasi (PRI) alih-alih AKG, dan Kebutuhan Rata-rata alih-alih EAR. AI dan UL didefinisikan sama seperti di Amerika Serikat. Untuk orang berusia 15 tahun ke atas, AI ditetapkan sebesar 3,0 mg/hari. AI untuk ibu hamil dan menyusui adalah 3,0 mg/hari. Untuk anak usia 1–14 tahun, AI meningkat seiring bertambahnya usia dari 0,5 menjadi 2,0 mg/hari. AI dewasa lebih tinggi dari AKG Amerika Serikat.<ref>{{cite web | title = Overview on Dietary Reference Values for the EU population as derived by the EFSA Panel on Dietetic Products, Nutrition and Allergies| year = 2017| url = https://www.efsa.europa.eu/sites/default/files/assets/DRV_Summary_tables_jan_17.pdf}}</ref> EFSA meninjau pertanyaan keamanan yang sama dan memutuskan bahwa tidak ada cukup informasi untuk menetapkan UL.<ref>{{citation| title = Tolerable Upper Intake Levels For Vitamins And Minerals| publisher = European Food Safety Authority| year = 2006| url = http://www.efsa.europa.eu/sites/default/files/efsa_rep/blobserver_assets/ndatolerableuil.pdf}}</ref> |
|||
Untuk tujuan pelabelan makanan dan suplemen makanan A.S., jumlah dalam satu porsi dinyatakan sebagai persentase dari Nilai Harian (%DV). Untuk tujuan pelabelan mangan, 100% Nilai Harian adalah 2,0 mg, tetapi pada 27 Mei 2016 direvisi menjadi 2,3 mg agar sesuai dengan AKG.<ref name="FedReg">{{cite web|url=https://www.gpo.gov/fdsys/pkg/FR-2016-05-27/pdf/2016-11867.pdf |title=Federal Register May 27, 2016 Food Labeling: Revision of the Nutrition and Supplement Facts Labels. FR page 33982.}}</ref><ref>{{cite web | title=Daily Value Reference of the Dietary Supplement Label Database (DSLD) | website=Dietary Supplement Label Database (DSLD) | url=https://www.dsld.nlm.nih.gov/dsld/dailyvalue.jsp | access-date=27 Juni 2023 | archive-date=7 April 2020 | archive-url=https://web.archive.org/web/20200407073956/https://dsld.nlm.nih.gov/dsld/dailyvalue.jsp | url-status=dead }}</ref> Tabel nilai harian dewasa lama dan baru disediakan di [[Asupan Harian Referensi]]. |
|||
Paparan atau asupan yang berlebihan dapat menyebabkan kondisi yang dikenal sebagai [[manganisme]], sebuah gangguan [[Penyakit neurodegeneratif|neurodegeneratif]] yang dapat menyebabkan kematian neuron [[dopamin]]ergik dan memiliki gejala yang mirip dengan [[penyakit Parkinson]].<ref name="Emsley2001" /><ref>{{cite book |first1=Daiana|last1=Silva Avila|first2=Robson|last2=Luiz Puntel|first3=Michael|last3=Aschner|editor=Astrid Sigel|editor2=Helmut Sigel |editor3=Roland K. O. Sigel|title=Interrelations between Essential Metal Ions and Human Diseases|series=Metal Ions in Life Sciences |
|||
|volume=13|date=2013|publisher=Springer|pages=199–227|chapter=Chapter 7. Manganese in Health and Disease |doi=10.1007/978-94-007-7500-8_7|pmid=24470093|pmc=6589086|isbn=978-94-007-7499-5}}</ref> |
|||
====Kekurangan mangan==== |
|||
{{Utama|Kekurangan mangan (kedokteran)|l1=Kekurangan mangan}} |
|||
Kekurangan mangan pada manusia, yang jarang terjadi, dapat mengakibatkan sejumlah masalah medis. Kekurangan mangan menyebabkan deformasi tulang pada hewan dan menghambat produksi kolagen dalam penyembuhan luka.{{Butuh rujukan|date=Juni 2023}} |
|||
===Toksisitas dalam kehidupan laut=== |
|||
Banyak sistem enzimatik membutuhkan Mn untuk berfungsi, tetapi dalam kadar tinggi, Mn dapat menjadi racun. Salah satu alasan lingkungan mengapa tingkat Mn dapat meningkat dalam air laut adalah ketika periode hipoksia terjadi.<ref>{{Cite journal|last1=Hernroth|first1=Bodil|last2=Krång|first2=Anna-Sara|last3=Baden|first3=Susanne|date=February 2015|title=Bacteriostatic suppression in Norway lobster (Nephrops norvegicus) exposed to manganese or hypoxia under pressure of ocean acidification|url=http://dx.doi.org/10.1016/j.aquatox.2014.11.025|journal=Aquatic Toxicology|volume=159|pages=217–224|doi=10.1016/j.aquatox.2014.11.025|pmid=25553539|issn=0166-445X}}</ref> Sejak tahun 1990, telah ada laporan mengenai akumulasi Mn pada organisme laut meliputi ikan, [[krustasea]], [[moluska]], dan [[echinodermata|ekinodermata]]. Jaringan spesifik adalah target pada spesies yang berbeda, meliputi insang, otak, darah, ginjal, dan hati/hepatopankreas. Efek fisiologis telah dilaporkan pada spesies ini. Mn dapat memengaruhi pembaharuan imunosit dan fungsinya, seperti fagositosis dan aktivasi pro-fenoloksidase, menekan sistem kekebalan organisme. Hal ini akan menyebabkan organisme menjadi lebih rentan terhadap infeksi. Saat perubahan iklim terjadi, distribusi patogen akan meningkat, dan agar organisme dapat bertahan hidup dan mempertahankan diri dari patogen ini, mereka memerlukan sistem kekebalan yang sehat dan kuat. Jika sistem mereka dikompromikan dari tingkat Mn yang tinggi, mereka tidak akan mampu melawan patogen ini dan akhirnya mati.<ref name="Hernroth-2020" /> |
|||
===Peran biologis pada bakteri=== |
|||
Mn-SOD adalah jenis SOD yang terdapat pada [[mitokondria]] [[eukariota|eukariotik]], dan juga di sebagian besar bakteri (fakta ini sesuai dengan teori mitokondria berasal dari bakteri). Enzim Mn-SOD mungkin salah satu yang paling kuno, karena hampir semua organisme yang hidup dengan adanya oksigen menggunakannya untuk mengatasi efek racun dari [[superoksida]] ({{chem|O|2|-}}), yang terbentuk dari reduksi 1 elektron dioksigen. Pengecualiannya, yang semuanya adalah bakteri, meliputi ''[[Lactiplantibacillus plantarum|Lactobacillus plantarum]]'' dan [[lactobacillus|laktobasili]] terkait, yang menggunakan sebuah mekanisme nonenzimatik yang berbeda dengan ion mangan (Mn<sup>2+</sup>) yang dikomplekskan dengan polifosfat, menunjukkan jalur evolusi untuk fungsi ini dalam kehidupan aerobik.{{Butuh rujukan|date=Juni 2023}} |
|||
===Peran biologis pada tumbuhan=== |
|||
{{Lihat pula|Kekurangan mangan (tumbuhan)}} |
|||
Mangan juga penting dalam [[evolusi oksigen]] fotosintesis dalam [[kloroplas]] pada tumbuhan. [[Kompleks evolusi oksigen]] (OEC) adalah bagian dari fotosistem II yang terkandung dalam membran tilakoid kloroplas; ia bertanggung jawab atas [[Evolusi oksigen|fotooksidasi terminal air]] selama [[Reaksi yang bergantung-cahaya|reaksi cahaya]] [[fotosintesis]], dan memiliki inti metaloenzim yang mengandung empat atom mangan.<ref>{{cite journal|last1=Umena|first1=Yasufumi|last2=Kawakami|first2=Keisuke|last3=Shen|first3=Jian-Ren|last4=Kamiya |first4=Nobuo|title=Crystal structure of oxygen-evolving photosystem II at a resolution of 1.9 Å|journal=Nature|volume=473|issue=7345|pages=55–60|doi=10.1038/nature09913|pmid=21499260|date=Mei 2011|bibcode=2011Natur.473...55U|s2cid=205224374|url=http://ousar.lib.okayama-u.ac.jp/files/public/4/47455/20160528084139320094/Nature_473_55–60.pdf}}</ref><ref>{{cite encyclopedia|last=Dismukes|first=G. Charles|author2=Willigen, Rogier T. van|title=Manganese: The Oxygen-Evolving Complex & Models Based in part on the article Manganese: Oxygen-Evolving Complex & Models by Lars-Erik Andréasson & Tore Vänngård which appeared in the Encyclopedia of Inorganic Chemistry, First Edition, First Edition|date=2006|encyclopedia=Encyclopedia of Inorganic Chemistry|doi=10.1002/0470862106.ia128|chapter=Manganese: The Oxygen-Evolving Complex & Models|isbn=978-0470860786}}</ref> Untuk memenuhi persyaratan ini, sebagian besar pupuk tumbuhan berspektrum-luas mengandung mangan.{{Butuh rujukan|date=Juni 2023}} |
|||
==Pencegahan== |
|||
{{Chembox |
|||
| container_only = yes |
|||
|Section7={{Chembox Hazards |
|||
| ExternalSDS = |
|||
| GHSPictograms = |
|||
| GHSSignalWord = |
|||
| HPhrases = {{H-phrases|401}} |
|||
| PPhrases = {{P-phrases|273|501}}<ref>{{cite web |url=https://www.sigmaaldrich.com/MSDS/MSDS/DisplayMSDSPage.do?country=US&language=en&productNumber=266167&brand=ALDRICH&PageToGoToURL=https%3A%2F%2Fwww.sigmaaldrich.com%2Fcatalog%2Fproduct%2Faldrich%2F266167%3Flang%3Den |title=Safety Data Sheet |publisher=Sigma-Aldrich |access-date=28 Juni 2023 }}</ref> |
|||
| NFPA-H = 0 |
|||
| NFPA-F = 0 |
|||
| NFPA-R = 0 |
|||
| NFPA-S = |
|||
| NFPA_ref = |
|||
}} |
|||
}} |
|||
Senyawa mangan kurang beracun dibandingkan dengan logam lain yang tersebar luas, seperti [[nikel]] dan [[tembaga]].<ref>{{cite book|pages=31 |title=Manganese|first=Heather|last=Hasan|publisher=The Rosen Publishing Group|date=2008|isbn=978-1-4042-1408-8 |url=https://books.google.com/books?id=nRmpEaudmTYC&pg=PA31}}</ref> Namun, paparan debu dan asap mangan tidak boleh melebihi nilai tertinggi sebesar 5 mg/m<sup>3</sup> bahkan untuk waktu yang singkat karena tingkat toksisitasnya.<ref>{{cite web|url=http://www.environmentwriter.org/resources/backissues/chemicals/manganese.htm |archive-url=https://web.archive.org/web/20060828211701/http://www.environmentwriter.org/resources/backissues/chemicals/manganese.htm |url-status=dead |archive-date=28 Agustus 2006 |title=Manganese Chemical Background |access-date=28 Juni 2023 |publisher=Metcalf Institute for Marine and Environmental Reporting University of Rhode Island |date=April 2006 }}</ref> <!--Mangan dapat menimbulkan risiko tertentu bagi anak-anak karena kecenderungannya untuk berikatan dengan reseptor CH-7.{{Butuh klarifikasi|date=Juni 2023}}--> Keracunan mangan telah dikaitkan dengan gangguan keterampilan motorik dan gangguan kognitif.<ref>{{cite web|url=http://rais.ornl.gov/tox/profiles/mn.html|publisher=[[Laboratorium Nasional Oak Ridge]]|title=Risk Assessment Information System Toxicity Summary for Manganese|access-date=28 Juni 2023}}</ref> |
|||
Permanganat menunjukkan toksisitas yang lebih tinggi daripada senyawa mangan(II). Dosis fatalnya ialah sekitar 10 g, dan beberapa keracunan fatal telah terjadi. Efek oksidatifnya yang kuat dapat menyebabkan [[nekrosis]] pada [[membran mukosa|selaput lendir]]. Misalnya, [[esofagus|kerongkongan]] akan terpengaruh jika permanganat tertelan. Hanya sejumlah kecil yang diserap oleh usus, tetapi jumlah kecil ini menunjukkan efek yang parah pada ginjal dan hati.<ref>{{cite journal|doi=10.1136/emj.14.1.43|title=Potassium permanganate poisoning – a rare cause of fatal self poisoning|date=1997|last1=Ong|first1=K. L.|journal=Emergency Medicine Journal|volume=14|pages=43–45|pmid=9023625|last2=Tan |last3=Cheung|issue=1|first2=T. H.|first3=W. L.|pmc=1342846}}</ref><ref>{{cite journal|doi=10.1177/096032719601500313|title=Fatal acute hepatorenal failure following potassium permanganate ingestion|url=https://archive.org/details/sim_human-and-experimental-toxicology_1996-03_15_3/page/n84|date=1996|last1=Young|first1=R.|journal=Human & Experimental Toxicology |volume=15|pages=259–61|pmid=8839216|last2=Critchley|last3=Young|last4=Freebairn|last5=Reynolds|last6=Lolin|issue=3|first2=J. A. |first3=K. K.|first4=R. C.|first5=A. P.|first6=Y. I.|s2cid=8993404}}</ref> |
|||
Paparan mangan di [[Amerika Serikat]] diatur oleh [[Administrasi Keselamatan dan Kesehatan Kerja]] (OSHA).<ref name="osha.gov">{{cite web|title=Safety and Health Topics: Manganese Compounds (as Mn)|url=https://www.osha.gov/dts/chemicalsampling/data/CH_250190.html|publisher=U.S. [[Administrasi Keselamatan dan Kesehatan Kerja|Occupational Safety and Health Administration]]}}</ref> Seseorang dapat terpapar mangan di tempat kerja dengan menghirup atau menelannya. OSHA telah menetapkan batas legal ([[batas paparan diizinkan|batas paparan yang diizinkan]]) untuk paparan mangan di tempat kerja sebesar 5 mg/m<sup>3</sup> selama 8 jam hari kerja. [[Institut Nasional untuk Keselamatan dan Kesehatan Kerja]] (NIOSH) telah menetapkan [[batas paparan direkomendasikan|batas paparan yang direkomendasikan]] (REL) sebesar 1 mg/m<sup>3</sup> selama 8 jam hari kerja dan batas jangka pendek sebesar 3 mg/m<sup>3</sup>. Pada kadar 500 mg/m<sup>3</sup>, mangan [[IDLH|langsung berbahaya bagi kehidupan dan kesehatan]].<ref>{{cite web|title=NIOSH Pocket Guide to Chemical Hazards – Manganese compounds and fume (as Mn)|url=https://www.cdc.gov/niosh/npg/npgd0379.html|publisher=Centers for Disease Control|access-date=28 Juni 2023}}</ref> |
|||
Secara umum, paparan terhadap konsentrasi udara Mn sekitar yang melebihi 5 μg Mn/m<sup>3</sup> dapat menyebabkan gejala yang diinduksi oleh Mn. Peningkatan ekspresi protein [[feroportin]] dalam sel ginjal embrionik manusia (HEK293) dikaitkan dengan penurunan konsentrasi Mn intraseluler dan [[sitotoksisitas]] yang dilemahkan, ditandai dengan pembalikan serapan [[asam glutamat|glutamat]] yang dikurangi Mn dan berkurangnya kebocoran [[laktat dehidrogenase]].<ref>{{cite journal|pmid=20002294|last1=Yin|first1=Z.|date=2010|pages=1190–8|issue=5|volume=112|last2=Jiang|first2=H.|journal=Journal of Neurochemistry|last3=Lee|first3=E. S.|last4=Ni|first4=M.|last5=Erikson|first5=K. M.|last6=Milatovic|first6=D.|last7=Bowman|first7=A. B.|last8=Aschner|first8=M.|title=Ferroportin is a manganese-responsive protein that decreases manganese cytotoxicity and accumulation |url=http://libres.uncg.edu/ir/uncg/f/K_Erickson_Ferroportin_2009.pdf|pmc=2819584|doi=10.1111/j.1471-4159.2009.06534.x}}</ref> |
|||
==Masalah kesehatan lingkungan== |
|||
===Dalam air minum=== |
|||
Mangan yang ditularkan melalui air memiliki [[bioavailabilitas]] yang lebih besar daripada mangan makanan. Menurut hasil dari penelitian tahun 2010,<ref name="Bouchard 138–143">{{cite journal|doi=10.1289/ehp.1002321 |volume=119|pages=138–143|pmid=20855239 |issue=1 |pmc=3018493|year=2011 |last1=Bouchard |first1=M. F |title=Intellectual impairment in school-age children exposed to manganese from drinking water |journal=Environmental Health Perspectives |last2=Sauvé |first2=S |last3=Barbeau |first3=B |last4=Legrand |first4=M |last5=Bouffard |first5=T |last6=Limoges |first6=E |last7=Bellinger |first7=D. C |last8=Mergler |first8=D }}</ref> tingkat paparan mangan yang lebih tinggi dalam [[air minum]] dikaitkan dengan peningkatan [[Disabilitas perkembangan|gangguan intelektual]] dan penurunan [[kecerdasan intelektual]] (IQ) pada anak usia sekolah. Dihipotesiskan bahwa paparan jangka panjang karena menghirup mangan alami dalam air pancuran membuat 8,7 juta orang Amerika berisiko.<ref>{{cite journal|doi=10.1081/CLT-100102427|pmid=10382563|title=Manganese|date=1999 |author=Barceloux, Donald |journal=Clinical Toxicology|volume=37|last2=Barceloux|first2=Donald|issue=2|pages=293–307}}</ref> Namun, data menunjukkan bahwa tubuh manusia dapat pulih dari efek samping tertentu dari paparan berlebih terhadap mangan jika paparan dihentikan dan tubuh dapat membersihkan kelebihannya.<ref>{{cite journal|pmid=8143974 |year=1994 |last1=Devenyi |first1=A. G |title=Dystonia, hyperintense basal ganglia, and high whole blood manganese levels in Alagille's syndrome |url=https://archive.org/details/sim_gastroenterology_1994-04_106_4/page/n293 |journal=Gastroenterology |volume=106 |issue=4 |pages=1068–71 |last2=Barron |first2=T. F |last3=Mamourian |first3=A. C |doi=10.1016/0016-5085(94)90769-2|s2cid=2711273 }}</ref> |
|||
===Dalam bensin=== |
|||
[[Berkas:Methylcyclopentadienyl manganese tricarbonyl.tif|thumb|upright|Model molekuler dari [[metilsiklopentadienil mangan trikarbonil]] (MMT)]] |
|||
[[Metilsiklopentadienil mangan trikarbonil]] (MMT) adalah aditif [[bensin]] yang digunakan untuk menggantikan senyawa timbal pada bensin tanpa timbal untuk meningkatkan [[bilangan oktan|nilai oktan]] distilat minyak beroktan rendah. Ia dapat mengurangi agen [[detonasi|ketukan mesin]] melalui aksi [[karbonil|gugus karbonil]]. Bahan bakar yang mengandung mangan cenderung membentuk mangan karbida, yang dapat merusak [[Katup poppet|katup buang]]. Dibandingkan dengan tahun 1953, saat ini kadar mangan di udara telah menurun.<ref>Agency for Toxic Substances and Disease Registry (2012) [http://www.atsdr.cdc.gov/toxprofiles/tp151-c6.pdf 6. Potential for human exposure], dalam [http://www.atsdr.cdc.gov/ToxProfiles/tp.asp?id=102&tid=23 ''Toxicological Profile for Manganese''], Atlanta, GA: U.S. Department of Health and Human Services.</ref> |
|||
===Dalam asap tembakau=== |
|||
[[Nicotiana|Tumbuhan tembakau]] dapat dengan mudah menyerap dan mengakumulasi [[logam berat]] seperti mangan dari tanah di sekitarnya ke dalam daunnya. Mereka kemudian dihirup selama [[pengisapan tembakau]].<ref>{{cite journal|pmc=3586865|year=2012|last1=Pourkhabbaz|first1=A|title=Investigation of Toxic Metals in the Tobacco of Different Iranian Cigarette Brands and Related Health Issues|journal=Iranian Journal of Basic Medical Sciences|volume=15|issue=1|pages=636–644|last2=Pourkhabbaz|first2=H|pmid=23493960}}</ref> Walaupun mangan adalah salah satu konstituen dari [[asap tembakau]],<ref name="TalhoutSchulz2011">{{cite journal|last1=Talhout|first1=Reinskje|last2=Schulz|first2=Thomas|last3=Florek|first3=Ewa|last4=Van Benthem|first4=Jan|last5=Wester|first5=Piet|last6=Opperhuizen|first6=Antoon|title=Hazardous Compounds in Tobacco Smoke|journal=International Journal of Environmental Research and Public Health|volume=8|issue=12|year=2011|pages=613–628|doi=10.3390/ijerph8020613|pmid=21556207|pmc=3084482|doi-access=free}}</ref> sebagian besar penelitian menyimpulkan bahwa konsentrasinya tidak berbahaya bagi kesehatan manusia.<ref>{{cite journal|doi=10.1080/15216540500459667|pmid=16393783|title=Metals in cigarette smoke|journal=IUBMB Life |volume=57|issue=12|pages=805–9|year=2005|last1=Bernhard|first1=David|last2=Rossmann|first2=Andrea|last3=Wick|first3=Georg|s2cid=35694266|doi-access=free}}</ref> |
|||
==Peran dalam gangguan neurologis== |
|||
===Manganisme=== |
|||
{{Utama|Manganisme}} |
|||
Paparan mangan berlebih paling sering dikaitkan dengan [[manganisme]], sebuah kelainan neurologis langka yang terkait dengan konsumsi atau inhalasi mangan yang berlebihan. Secara historis, orang yang bekerja dalam produksi atau pemrosesan paduan mangan<ref>Baselt, R. (2008) ''Disposition of Toxic Drugs and Chemicals in Man'', edisi ke-8, Biomedical Publications, Foster City, CA, hlm. 883–886, {{ISBN|0-9626523-7-7}}.</ref><ref>{{cite journal|doi=10.1023/A:1021970120965|date=2002|author=Normandin, Louise|journal=Metabolic Brain Disease |volume=17|pages=375–87|pmid=12602514|last2=Hazell|first2=A. S.|title=Manganese neurotoxicity: an update of pathophysiologic mechanisms |issue=4|s2cid=23679769}}</ref> berisiko mengembangkan manganisme; namun, peraturan kesehatan dan keselamatan saat ini telah melindungi para pekerja di negara maju.<ref name="osha.gov" /> Gangguan ini pertama kali dijelaskan pada tahun 1837 oleh akademisi Inggris John Couper, yang mempelajari dua pasien yang merupakan penggiling mangan.<ref name="Couper 1837 41–42">{{cite journal|last=Couper|first=John|title=On the effects of black oxide of manganese when inhaled into the lungs|journal=Br. Ann. Med. Pharm. Vital. Stat. Gen. Sci.|date=1837|volume=1 |pages=41–42}}</ref> |
|||
Manganisme adalah sebuah gangguan bifasik. Pada tahap awal, orang yang teler mungkin mengalami depresi, perubahan suasana hati, perilaku kompulsif, dan psikosis. Gejala neurologis awal digantikan oleh manganisme tahap akhir, yang menyerupai [[penyakit Parkinson]]. Gejala-gejalanya meliputi kelemahan, bicara monoton dan lambat, wajah tanpa ekspresi, tremor, gaya berjalan condong ke depan, ketidakmampuan untuk berjalan mundur tanpa jatuh, kekakuan, serta masalah umum dengan ketangkasan, gaya berjalan dan keseimbangan.<ref name="Couper 1837 41–42" /><ref name="Cersosimo 2007 340–346">{{cite journal|last=Cersosimo|first=M. G.|author2=Koller, W.C.|title=The diagnosis of manganese-induced parkinsonism |journal=NeuroToxicology|date=2007|volume=27|pages=340–346|doi=10.1016/j.neuro.2005.10.006|pmid=16325915|issue=3}}</ref> Tidak seperti penyakit Parkinson, manganisme tidak terkait dengan hilangnya indra penciuman dan pasien biasanya tidak responsif terhadap pengobatan dengan [[L-DOPA]].<ref>{{cite journal|last=Lu|first=C. S.|author2=Huang, C.C |author3=Chu, N.S. |author4=Calne, D.B. |title=Levodopa failure in chronic manganism|url=https://archive.org/details/sim_neurology_1994-09_44_9/page/1600|journal=Neurology|date=1994|volume=44|pages=1600–1602|doi=10.1212/WNL.44.9.1600|pmid=7936281|issue=9|s2cid=38040913}}</ref> Gejala manganisme tahap akhir menjadi lebih parah dari waktu ke waktu bahkan jika sumber paparan dihilangkan dan kadar mangan di otak kembali normal.<ref name="Cersosimo 2007 340–346" /> |
|||
Paparan mangan kronis telah terbukti menghasilkan penyakit seperti Parkinsonisme yang ditandai dengan kelainan gerakan.<ref name="Guilarte2015">{{cite journal | vauthors = Guilarte TR, Gonzales KK | title = Manganese-Induced Parkinsonism Is Not Idiopathic Parkinson's Disease: Environmental and Genetic Evidence | journal = Toxicological Sciences| volume = 146 | issue = 2 | pages = 204–12 | date = August 2015 | pmid = 26220508 | pmc = 4607750 | doi = 10.1093/toxsci/kfv099 | type= Review}}</ref> Kondisi ini tidak responsif terhadap [[Manajemen penyakit Parkinson|terhadap terapi tipikal yang digunakan dalam pengobatan PD]], menyarankan jalur alternatif selain kehilangan [[dopamin]]ergik tipikal di dalam [[substantia nigra]].<ref name="Guilarte2015" /> Mangan dapat menumpuk di [[basal ganglia]], menyebabkan gerakan abnormal.<ref name="Kwakye2015">{{cite journal | vauthors = Kwakye GF, Paoliello MM, Mukhopadhyay S, Bowman AB, Aschner M | title = Manganese-Induced Parkinsonism and Parkinson's Disease: Shared and Distinguishable Features | journal = Int J Environ Res Public Health | volume = 12 | issue = 7 | pages = 7519–40 | date = Juli 2015 | pmid = 26154659 | pmc = 4515672 | doi = 10.3390/ijerph120707519 | type= Review | doi-access = free }}</ref> Mutasi gen SLC30A10, transporter efluks mangan yang diperlukan untuk menurunkan Mn intraseluler, telah dikaitkan dengan perkembangan penyakit mirip Parkinsonisme ini.<ref name="Peres2016">{{cite journal | vauthors = Peres TV, Schettinger MR, Chen P, Carvalho F, Avila DS, Bowman AB, Aschner M | title = Manganese-induced neurotoxicity: a review of its behavioral consequences and neuroprotective strategies | journal = BMC Pharmacology & Toxicology| volume = 17 | issue = 1 | pages = 57 | date = November 2016 | pmid = 27814772 | pmc = 5097420 | doi = 10.1186/s40360-016-0099-0 | type= Review }}</ref> [[Badan Lewy]] khas untuk PD tidak terlihat pada parkinsonisme yang diinduksi oleh Mn.<ref name="Kwakye2015" /> |
|||
Eksperimen pada hewan telah memberikan kesempatan untuk memeriksa konsekuensi dari paparan berlebih mangan dalam kondisi yang terkendali. Pada tikus besar (''rat'') (yang tidak agresif), mangan akan menginduksi perilaku membunuh-tikus-kecil (''mouse-killing'').<ref>{{cite journal|last1=Lazrishvili|display-authors=etal|first1=I.|title=Manganese loading induces mouse-killing behaviour in nonaggressive rats|journal= Journal of Biological Physics and Chemistry|date=2016|volume=16|issue=3|pages=137–141 |doi=10.4024/31LA14L.jbpc.16.03}}</ref> |
|||
===Gangguan perkembangan anak=== |
|||
Beberapa penelitian baru-baru ini mencoba untuk menguji efek paparan mangan berlebih dosis rendah kronis pada [[perkembangan anak]]. Penelitian paling awal dilakukan di [[Shanxi|provinsi Shanxi]], Tiongkok. Air minum di sana telah terkontaminasi melalui irigasi limbah yang tidak tepat dan mengandung 240–350 μg Mn/L. Meskipun konsentrasi Mn pada atau di bawah 300 μg Mn/L dianggap aman pada saat penelitian oleh EPA A.S. dan 400 μg Mn/L oleh [[Organisasi Kesehatan Dunia]], 92 anak yang diambil sampelnya (berusia antara 11 dan 13 tahun) dari provinsi ini menunjukkan kinerja yang lebih rendah pada tes ketangkasan dan kecepatan manual, memori jangka pendek, dan identifikasi visual, dibandingkan dengan anak-anak dari daerah yang tidak terkontaminasi. Baru-baru ini, sebuah penelitian terhadap anak-anak berusia 10 tahun di Bangladesh menunjukkan hubungan antara konsentrasi Mn dalam air sumur dan penurunan skor IQ. Penelitian ketiga yang dilakukan di [[Quebec]] meneliti anak sekolah antara usia 6 dan 15 tahun yang tinggal di rumah yang menerima air dari sumur yang mengandung 610 μg Mn/L; harus terdapat kontrol di rumah yang menerima air dari sumur yang mengandung 160 μg Mn/L. Anak-anak dalam kelompok eksperimen ini menunjukkan peningkatan perilaku hiperaktif dan menentang.<ref name="Bouchard 138–143" /> |
|||
Konsentrasi aman maksimum saat ini berdasarkan peraturan EPA adalah 50 μg Mn/L.<ref name="EPA drinking water">{{cite web|title=Drinking Water Contaminants|url=http://water.epa.gov/drink/contaminants/index.cfm|publisher=US EPA|access-date=28 Juni 2023}}</ref> |
|||
===Penyakit neurodegeneratif=== |
|||
Sebuah protein yang disebut [[DMT1]] adalah pengangkut utama dalam penyerapan mangan dari usus, dan mungkin merupakan pengangkut utama mangan melintasi [[sawar darah otak|sawar darah–otak]]. DMT1 juga mengangkut mangan yang dihirup melintasi epitel hidung. Mekanisme yang diusulkan untuk toksisitas mangan adalah bahwa disregulasi akan menyebabkan stres oksidatif, disfungsi mitokondria, [[eksitotoksisitas]] yang dimediasi glutamat, dan agregasi protein.<ref>{{Cite journal|last1=Prabhakaran|first1=K.|last2=Ghosh|first2=D.|last3=Chapman|first3=G.D.|last4=Gunasekar|first4=P.G.|date=2008|title=Molecular mechanism of manganese exposure-induced dopaminergic toxicity|journal=Brain Research Bulletin|volume=76|issue=4|pages=361–367|doi=10.1016/j.brainresbull.2008.03.004|pmid=18502311|s2cid=206339744|issn=0361-9230}}</ref> |
|||
==Lihat pula== |
|||
* [[Eksportir mangan]], protein transpor membran |
|||
* [[Daftar negara menurut produksi mangan]] |
|||
* [[Pelapisan konversi fosfat#Parkerisasi|Parkerisasi]] |
|||
==Referensi== |
|||
{{Reflist|30em}} |
|||
==Pranala luar== |
|||
{{Commons|Manganese}} |
|||
{{Wiktionary|mangan}} |
|||
* {{en}} [http://www.npi.gov.au/substances/manganese/index.html National Pollutant Inventory – Lembar Fakta Mangan dan Senyawanya] |
|||
* {{en}} [http://www.manganese.org Institut Mangan Internasional] |
|||
* {{en}} [https://www.cdc.gov/niosh/topics/manganese/ Halaman Topik Mangan NIOSH] |
|||
* {{en}} [http://www.periodicvideos.com/videos/025.htm Mangan] di ''[[The Periodic Table of Videos]]'' (Universitas Nottingham) |
|||
* {{en}} [https://www.manganese-dendrite.com Semua tentang Dendrit Mangan] |
|||
* {{en}} [https://www.epa.gov/smm/electric-arc-furnace-eaf-slag Terak Tanur Busur Listrik (EAF)] |
|||
{{Tabel periodik unsur kimia}} |
|||
{{Senyawa mangan}} |
|||
{{Authority control}} |
|||
[[Kategori:Mangan| ]] |
|||
[[Kategori:Unsur kimia]] |
[[Kategori:Unsur kimia]] |
||
[[Kategori:Logam transisi]] |
[[Kategori:Logam transisi]] |
||
[[Kategori: |
[[Kategori:Deoksidator]] |
||
[[Kategori:Kesehatan dan keselamatan kerja]] |
|||
[[Kategori:Mineral makanan]] |
|||
[[Kategori:Reduktor]] |
|||
[[Kategori:Unsur kimia dengan struktur kubus berpusat-badan]] |
|||
[[Kategori:Mineral unsur asli]] |
|||
Revisi terkini sejak 10 April 2024 19.02
25Mn Mangan | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Kubus mangan murni dan potongan mangan teroksidasi | ||||||||||||||||||||||||||||||||
Garis spektrum mangan | ||||||||||||||||||||||||||||||||
| Sifat umum | ||||||||||||||||||||||||||||||||
| Pengucapan | /mangan/[1] | |||||||||||||||||||||||||||||||
| Penampilan | metalik keperakan | |||||||||||||||||||||||||||||||
| Mangan dalam tabel periodik | ||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 25 | |||||||||||||||||||||||||||||||
| Golongan | golongan 7 | |||||||||||||||||||||||||||||||
| Periode | periode 4 | |||||||||||||||||||||||||||||||
| Blok | blok-d | |||||||||||||||||||||||||||||||
| Kategori unsur | logam transisi | |||||||||||||||||||||||||||||||
| Berat atom standar (Ar) |
| |||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Ar] 4s2 3d5 | |||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 13, 2 | |||||||||||||||||||||||||||||||
| Sifat fisik | ||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | |||||||||||||||||||||||||||||||
| Titik lebur | 1519 K (1246 °C, 2275 °F) | |||||||||||||||||||||||||||||||
| Titik didih | 2334 K (2061 °C, 3742 °F) | |||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 7,21 g/cm3 | |||||||||||||||||||||||||||||||
| saat cair, pada t.l. | 5,95 g/cm3 | |||||||||||||||||||||||||||||||
| Kalor peleburan | 12,91 kJ/mol | |||||||||||||||||||||||||||||||
| Kalor penguapan | 221 kJ/mol | |||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 26,32 J/(mol·K) | |||||||||||||||||||||||||||||||
Tekanan uap
| ||||||||||||||||||||||||||||||||
| Sifat atom | ||||||||||||||||||||||||||||||||
| Bilangan oksidasi | −3, −2, −1, 0, +1, +2, +3, +4, +5, +6, +7 (tergantung pada bilangan oksidasinya, oksida asam, basa, atau amfoter) | |||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 1,55 | |||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 717,3 kJ/mol ke-2: 1509,0 kJ/mol ke-3: 3248 kJ/mol (artikel) | |||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 127 pm | |||||||||||||||||||||||||||||||
| Jari-jari kovalen | Spin rendah: 139±5 pm Spin tinggi: 161±8 pm | |||||||||||||||||||||||||||||||
| Lain-lain | ||||||||||||||||||||||||||||||||
| Kelimpahan alami | primordial | |||||||||||||||||||||||||||||||
| Struktur kristal | kubus berpusat badan (bcc) | |||||||||||||||||||||||||||||||
| Kecepatan suara batang ringan | 5150 m/s (suhu 20 °C) | |||||||||||||||||||||||||||||||
| Ekspansi kalor | 21,7 µm/(m·K) (suhu 25 °C) | |||||||||||||||||||||||||||||||
| Konduktivitas termal | 7,81 W/(m·K) | |||||||||||||||||||||||||||||||
| Resistivitas listrik | 1,44 µΩ·m (suhu 20 °C) | |||||||||||||||||||||||||||||||
| Arah magnet | paramagnetik | |||||||||||||||||||||||||||||||
| Suseptibilitas magnetik molar | (α) +529,0×10−6 cm3/mol (293 K)[2] | |||||||||||||||||||||||||||||||
| Modulus Young | 198 GPa | |||||||||||||||||||||||||||||||
| Modulus curah | 120 GPa | |||||||||||||||||||||||||||||||
| Skala Mohs | 6,0 | |||||||||||||||||||||||||||||||
| Skala Brinell | 196 MPa | |||||||||||||||||||||||||||||||
| Nomor CAS | 7439-96-5 | |||||||||||||||||||||||||||||||
| Sejarah | ||||||||||||||||||||||||||||||||
| Penemuan | Carl W. Scheele (1774) | |||||||||||||||||||||||||||||||
| Isolasi pertama | Johann G. Gahn (1774) | |||||||||||||||||||||||||||||||
| Isotop mangan yang utama | ||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||
Mangan, batu kawi, atau bekawi adalah sebuah unsur kimia dengan lambang Mn dan nomor atom 25. Ia adalah logam yang keras, rapuh, dan berwarna keperakan yang sering ditemukan dalam mineral yang dikombinasikan dengan besi. Mangan adalah sebuah logam transisi dengan beragam penggunaan paduan industri, khususnya baja nirkarat. Ia dapat meningkatkan kekuatan, kemampuan kerja, dan ketahanan aus. Mangan oksida digunakan sebagai zat pengoksidasi; sebagai aditif karet; serta dalam pembuatan kaca, pupuk, dan keramik. Mangan sulfat dapat digunakan sebagai fungisida.
Mangan juga merupakan unsur makanan manusia yang penting, penting dalam metabolisme makronutrien, pembentukan tulang, dan sistem pertahanan radikal bebas. Ia adalah komponen penting dalam lusinan protein dan enzim.[3] Sebagian besar mangan ditemukan di tulang, tetapi juga di hati, ginjal, dan otak.[4] Di otak manusia, mangan terikat pada metaloprotein mangan, terutama glutamin sintetase dalam astrosit.
Mangan pertama kali diisolasi pada tahun 1774. Ia dikenal di laboratorium dalam bentuk garam kalium permanganat berwarna lembayung tua. Ia terjadi di sisi aktif pada beberapa enzim.[5] Salah satu hal yang menarik adalah penggunaan sebuah gugus Mn–O, kompleks yang mengembangkan oksigen, dalam produksi oksigen oleh tumbuhan.
Karakteristik
[sunting | sunting sumber]Sifat fisik
[sunting | sunting sumber]Mangan adalah sebuah logam berwarna abu-abu keperakan yang menyerupai besi. Logam ini keras dan sangat rapuh, sulit melebur, tetapi mudah teroksidasi.[6] Logam mangan dan ionnya yang umum bersifat paramagnetik.[7] Mangan akan ternoda perlahan di udara dan teroksidasi ("berkarat") seperti besi dalam air yang mengandung oksigen terlarut.[butuh rujukan]
Isotop
[sunting | sunting sumber]Mangan alami terdiri dari satu isotop stabil, 55Mn. Beberapa radioisotop telah diisolasi dan dijelaskan, dengan berat atom mulai dari 46 u (46Mn) hingga 72 u (72Mn). Isotop yang paling stabil adalah 53Mn dengan waktu paruh 3,7 juta tahun, 54Mn dengan waktu paruh 312,2 hari, dan 52Mn dengan waktu paruh 5,591 hari. Semua isotop radioaktif yang tersisa memiliki waktu paruh kurang dari 3 jam, dan sebagian besar kurang dari 1 menit. Mode peluruhan utama dari isotop yang lebih ringan daripada isotop stabil yang paling melimpah, 55Mn, adalah penangkapan elektron dan mode utama dari isotop yang lebih berat adalah peluruhan beta.[8] Mangan juga memiliki tiga keadaan meta.[8]
Mangan adalah bagian dari unsur-unsur gugus besi, yang diperkirakan disintesis di bintang besar sesaat sebelum ledakan supernova.[9] 53Mn meluruh menjadi 53Cr dengan waktu paruh 3,7 juta tahun. Karena waktu paruhnya yang relatif pendek, 53Mn relatif jarang, dihasilkan oleh tumbukan sinar kosmik pada besi.[10] Kandungan isotop mangan biasanya digabungkan dengan kandungan isotop kromium dan telah memiliki aplikasi dalam geologi isotop dan penanggalan radiometrik. Rasio isotop Mn–Cr memperkuat bukti dari 26Al dan 107Pd untuk sejarah awal Tata Surya. Variasi dalam rasio 53Cr/52Cr dan Mn/Cr dari beberapa meteorit menunjukkan rasio awal 53Mn/55Mn, yang menunjukkan bahwa komposisi isotop Mn–Cr harus dihasilkan dari peluruhan in situ dari 53Mn dalam benda planet yang berbeda. Oleh karena itu, 53Mn memberikan bukti tambahan untuk proses nukleosintesis segera sebelum penggabungan Tata Surya.[11][12][13][14]
Alotrop
[sunting | sunting sumber] |
 |
Empat alotrop (bentuk struktural) mangan padat telah diketahui, diberi label α, β, γ dan δ, dan terjadi pada peningkatan suhu secara berturut-turut. Semuanya metalik, stabil pada tekanan standar, dan memiliki kisi kristal kubik, tetapi struktur atomnya sangat bervariasi.[15][16][17]
Mangan alfa (Mn-α) adalah fase kesetimbangan pada suhu kamar. Ia memiliki kisi kubus berpusat-badan dan tidak biasa di antara logam elemental karena memiliki sel unit yang sangat kompleks, dengan 58 atom per sel (29 atom per sel unit sederhana) dalam empat jenis lokasi yang berbeda.[15][18] Ia bersifat paramagnetik pada suhu kamar dan antiferomagnetik pada suhu di bawah 95 K (−178 °C).[19]
 |
Mangan beta (Mn-β) terbentuk ketika dipanaskan di atas suhu transisi (973 K (700 °C; 1.290 °F)). Ia memiliki struktur kubus sederhana dengan 20 atom per sel unit di dua jenis lokasi, yang sama rumitnya dengan logam elemental lainnya.[20] Ia mudah diperoleh sebagai fase metastabil pada suhu kamar melalui pendinginan cepat. Ia tidak menunjukkan pengarahan magnetik, akan tetap bersifat paramagnetik hingga suhu terendah yang diukur (1,1 K).[20][21][22]
Mangan gama (Mn-γ) terbentuk ketika dipanaskan di atas suhu 1.370 K (1.100 °C; 2.010 °F). Ia memiliki struktur kubus berpusat-muka sederhana (empat atom per sel unit). Ketika didinginkan ke suhu kamar, ia akan berubah menjadi Mn-β, tetapi ia dapat distabilkan pada suhu kamar dengan memadukannya dengan setidaknya 5 persen unsur lain (seperti C, Fe, Ni, Cu, Pd atau Au), dan paduan yang distabilkan larutan ini akan terdistorsi menjadi struktur tetragon berpusat-muka.[22][23]
Mangan delta (Mn-δ) terbentuk ketika dipanaskan di atas suhu 1.406 K (1.130 °C; 2.070 °F) dan stabil hingga titik lebur mangan sebesar 1.519 K (1.250 °C; 2.270 °F). Ia memiliki struktur kubus berpusat-badan (dua atom per sel unit kubus).[16][22]
Senyawa
[sunting | sunting sumber]
Keadaan oksidasi umum mangan adalah +2, +3, +4, +6, dan +7, meskipun semua keadaan oksidasi dari −3 hingga +7 telah diamati. Mangan dalam keadaan oksidasi +7 diwakili oleh garam dari anion permanganat MnO4− yang berwarna sangat ungu. Kalium permanganat adalah sebuah reagen laboratorium yang umum digunakan karena sifat pengoksidasinya; ia digunakan sebagai obat topikal (misalnya, dalam pengobatan penyakit ikan). Larutan kalium permanganat adalah salah satu pewarna dan fiksatif pertama yang digunakan dalam persiapan sel dan jaringan biologis untuk mikroskop elektron.[25]
Selain berbagai garam permanganat, Mn(VII) diwakili oleh turunan Mn2O7 yang tidak stabil dan bersifat volatil. Oksihalida (MnO3F dan MnO3Cl) adalah oksidator kuat.[6] Contoh paling menonjol dari Mn dalam keadaan oksidasi +6 adalah anion manganat [MnO4]2- yang berwarna hijau. Garam mangan adalah zat antara dalam ekstraksi mangan dari bijihnya. Senyawa dengan keadaan oksidasi +5 agak sulit dipahami, salah satu contohnya adalah anion hipomanganat [MnO4]3- yang berwarna biru.
Senyawa dengan Mn dalam keadaan oksidasi +5 jarang dijumpai dan sering ditemui berasosiasi dengan ligan oksida (O2-) atau nitrida (N3-).[26][27]
Mn(IV) agak membingungkan karena ia umum di alam tetapi jauh lebih jarang dalam kimia sintetis. Bijih Mn yang paling umum, pirolusit, adalah MnO2. Ia adalah pigmen cokelat tua dari banyak lukisan gua, tetapi juga merupakan bahan umum dalam baterai sel kering. Kompleks Mn(IV) telah dikenal, tetapi mereka membutuhkan ligan yang rumit. Kompleks Mn(IV)-OH merupakan zat antara dalam beberapa enzim, termasuk pusat evolusi oksigen (OEC) pada tumbuhan.[28]
Turunan sederhana Mn+3 jarang ditemukan tetapi dapat distabilkan dengan ligan basa yang sesuai. Mangan(III) asetat adalah oksidan yang berguna dalam sintesis organik. Senyawa padat mangan(III) dicirikan oleh warna ungu-merah yang kuat dan preferensi untuk koordinasi oktahedron yang terdistorsi akibat efek Jahn–Teller.[butuh rujukan]

Keadaan oksidasi yang sangat umum untuk mangan dalam larutan berair adalah +2, yang memiliki warna merah muda pucat. Banyak senyawa mangan(II) yang diketahui, seperti kompleks akuo yang diturunkan dari mangan(II) sulfat (MnSO4) dan mangan(II) klorida (MnCl2). Keadaan oksidasi ini juga terlihat pada mineral rodokrosit (mangan(II) karbonat). Mangan(II) umumnya eksis dengan spin tinggi, S = 5/2 keadaan dasar karena energi pasangan yang tinggi untuk mangan(II). Tidak ada transisi d–d yang diperbolehkan spin dalam mangan(II), yang menjelaskan warnanya yang redup.[29]
| Keadaan oksidasi mangan[30] | |
|---|---|
| 0 | Mn2(CO)10 |
| +1 | MnC5H4CH3(CO)3 |
| +2 | MnCl2, MnCO3, MnO |
| +3 | MnF3, Mn(OAc)3, Mn2O3 |
| +4 | MnO2 |
| +5 | K3MnO4 |
| +6 | K2MnO4 |
| +7 | KMnO4, Mn2O7 |
| Keadaan oksidasi yang umum dicetak tebal. | |
Senyawa organomangan
[sunting | sunting sumber]Mangan membentuk berbagai macam turunan organologam, yaitu senyawa dengan ikatan Mn–C. Turunan organologam mencakup banyak contoh Mn dalam keadaan oksidasi yang lebih rendah, yaitu Mn(-III) hingga Mn(I). Bidang kimia organologam ini dinilai menarik karena Mn tidak mahal dan toksisitasnya relatif rendah.[butuh rujukan]
Minat komersial terbesar adalah "MMT", metilsiklopentadienil mangan trikarbonil, yang digunakan sebagai sebuah senyawa antiketuk yang ditambahkan pada bensin di beberapa negara. Ia memiliki Mn(I). Konsisten dengan aspek kimia Mn(II) lainnya, manganosena (Mn(C
5H
5)
2) memiliki spin tinggi. Sebaliknya, logam tetangganya besi membentuk turunan spin rendah yang stabil di udara dalam bentuk ferosena (Fe(C
5H
5)
2). Ketika dilakukan di bawah atmosfer karbon monoksida, reduksi garam Mn(II) akan menghasilkan dimangan dekakarbonil Mn
2(CO)
10, sebuah padatan berwarna jingga dan volatil. Stabilitas udara dari senyawa Mn(0) ini (dan banyak turunannya) mencerminkan sifat akseptor elektron yang kuat dari karbon monoksida. Banyak kompleks alkena dan kompleks alkuna diturunkan dari Mn
2(CO)
10.[butuh rujukan]
Dalam Mn(CH3)2(dmpe)2, Mn(II) memiliki spin rendah, yang kontras dengan karakter spin tinggi dari prekursornya, MnBr2(dmpe)2 (dmpe = (CH3)2PCH2CH2P(CH3)2).[31] Turunan polialkil dan poliaril dari mangan sering berada pada keadaan oksidasi yang lebih tinggi, mencerminkan sifat pelepasan elektron dari ligan alkil dan aril. Salah satu contohnya adalah [Mn(CH3)6]2-.[butuh rujukan]
Sejarah
[sunting | sunting sumber]Asal usul nama mangan memang kompleks. Pada zaman kuno, dua mineral hitam diidentifikasi dari wilayah Magnetes (antara Magnesia, yang terletak di Yunani modern, atau Magnesia ad Sipylum, yang terletak di Turki modern).[32] Keduanya disebut magnes dari tempat asalnya, tetapi dianggap berbeda jenis kelamin. Magnes jantan dapat menarik besi, dan bijih besi sekarang dikenal sebagai batu magnet atau magnetit, dan yang mungkin memberi kita istilah magnet. Bijih magnes betina tidak menarik besi, tetapi digunakan untuk menghilangkan warna kaca. Magnes betina ini kemudian disebut magnesia, yang sekarang dikenal di zaman modern sebagai pirolusit atau mangan dioksida.[butuh rujukan] Baik mineral maupun mangan elemental ini tidak bersifat magnetis. Pada abad ke-16, mangan dioksida disebut manganesum (perhatikan adanya dua N, bukan satu) oleh pembuat kaca, mungkin sebagai korupsi dan gabungan dari dua kata, karena ahli alkimia dan pembuat kaca akhirnya harus membedakan magnesia nigra (bijih hitam) dari magnesia alba (bijih putih, juga dari Magnesia, yang juga berguna dalam pembuatan kaca). Michele Mercati menyebut magnesia nigra sebagai manganesa, dan akhirnya logam yang diisolasi darinya dikenal sebagai manganese (bahasa Indonesia: Mangan). Nama magnesia akhirnya digunakan untuk merujuk hanya pada magnesia alba (magnesium oksida) putih, yang memberi nama magnesium untuk unsur bebasnya ketika diisolasi beberapa waktu kemudian.[33]

Mangan dioksida yang melimpah di alam telah lama digunakan sebagai pigmen. Lukisan gua di Gargas yang berusia 30.000 hingga 24.000 tahun terbuat dari mineral berupa pigmen MnO2.[35]
Senyawa mangan digunakan oleh pembuat kaca di Mesir dan Romawi, baik untuk menambah, atau menghilangkan, warna dari kaca.[36] Penggunaannya sebagai "sabun pembuat kaca" berlanjut hingga Abad Pertengahan hingga zaman modern dan terbukti dalam kaca abad ke-14 dari Venesia.[37]

Karena digunakan dalam pembuatan kaca, mangan dioksida tersedia untuk percobaan oleh beberapa ahli alkimia, kimiawan pertama. Ignatius G. Kaim (1770) dan Johann R. Glauber (abad ke-17) menemukan bahwa mangan dioksida dapat diubah menjadi permanganat, sebuah reagen laboratorium yang berguna.[38] Pada pertengahan abad ke-18, kimiawan Swedia Carl W. Scheele menggunakan mangan dioksida untuk menghasilkan klorin. Pertama, asam klorida, atau campuran asam sulfat encer dan natrium klorida dibuat untuk bereaksi dengan mangan dioksida, dan kemudian asam klorida dari proses Leblanc digunakan, dan mangan dioksida didaur ulang melalui proses Weldon. Produksi zat pemutih klorin dan hipoklorit merupakan konsumen bijih mangan yang besar.[butuh rujukan]
Scheele dan yang lainnya menyadari bahwa pirolusit (bentuk mineral mangan dioksida) mengandung sebuah unsur baru. Johan G. Gahn adalah orang pertama yang mengisolasi sampel logam mangan yang tidak murni pada tahun 1774, yang dilakukannya dengan mereduksi mangan dioksida dengan karbon.[butuh rujukan]
Kandungan mangan dari beberapa bijih besi yang digunakan di Yunani menimbulkan spekulasi bahwa baja yang dihasilkan dari bijih tersebut mengandung mangan tambahan, membuat baja Sparta sangatlah keras.[39] Sekitar awal abad ke-19, mangan digunakan dalam pembuatan baja dan beberapa paten diberikan. Pada tahun 1816, didokumentasikan bahwa paduan besi dengan mangan lebih keras tetapi tidak lebih rapuh. Pada tahun 1837, akademisi Inggris James Couper mencatat hubungan antara paparan berat mangan pada penambang dan bentuk penyakit Parkinson.[40] Pada tahun 1912, paten Amerika Serikat diberikan untuk melindungi senjata api dari karat dan korosi dengan pelapisan konversi elektrokimia mangan fosfat, dan proses tersebut telah digunakan secara luas sejak saat itu.[41]
Penemuan sel Leclanché pada tahun 1866 dan perbaikan baterai selanjutnya yang mengandung mangan dioksida sebagai depolarisator katodik meningkatkan permintaan mangan dioksida. Hingga pengembangan baterai dengan nikel–kadmium dan litium, sebagian besar baterai mengandung mangan. Baterai seng–karbon dan baterai alkalin biasanya menggunakan mangan dioksida yang diproduksi secara industri karena mangan dioksida alami mengandung kotoran. Pada abad ke-20, mangan dioksida banyak digunakan sebagai katodik untuk baterai kering sekali pakai komersial baik tipe standar (seng–karbon) maupun alkalin.[42]
Keterjadian
[sunting | sunting sumber]Mangan menyusun sekitar 1000 ppm (0,1%) kerak Bumi, menjadi unsur kerak Bumi yang paling melimpah ke-12.[4] Tanah mengandung 7–9000 ppm mangan dengan rata-rata 440 ppm.[4] Atmosfer mengandung 0,01 μg/m3.[4] Mangan terjadi terutama sebagai pirolusit (MnO2), braunit (Mn2+Mn3+6)SiO12),[43] psilomelan (Ba,H
2O)
2Mn
5O
10, dan pada tingkat yang lebih rendah sebagai rodokrosit (MnCO3).
 |
 |
 |
 |
 |
| Bijih mangan | Psilomelan (bijih mangan) | Spiegeleisen adalah sebuah paduan besi dengan kandungan mangan sekitar 15% | Dendrit mangan oksida pada batu gamping dari Solnhofen, Jerman – sejenis pseudofosil. Skala dalam mm | Mineral rodokrosit (mangan(II) karbonat) |

Bijih mangan yang paling penting adalah pirolusit (MnO2). Bijih mangan lain yang penting secara ekonomi biasanya menunjukkan hubungan spasial yang dekat dengan bijih besi, seperti sfalerit.[6][45] Sumber daya berbasis lahan berjumlah besar tetapi didistribusikan secara tidak teratur. Sekitar 80% dari sumber mangan dunia yang diketahui terdapat di Afrika Selatan; endapan mangan penting lainnya terdapat di Ukraina, Australia, India, Tiongkok, Gabon, dan Brasil.[44] Menurut perkiraan tahun 1978, dasar lautan memiliki 500 miliar ton nodul mangan.[46] Upaya untuk menemukan metode pemanenan nodul mangan yang layak secara ekonomi ditinggalkan pada tahun 1970-an.[47]
Di Afrika Selatan, endapan yang paling teridentifikasi terletak di dekat Hotazel di Provinsi Northern Cape (ladang mangan Kalahari), dengan perkiraan tahun 2011 sebesar 15 miliar ton. Pada tahun 2011, Afrika Selatan menghasilkan 3,4 juta ton, melampaui semua negara lain.[48]
Mangan ditambang terutama di Afrika Selatan, Australia, Tiongkok, Gabon, Brasil, India, Kazakhstan, Ghana, Ukraina, dan Malaysia.[49]
Produksi
[sunting | sunting sumber]Untuk produksi feromangan, bijih mangan dicampur dengan bijih besi dan karbon, dan kemudian direduksi baik dalam tanur tiup atau tanur busur listrik.[50] Feromangan yang dihasilkan memiliki kandungan mangan 30 hingga 80%.[6] Mangan murni yang digunakan untuk produksi paduan bebas besi diproduksi dengan melindi bijih mangan dengan asam sulfat dan proses elektrodeposisi berikutnya.[51]

Proses ekstraksi yang lebih progresif melibatkan pereduksian bijih mangan (kadar rendah) secara langsung melalui pelindian timbunan. Ini dilakukan dengan memerkolasi gas alam melalui dasar tumpukan; gas alam menyediakan panas (perlu setidaknya 850 °C) dan zat pereduksi (karbon monoksida). Ini akan mereduksi semua bijih mangan menjadi mangan oksida (MnO), yang merupakan bentuk yang dapat dilindi. Bijih kemudian bergerak melalui sebuah sirkuit penggilingan untuk mengurangi ukuran partikel bijih menjadi antara 150 dan 250 μm, meningkatkan luas permukaan untuk membantu pelindian. Bijih tersebut kemudian ditambahkan ke dalam tangki pelindian asam sulfat dan ion fero (Fe2+) dengan perbandingan 1,6:1. Besi kemudian bereaksi dengan mangan dioksida (MnO2) untuk membentuk besi hidroksida (FeO(OH)) dan mangan elemental (Mn).[butuh rujukan]
Proses ini menghasilkan sekitar 92% pemulihan mangan. Untuk pemurnian lebih lanjut, mangan kemudian dapat dikirim ke sebuah fasilitas elektrodeposisi.[52]
Pada tahun 1972, Proyek Azorian CIA, melalui miliarder Howard Hughes, menugaskan kapal Hughes Glomar Explorer dengan "cerita sampul" memanen nodul mangan dari dasar laut.[53] Hal itu memicu kesibukan untuk mengumpulkan nodul mangan, yang sebenarnya tidak praktis. Misi sebenarnya dari Hughes Glomar Explorer adalah mengangkat kapal selam Soviet yang tenggelam, K-129, dengan tujuan mengambil buku kode Soviet.[54]
Sumber daya mangan yang melimpah berupa nodul mangan yang ditemukan di dasar laut.[55][56] Nodul-nodul ini, yang terdiri dari 29% mangan,[57] terletak di sepanjang dasar laut dan dampak potensial penambangan nodul-nodul ini sedang diteliti. Dampak lingkungan fisik, kimia, dan biologis dapat terjadi karena penambangan nodul ini mengganggu dasar laut dan menyebabkan terbentuknya gumpalan sedimen. Suspensi ini meliputi logam dan nutrisi anorganik, yang dapat menyebabkan kontaminasi perairan dekat dasar dari senyawa beracun terlarut. Nodul mangan juga merupakan tempat merumput, ruang hidup, dan perlindungan untuk sistem endo- dan epifauna. Ketika nodul ini dihilangkan, sistem ini secara langsung akan terpengaruh. Secara keseluruhan, hal ini dapat menyebabkan spesies meninggalkan area tersebut atau mati total.[58] Sebelum dimulainya penambangan itu sendiri, penelitian sedang dilakukan oleh badan-badan afiliasi Perserikatan Bangsa-Bangsa dan perusahaan yang disponsori negara dalam upaya untuk memahami sepenuhnya dampak lingkungan dengan harapan dapat mengurangi dampak tersebut.[59]
Lingkungan lautan
[sunting | sunting sumber]Banyak unsur renik di lautan berasal dari partikel hidrotermal yang kaya logam dari ventilasi hidrotermal.[60] Mangan terlarut (dMn) ditemukan di seluruh lautan dunia, 90% di antaranya berasal dari lubang hidrotermal.[61] Partikulat Mn berkembang dalam gumpalan apung di atas sumber ventilasi aktif, sedangkan dMn berperilaku secara konservatif.[60] Konsentrasi Mn bervariasi antara kolom air laut. Di permukaan, dMn terangkat karena masukan dari sumber eksternal seperti sungai, debu, dan sedimen landas. Sedimen pesisir biasanya memiliki konsentrasi Mn yang lebih rendah, tetapi dapat meningkat akibat pembuangan antropogenik dari industri seperti pertambangan dan pabrik baja, yang masuk ke laut dari input sungai. Konsentrasi dMn permukaan juga dapat ditingkatkan secara biologis melalui fotosintesis dan secara fisik dari pembalikan massa air pantai dan arus permukaan yang digerakkan oleh angin. Siklus internal seperti fotoreduksi dari radiasi UV juga dapat meningkatkan level dengan mempercepat disolusi Mn-oksida dan pemulungan oksidatif, mencegah Mn tenggelam ke perairan yang lebih dalam.[62] Tingkat yang lebih tinggi di pertengahan kedalaman dapat terjadi di dekat pegunungan tengah laut dan ventilasi hidrotermal. Ventilasi hidrotermal melepaskan cairan yang diperkaya dMn ke dalam air. dMn kemudian dapat melakukan perjalanan hingga 4.000 km karena adanya kapsul mikroba, mencegah pertukaran dengan partikel, menurunkan tingkat penenggelaman. Konsentrasi Mn terlarut bahkan lebih tinggi ketika kadar oksigen rendah. Secara keseluruhan, konsentrasi dMn biasanya lebih tinggi di wilayah pesisir dan akan menurun saat bergerak ke lepas pantai.[62]
Tanah
[sunting | sunting sumber]Mangan terjadi di tanah dalam tiga keadaan oksidasi: kation divalen, Mn2+ serta sebagai oksida hitam kecokelatan dan hidroksida yang mengandung Mn(III,IV), seperti MnOOH dan MnO2. Kondisi pH tanah dan oksidasi-reduksi akan memengaruhi yang mana dari ketiga bentuk Mn ini yang dominan dalam tanah tertentu. Pada pH kurang dari 6 atau dalam kondisi anaerobik, Mn(II) mendominasi, sedangkan pada kondisi yang lebih basa dan aerobik, Mn(III,IV) oksida dan hidroksida mendominasi. Efek keasaman tanah dan keadaan aerasi pada bentuk Mn ini dapat dimodifikasi atau dikendalikan oleh aktivitas mikroba. Respirasi mikroba dapat menyebabkan oksidasi Mn2+ menjadi mangan oksida, dan dapat menyebabkan reduksi oksida tersebut menjadi kation divalen.[63]
Oksida Mn(III,IV) terdapat sebagai noda hitam kecokelatan dan nodul kecil pada partikel pasir, lanau, dan lempung. Lapisan permukaan pada partikel tanah lainnya ini memiliki luas permukaan yang tinggi dan membawa muatan negatif. Sisi bermuatan dapat menyerap dan mempertahankan berbagai kation, terutama logam berat (misalnya Cr3+, Cu2+, Zn2+, dan Pb2+). Selain itu, oksida tersebut dapat menyerap asam organik dan senyawa lainnya. Adsorpsi logam dan senyawa organik kemudian dapat menyebabkannya teroksidasi sedangkan oksida Mn(III,IV) direduksi menjadi Mn2+ (misalnya Cr3+ menjadi Cr(VI) dan hidrokuinon tidak berwarna menjadi polimer kuinon berwarna teh).[64]
Aplikasi
[sunting | sunting sumber]Mangan tidak memiliki pengganti yang memuaskan dalam aplikasi utamanya dalam metalurgi.[44] Dalam aplikasi kecil (misalnya pemfosfatan mangan), seng dan kadang-kadang vanadium adalah pengganti yang layak.
Baja
[sunting | sunting sumber]
Mangan sangat penting untuk produksi baja dan besi berdasarkan sifat pengikat belerang, deoksidasi, dan pemaduannya, seperti yang pertama kali diakui oleh ahli metalurgi Inggris Robert F. Mushet (1811–1891) yang, pada tahun 1856, memperkenalkan unsur tersebut, dalam bentuk spiegeleisen, menjadi baja untuk tujuan khusus untuk menghilangkan kelebihan oksigen, belerang, dan fosforus terlarut untuk meningkatkan kelenturannya. Pembuatan baja,[65] termasuk komponen pembuatan besinya, telah menyumbang sebagian besar permintaan mangan, saat ini berkisar antara 85% sampai 90% dari total permintaan.[51] Mangan adalah komponen utama dari baja nirkarat berbiaya rendah.[66][67] Seringkali feromangan (biasanya sekitar 80% mangan) menjadi zat antara dalam proses modern.
Sejumlah kecil mangan dapat meningkatkan kemampuan kerja baja pada suhu tinggi dengan membentuk sulfida dengan titik lebur tinggi dan mencegah pembentukan besi sulfida cair pada batas butir. Jika kandungan mangan mencapai 4%, kegetasan baja menjadi ciri yang dominan. Penggetasan akan menurun pada konsentrasi mangan yang lebih tinggi dan mencapai tingkat yang dapat diterima pada 8%. Baja yang mengandung 8 hingga 15% mangan memiliki kekuatan tarik yang tinggi hingga 863 MPa.[68][69] Baja dengan mangan 12% ditemukan pada tahun 1882 oleh Robert Hadfield dan masih dikenal sebagai baja Hadfield (mangaloi). Baja ini digunakan untuk helm baja militer Britania Raya dan kemudian oleh militer Amerika Serikat.[70]
Paduan aluminium
[sunting | sunting sumber]Mangan digunakan dalam produksi beberapa paduan dengan aluminium. Aluminium dengan sekitar 1,5% mangan dapat meningkatkan ketahanan terhadap korosi melalui butiran yang menyerap kotoran yang akan menyebabkan korosi galvanik.[71] Paduan aluminium tahan korosi 3004 dan 3104 (0,8 hingga 1,5% mangan) digunakan untuk sebagian besar kaleng minuman.[72] Sebelum tahun 2000, lebih dari 1,6 juta ton paduan tersebut digunakan; dengan 1% mangan, paduan ini menghabiskan 16.000 ton mangan.[Verifikasi gagal][72]
Baterai
[sunting | sunting sumber]Mangan(IV) oksida digunakan pada baterai sel kering tipe asli sebagai akseptor elektron dari seng, dan merupakan bahan kehitaman pada sel senter tipe karbon–seng. Mangan dioksida akan direduksi menjadi mangan oksida-hidroksida MnO(OH) selama pemakaian, mencegah pembentukan hidrogen pada anoda baterai.[73]
- MnO2 + H2O + e− → MnO(OH) + OH−
Bahan yang sama juga berfungsi pada baterai alkalin (biasanya sel baterai) yang lebih baru, yang menggunakan reaksi dasar yang sama, tetapi campuran elektrolitnya berbeda. Pada tahun 2002, lebih dari 230.000 ton mangan dioksida digunakan untuk tujuan ini.[42][73]

Resistor
[sunting | sunting sumber]Paduan tembaga mangan, seperti Manganin, umumnya ditemukan dalam resistor shunt unsur logam yang digunakan untuk mengukur jumlah arus yang relatif besar. Paduan ini memiliki koefisien ketahanan suhu yang sangat rendah dan tahan terhadap belerang. Hal ini membuat paduan ini sangat berguna di lingkungan otomotif dan industri yang keras.[74]
Ceruk
[sunting | sunting sumber]Metilsiklopentadienil mangan trikarbonil adalah sebuah aditif dalam beberapa bensin tanpa timbal untuk meningkatkan nilai oktan dan mengurangi ketukan mesin.[75]
Mangan(IV) oksida (mangan dioksida, MnO2) digunakan sebagai reagen dalam kimia organik untuk oksidasi alkohol benzilik (di mana gugus hidroksil berdekatan dengan sebuah cincin aromatik). Mangan dioksida telah digunakan sejak zaman dahulu untuk mengoksidasi dan menetralkan semburat kehijauan pada kaca dari sejumlah kecil besi pengotor.[37] MnO2 juga digunakan dalam pembuatan oksigen dan klorin serta dalam pengeringan cat hitam. Dalam beberapa pembuatan, ia adalah pigmen cokelat untuk cat dan merupakan penyusun serbuk kopi alami.[76]
Mangan tetravalen digunakan sebagai aktivator dalam fosfor pemancar merah. Walaupun banyak senyawa diketahui dapat menunjukkan luminesensi,[77] mayoritas dari mereka tidak digunakan dalam aplikasi komersial karena efisiensinya rendah atau pancarannya berwarna merah tua.[78][79] Namun, beberapa fluorida teraktivasi Mn4+ dilaporkan sebagai fosfor pemancar merah potensial untuk LED putih-hangat.[80][81] Namun hingga hari ini, hanya K2SiF6:Mn4+ yang tersedia secara komersial untuk digunakan dalam LED putih-hangat.[82]
Logam ini terkadang digunakan dalam koin; hingga tahun 2000, satu-satunya koin Amerika Serikat yang menggunakan mangan adalah nikel "masa perang" dari tahun 1942 hingga 1945.[83] Sebuah paduan 75% tembaga dan 25% nikel secara tradisional digunakan untuk produksi koin nikel. Namun, karena pasokan logam nikel yang terus berkurang selama perang, ia diganti dengan perak dan mangan yang lebih tersedia, sehingga menghasilkan paduan 56% tembaga, 35% perak, dan 9% mangan. Sejak tahun 2000, koin dolar, misalnya dolar Sacagawea dan koin Presiden $1, dibuat dari kuningan yang mengandung 7% mangan dengan inti tembaga murni.[84] Dalam kedua kasus nikel dan dolar, penggunaan mangan dalam koin ini adalah untuk menduplikasi sifat elektromagnetik dari koin berukuran dan bernilai identik sebelumnya dalam mekanisme mesin penjual otomatis. Dalam kasus koin dolar A.S. selanjutnya, paduan mangan dimaksudkan untuk menduplikasi sifat paduan tembaga/nikel yang digunakan dalam dolar Susan B. Anthony.
Senyawa mangan telah digunakan sebagai pigmen dan pewarna keramik dan kaca. Warna cokelat pada keramik terkadang merupakan hasil dari senyawa mangan.[85] Dalam industri kaca, senyawa mangan digunakan untuk dua efek. Mangan(III) akan bereaksi dengan besi(II) untuk mengurangi warna hijau yang kuat pada kaca dengan membentuk besi(III) yang kurang berwarna dan mangan(II) yang berwarna agak merah muda, mengimbangi sisa warna besi(III).[37] Jumlah mangan yang lebih besar digunakan untuk menghasilkan kaca berwarna merah muda. Pada tahun 2009, Profesor Mas Subramanian dan rekannya di Universitas Negeri Oregon menemukan bahwa mangan dapat digabungkan dengan itrium dan indium untuk membentuk pigmen yang sangat biru, tidak beracun, lengai, dan tahan pudar, yaitu biru YInMn, pigmen biru baru pertama yang ditemukan pada tahun 200 terakhir.[butuh rujukan]
Peran biologis
[sunting | sunting sumber]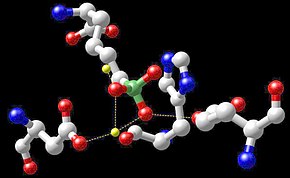
Biokimia
[sunting | sunting sumber]Kelas enzim yang memiliki kofaktor mangan meliputi oksidoreduktase, transferase, hidrolase, liase, isomerase, dan ligase. Enzim lain yang mengandung mangan adalah arginase dan superoksida dismutase yang mengandung Mn (Mn-SOD). Juga, kelas enzim transkriptase balik dari banyak retrovirus (meskipun bukan lentivirus seperti HIV) mengandung mangan. Polipeptida yang mengandung mangan adalah toksin difteri, lektin, dan integrin.[86]
Peran biologis pada manusia
[sunting | sunting sumber]Mangan adalah unsur makanan manusia yang penting. Ia hadir sebagai sebuah koenzim dalam beberapa proses biologis, yang meliputi metabolisme makronutrien, pembentukan tulang, dan sistem pertahanan radikal bebas. Ia adalah komponen penting dalam lusinan protein dan enzim.[3] Tubuh manusia mengandung sekitar 12 mg mangan, kebanyakan di tulang. Sisa jaringan lunak terkonsentrasi di hati dan ginjal.[4] Di otak manusia, mangan terikat pada metaloprotein mangan, terutama glutamin sintetase dalam astrosit.[87]
Nutrisi
[sunting | sunting sumber]| Pria | Wanita | ||
|---|---|---|---|
| Usia | AI (mg/hari) | Usia | AI (mg/hari) |
| 1–3 | 1,2 | 1–3 | 1,2 |
| 4–8 | 1,5 | 4–8 | 1,5 |
| 9–13 | 1,9 | 9–13 | 1,6 |
| 14–18 | 2,2 | 14–18 | 1,6 |
| 19+ | 2,3 | 19+ | 1,8 |
| hamil: 2 | |||
| menyusui: 2,6 | |||
Institut Kedokteran A.S. (IOM) memperbarui Kebutuhan Perkiraan Rata-rata (EAR) dan Angka Kecukupan Gizi (AKG) untuk mineral pada tahun 2001. Untuk mangan, tidak ada informasi yang cukup untuk menetapkan EAR dan AKG, sehingga kebutuhannya digambarkan sebagai perkiraan Asupan Adekuat (AI). Mengenai keamanan, IOM menetapkan Batas Atas Asupan (UL) yang dapat ditoleransi untuk vitamin dan mineral bila bukti cukup. Dalam kasus mangan, UL dewasa ditetapkan pada 11 mg/hari. Secara kolektif EAR, AKG, AI, dan UL disebut sebagai Asupan Referensi Diet (DRI).[88] Kekurangan mangan jarang terjadi.[89]
Otoritas Keamanan Makanan Eropa (EFSA) menyebut kumpulan informasi kolektif tersebut sebagai Nilai Referensi Diet, dengan Asupan Referensi Populasi (PRI) alih-alih AKG, dan Kebutuhan Rata-rata alih-alih EAR. AI dan UL didefinisikan sama seperti di Amerika Serikat. Untuk orang berusia 15 tahun ke atas, AI ditetapkan sebesar 3,0 mg/hari. AI untuk ibu hamil dan menyusui adalah 3,0 mg/hari. Untuk anak usia 1–14 tahun, AI meningkat seiring bertambahnya usia dari 0,5 menjadi 2,0 mg/hari. AI dewasa lebih tinggi dari AKG Amerika Serikat.[90] EFSA meninjau pertanyaan keamanan yang sama dan memutuskan bahwa tidak ada cukup informasi untuk menetapkan UL.[91]
Untuk tujuan pelabelan makanan dan suplemen makanan A.S., jumlah dalam satu porsi dinyatakan sebagai persentase dari Nilai Harian (%DV). Untuk tujuan pelabelan mangan, 100% Nilai Harian adalah 2,0 mg, tetapi pada 27 Mei 2016 direvisi menjadi 2,3 mg agar sesuai dengan AKG.[92][93] Tabel nilai harian dewasa lama dan baru disediakan di Asupan Harian Referensi.
Paparan atau asupan yang berlebihan dapat menyebabkan kondisi yang dikenal sebagai manganisme, sebuah gangguan neurodegeneratif yang dapat menyebabkan kematian neuron dopaminergik dan memiliki gejala yang mirip dengan penyakit Parkinson.[4][94]
Kekurangan mangan
[sunting | sunting sumber]Kekurangan mangan pada manusia, yang jarang terjadi, dapat mengakibatkan sejumlah masalah medis. Kekurangan mangan menyebabkan deformasi tulang pada hewan dan menghambat produksi kolagen dalam penyembuhan luka.[butuh rujukan]
Toksisitas dalam kehidupan laut
[sunting | sunting sumber]Banyak sistem enzimatik membutuhkan Mn untuk berfungsi, tetapi dalam kadar tinggi, Mn dapat menjadi racun. Salah satu alasan lingkungan mengapa tingkat Mn dapat meningkat dalam air laut adalah ketika periode hipoksia terjadi.[95] Sejak tahun 1990, telah ada laporan mengenai akumulasi Mn pada organisme laut meliputi ikan, krustasea, moluska, dan ekinodermata. Jaringan spesifik adalah target pada spesies yang berbeda, meliputi insang, otak, darah, ginjal, dan hati/hepatopankreas. Efek fisiologis telah dilaporkan pada spesies ini. Mn dapat memengaruhi pembaharuan imunosit dan fungsinya, seperti fagositosis dan aktivasi pro-fenoloksidase, menekan sistem kekebalan organisme. Hal ini akan menyebabkan organisme menjadi lebih rentan terhadap infeksi. Saat perubahan iklim terjadi, distribusi patogen akan meningkat, dan agar organisme dapat bertahan hidup dan mempertahankan diri dari patogen ini, mereka memerlukan sistem kekebalan yang sehat dan kuat. Jika sistem mereka dikompromikan dari tingkat Mn yang tinggi, mereka tidak akan mampu melawan patogen ini dan akhirnya mati.[61]
Peran biologis pada bakteri
[sunting | sunting sumber]Mn-SOD adalah jenis SOD yang terdapat pada mitokondria eukariotik, dan juga di sebagian besar bakteri (fakta ini sesuai dengan teori mitokondria berasal dari bakteri). Enzim Mn-SOD mungkin salah satu yang paling kuno, karena hampir semua organisme yang hidup dengan adanya oksigen menggunakannya untuk mengatasi efek racun dari superoksida (O−2), yang terbentuk dari reduksi 1 elektron dioksigen. Pengecualiannya, yang semuanya adalah bakteri, meliputi Lactobacillus plantarum dan laktobasili terkait, yang menggunakan sebuah mekanisme nonenzimatik yang berbeda dengan ion mangan (Mn2+) yang dikomplekskan dengan polifosfat, menunjukkan jalur evolusi untuk fungsi ini dalam kehidupan aerobik.[butuh rujukan]
Peran biologis pada tumbuhan
[sunting | sunting sumber]Mangan juga penting dalam evolusi oksigen fotosintesis dalam kloroplas pada tumbuhan. Kompleks evolusi oksigen (OEC) adalah bagian dari fotosistem II yang terkandung dalam membran tilakoid kloroplas; ia bertanggung jawab atas fotooksidasi terminal air selama reaksi cahaya fotosintesis, dan memiliki inti metaloenzim yang mengandung empat atom mangan.[96][97] Untuk memenuhi persyaratan ini, sebagian besar pupuk tumbuhan berspektrum-luas mengandung mangan.[butuh rujukan]
Pencegahan
[sunting | sunting sumber]| Bahaya | |
|---|---|
| H401 | |
| P273, P501[98] | |
Senyawa mangan kurang beracun dibandingkan dengan logam lain yang tersebar luas, seperti nikel dan tembaga.[99] Namun, paparan debu dan asap mangan tidak boleh melebihi nilai tertinggi sebesar 5 mg/m3 bahkan untuk waktu yang singkat karena tingkat toksisitasnya.[100] Keracunan mangan telah dikaitkan dengan gangguan keterampilan motorik dan gangguan kognitif.[101]
Permanganat menunjukkan toksisitas yang lebih tinggi daripada senyawa mangan(II). Dosis fatalnya ialah sekitar 10 g, dan beberapa keracunan fatal telah terjadi. Efek oksidatifnya yang kuat dapat menyebabkan nekrosis pada selaput lendir. Misalnya, kerongkongan akan terpengaruh jika permanganat tertelan. Hanya sejumlah kecil yang diserap oleh usus, tetapi jumlah kecil ini menunjukkan efek yang parah pada ginjal dan hati.[102][103]
Paparan mangan di Amerika Serikat diatur oleh Administrasi Keselamatan dan Kesehatan Kerja (OSHA).[104] Seseorang dapat terpapar mangan di tempat kerja dengan menghirup atau menelannya. OSHA telah menetapkan batas legal (batas paparan yang diizinkan) untuk paparan mangan di tempat kerja sebesar 5 mg/m3 selama 8 jam hari kerja. Institut Nasional untuk Keselamatan dan Kesehatan Kerja (NIOSH) telah menetapkan batas paparan yang direkomendasikan (REL) sebesar 1 mg/m3 selama 8 jam hari kerja dan batas jangka pendek sebesar 3 mg/m3. Pada kadar 500 mg/m3, mangan langsung berbahaya bagi kehidupan dan kesehatan.[105]
Secara umum, paparan terhadap konsentrasi udara Mn sekitar yang melebihi 5 μg Mn/m3 dapat menyebabkan gejala yang diinduksi oleh Mn. Peningkatan ekspresi protein feroportin dalam sel ginjal embrionik manusia (HEK293) dikaitkan dengan penurunan konsentrasi Mn intraseluler dan sitotoksisitas yang dilemahkan, ditandai dengan pembalikan serapan glutamat yang dikurangi Mn dan berkurangnya kebocoran laktat dehidrogenase.[106]
Masalah kesehatan lingkungan
[sunting | sunting sumber]Dalam air minum
[sunting | sunting sumber]Mangan yang ditularkan melalui air memiliki bioavailabilitas yang lebih besar daripada mangan makanan. Menurut hasil dari penelitian tahun 2010,[107] tingkat paparan mangan yang lebih tinggi dalam air minum dikaitkan dengan peningkatan gangguan intelektual dan penurunan kecerdasan intelektual (IQ) pada anak usia sekolah. Dihipotesiskan bahwa paparan jangka panjang karena menghirup mangan alami dalam air pancuran membuat 8,7 juta orang Amerika berisiko.[108] Namun, data menunjukkan bahwa tubuh manusia dapat pulih dari efek samping tertentu dari paparan berlebih terhadap mangan jika paparan dihentikan dan tubuh dapat membersihkan kelebihannya.[109]
Dalam bensin
[sunting | sunting sumber]
Metilsiklopentadienil mangan trikarbonil (MMT) adalah aditif bensin yang digunakan untuk menggantikan senyawa timbal pada bensin tanpa timbal untuk meningkatkan nilai oktan distilat minyak beroktan rendah. Ia dapat mengurangi agen ketukan mesin melalui aksi gugus karbonil. Bahan bakar yang mengandung mangan cenderung membentuk mangan karbida, yang dapat merusak katup buang. Dibandingkan dengan tahun 1953, saat ini kadar mangan di udara telah menurun.[110]
Dalam asap tembakau
[sunting | sunting sumber]Tumbuhan tembakau dapat dengan mudah menyerap dan mengakumulasi logam berat seperti mangan dari tanah di sekitarnya ke dalam daunnya. Mereka kemudian dihirup selama pengisapan tembakau.[111] Walaupun mangan adalah salah satu konstituen dari asap tembakau,[112] sebagian besar penelitian menyimpulkan bahwa konsentrasinya tidak berbahaya bagi kesehatan manusia.[113]
Peran dalam gangguan neurologis
[sunting | sunting sumber]Manganisme
[sunting | sunting sumber]Paparan mangan berlebih paling sering dikaitkan dengan manganisme, sebuah kelainan neurologis langka yang terkait dengan konsumsi atau inhalasi mangan yang berlebihan. Secara historis, orang yang bekerja dalam produksi atau pemrosesan paduan mangan[114][115] berisiko mengembangkan manganisme; namun, peraturan kesehatan dan keselamatan saat ini telah melindungi para pekerja di negara maju.[104] Gangguan ini pertama kali dijelaskan pada tahun 1837 oleh akademisi Inggris John Couper, yang mempelajari dua pasien yang merupakan penggiling mangan.[40]
Manganisme adalah sebuah gangguan bifasik. Pada tahap awal, orang yang teler mungkin mengalami depresi, perubahan suasana hati, perilaku kompulsif, dan psikosis. Gejala neurologis awal digantikan oleh manganisme tahap akhir, yang menyerupai penyakit Parkinson. Gejala-gejalanya meliputi kelemahan, bicara monoton dan lambat, wajah tanpa ekspresi, tremor, gaya berjalan condong ke depan, ketidakmampuan untuk berjalan mundur tanpa jatuh, kekakuan, serta masalah umum dengan ketangkasan, gaya berjalan dan keseimbangan.[40][116] Tidak seperti penyakit Parkinson, manganisme tidak terkait dengan hilangnya indra penciuman dan pasien biasanya tidak responsif terhadap pengobatan dengan L-DOPA.[117] Gejala manganisme tahap akhir menjadi lebih parah dari waktu ke waktu bahkan jika sumber paparan dihilangkan dan kadar mangan di otak kembali normal.[116]
Paparan mangan kronis telah terbukti menghasilkan penyakit seperti Parkinsonisme yang ditandai dengan kelainan gerakan.[118] Kondisi ini tidak responsif terhadap terhadap terapi tipikal yang digunakan dalam pengobatan PD, menyarankan jalur alternatif selain kehilangan dopaminergik tipikal di dalam substantia nigra.[118] Mangan dapat menumpuk di basal ganglia, menyebabkan gerakan abnormal.[119] Mutasi gen SLC30A10, transporter efluks mangan yang diperlukan untuk menurunkan Mn intraseluler, telah dikaitkan dengan perkembangan penyakit mirip Parkinsonisme ini.[120] Badan Lewy khas untuk PD tidak terlihat pada parkinsonisme yang diinduksi oleh Mn.[119]
Eksperimen pada hewan telah memberikan kesempatan untuk memeriksa konsekuensi dari paparan berlebih mangan dalam kondisi yang terkendali. Pada tikus besar (rat) (yang tidak agresif), mangan akan menginduksi perilaku membunuh-tikus-kecil (mouse-killing).[121]
Gangguan perkembangan anak
[sunting | sunting sumber]Beberapa penelitian baru-baru ini mencoba untuk menguji efek paparan mangan berlebih dosis rendah kronis pada perkembangan anak. Penelitian paling awal dilakukan di provinsi Shanxi, Tiongkok. Air minum di sana telah terkontaminasi melalui irigasi limbah yang tidak tepat dan mengandung 240–350 μg Mn/L. Meskipun konsentrasi Mn pada atau di bawah 300 μg Mn/L dianggap aman pada saat penelitian oleh EPA A.S. dan 400 μg Mn/L oleh Organisasi Kesehatan Dunia, 92 anak yang diambil sampelnya (berusia antara 11 dan 13 tahun) dari provinsi ini menunjukkan kinerja yang lebih rendah pada tes ketangkasan dan kecepatan manual, memori jangka pendek, dan identifikasi visual, dibandingkan dengan anak-anak dari daerah yang tidak terkontaminasi. Baru-baru ini, sebuah penelitian terhadap anak-anak berusia 10 tahun di Bangladesh menunjukkan hubungan antara konsentrasi Mn dalam air sumur dan penurunan skor IQ. Penelitian ketiga yang dilakukan di Quebec meneliti anak sekolah antara usia 6 dan 15 tahun yang tinggal di rumah yang menerima air dari sumur yang mengandung 610 μg Mn/L; harus terdapat kontrol di rumah yang menerima air dari sumur yang mengandung 160 μg Mn/L. Anak-anak dalam kelompok eksperimen ini menunjukkan peningkatan perilaku hiperaktif dan menentang.[107]
Konsentrasi aman maksimum saat ini berdasarkan peraturan EPA adalah 50 μg Mn/L.[122]
Penyakit neurodegeneratif
[sunting | sunting sumber]Sebuah protein yang disebut DMT1 adalah pengangkut utama dalam penyerapan mangan dari usus, dan mungkin merupakan pengangkut utama mangan melintasi sawar darah–otak. DMT1 juga mengangkut mangan yang dihirup melintasi epitel hidung. Mekanisme yang diusulkan untuk toksisitas mangan adalah bahwa disregulasi akan menyebabkan stres oksidatif, disfungsi mitokondria, eksitotoksisitas yang dimediasi glutamat, dan agregasi protein.[123]
Lihat pula
[sunting | sunting sumber]- Eksportir mangan, protein transpor membran
- Daftar negara menurut produksi mangan
- Parkerisasi
Referensi
[sunting | sunting sumber]- ^ (Indonesia) "Mangan". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. hlm. E110. ISBN 0-8493-0464-4.
- ^ a b Erikson, Keith M.; Ascher, Michael (2019). "Chapter 10. Manganese: Its Role in Disease and Health". Dalam Sigel, Astrid; Freisinger, Eva; Sigel, Roland K. O.; Carver, Peggy L. Essential Metals in Medicine:Therapeutic Use and Toxicity of Metal Ions in the Clinic. Metal Ions in Life Sciences. 19. Berlin: de Gruyter GmbH. hlm. 253–266. doi:10.1515/9783110527872-016. ISBN 978-3-11-052691-2. PMID 30855111.
- ^ a b c d e f Emsley, John (2001). "Manganese". Nature's Building Blocks: An A-Z Guide to the Elements. Oxford, UK: Oxford University Press. hlm. 249–253. ISBN 978-0-19-850340-8.
- ^ Roth, Jerome; Ponzoni, Silvia; Aschner, Michael (2013). "Chapter 6 Manganese Homeostasis and Transport". Dalam Banci, Lucia. Metallomics and the Cell. Metal Ions in Life Sciences. 12. Springer. hlm. 169–201. doi:10.1007/978-94-007-5561-1_6. ISBN 978-94-007-5560-4. PMC 6542352
 . PMID 23595673. Buku elektronik ISBN 978-94-007-5561-1.
. PMID 23595673. Buku elektronik ISBN 978-94-007-5561-1.
- ^ a b c d Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). "Mangan". Lehrbuch der Anorganischen Chemie (dalam bahasa Jerman) (edisi ke-91–100). Walter de Gruyter. hlm. 1110–1117. ISBN 978-3-11-007511-3.
- ^ Lide, David R. (2004). Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics. CRC press. ISBN 978-0-8493-0485-9. Diarsipkan dari versi asli
 tanggal 17 Desember 2019. Diakses tanggal 27 Juni 2023.
tanggal 17 Desember 2019. Diakses tanggal 27 Juni 2023.
- ^ a b Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. (2017). "The NUBASE2016 evaluation of nuclear properties" (PDF). Chinese Physics C. 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ^ Clery, Daniel (4 Juni 2020). "The galaxy's brightest explosions go nuclear with an unexpected trigger: pairs of dead stars". Science. Diakses tanggal 27 Juni 2023.
- ^ Schaefer, Jeorg; Faestermann, Thomas; Herzog, Gregory F.; Knie, Klaus; Korschinek, Gunther; Masarik, Jozef; Meier, Astrid; Poutivtsev, Michail; Rugel, Georg; Schlüchter, Christian; Serifiddin, Feride; Winckler, Gisela (2006). "Terrestrial manganese-53 – A new monitor of Earth surface processes". Earth and Planetary Science Letters. 251 (3–4): 334–345. Bibcode:2006E&PSL.251..334S. doi:10.1016/j.epsl.2006.09.016.
- ^ Birck, J.; Rotaru, M.; Allègre, C. (1999). "53Mn-53Cr evolution of the early solar system". Geochimica et Cosmochimica Acta. 63 (23–24): 4111–4117. Bibcode:1999GeCoA..63.4111B. doi:10.1016/S0016-7037(99)00312-9.
- ^ Lugmair, G.; Shukolyukov, A. (1998). "Early solar system timescales according to 53Mn-53Cr systematics". Geochimica et Cosmochimica Acta. 62 (16): 2863–2886. Bibcode:1998GeCoA..62.2863L. doi:10.1016/S0016-7037(98)00189-6.
- ^ Shukolyukov, Alexander; Lugmair, Günter W. (2000). "On The 53Mn Heterogeneity In The Early Solar System". Space Science Reviews. 92: 225–236. Bibcode:2000SSRv...92..225S. doi:10.1023/A:1005243228503.
- ^ Trinquier, A.; Birck, J.; Allègre, C.; Göpel, C.; Ulfbeck, D. (2008). "53Mn–53Cr systematics of the early Solar System revisited". Geochimica et Cosmochimica Acta. 72 (20): 5146–5163. Bibcode:2008GeCoA..72.5146T. doi:10.1016/j.gca.2008.03.023.
- ^ a b c Young, D.A. (1975). "Phase diagrams of the elements". International Nuclear Information System. LNL: 15. Diakses tanggal 27 Juni 2023.
- ^ a b Dhananjayan, N.; Banerjee, T. (1969). Crystallographic modifications of manganese and their transformation characteristics. Chapter 1 of: Structure of Electro-Deposited Manganese. CSIR-NML. hlm. 3–28.
- ^ Kemmitt, R. D. W.; Peacock, R. D. (1973). The Chemistry of Manganese, Technetium and Rhenium. Pergamon Texts in Inorganic Chemistry. Saint Louis: Elsevier Science. hlm. 778. ISBN 978-1-4831-3806-0. OCLC 961064866.
- ^ Bradley, A.J.; Thewlis, J. (1927). "The crystal structure of α-manganese". Proceedings of the Royal Society of London, Series A. 115 (771): 456–471. Bibcode:1927RSPSA.115..456B. doi:10.1098/rspa.1927.0103. ISSN 0950-1207.
- ^ Lawson, A. C.; Larson, Allen C.; Aronson, M. C.; et al. (1994). "Magnetic and crystallographic order in α‐manganese". J. Appl. Phys. 76 (10): 7049–7051. Bibcode:1994JAP....76.7049L. doi:10.1063/1.358024. ISSN 0021-8979.
- ^ a b Prior, Timothy J; Nguyen-Manh, Duc; Couper, Victoria J; Battle, Peter D (2004). "Ferromagnetism in the beta-manganese structure: Fe1.5Pd0.5Mo3N". Journal of Physics: Condensed Matter. 16 (13): 2273–2281. Bibcode:2004JPCM...16.2273P. doi:10.1088/0953-8984/16/13/008. ISSN 0953-8984.
- ^ Funahashi, S.; Kohara, T. (1984). "Neutron diffuse scattering in β‐manganese". J. Appl. Phys. 55 (6): 2048–2050. Bibcode:1984JAP....55.2048F. doi:10.1063/1.333561. ISSN 0021-8979.
- ^ a b c Duschanek, H.; Mohn, P.; Schwarz, K. (1989). "Antiferromagnetic and ferromagnetic gamma-manganese generalisation of the fixed-spin-moment method". Physica B: Condensed Matter. 161 (1–3): 139–142. doi:10.1016/0921-4526(89)90120-8. ISSN 0921-4526.
- ^ Bacon, G E; Cowlam, N (1970). "A study of some alloys of gamma -manganese by neutron diffraction". Journal of Physics C: Solid State Physics. 3 (3): 675–686. Bibcode:1970JPhC....3..675B. doi:10.1088/0022-3719/3/3/023. ISSN 0022-3719.
- ^ "Ch. 20". Shriver and Atkins' Inorganic Chemistry. Oxford University Press. 2010. ISBN 978-0-19-923617-6.
- ^ Luft, J. H. (1956). "Permanganate – a new fixative for electron microscopy". Journal of Biophysical and Biochemical Cytology. 2 (6): 799–802. doi:10.1083/jcb.2.6.799. PMC 2224005
 . PMID 13398447.
. PMID 13398447.
- ^ Man, Wai-Lun; Lam, William W. Y.; Lau, Tai-Chu (2014). "Reactivity of Nitrido Complexes of Ruthenium(VI), Osmium(VI), and Manganese(V) Bearing Schiff Base and Simple Anionic Ligands". Accounts of Chemical Research. 47 (2): 427–439. doi:10.1021/ar400147y. PMID 24047467.
- ^ Goldberg, David P. (2007). "Corrolazines: New Frontiers in High-Valent Metalloporphyrinoid Stability and Reactivity". Accounts of Chemical Research. 40 (7): 626–634. doi:10.1021/ar700039y. PMID 17580977.
- ^ Yano, Junko; Yachandra, Vittal (2014). "Mn4Ca Cluster in Photosynthesis: Where and How Water is Oxidized to Dioxygen". Chemical Reviews. 114 (8): 4175–4205. doi:10.1021/cr4004874. PMC 4002066
 . PMID 24684576.
. PMID 24684576.
- ^ Rayner-Canham, Geoffrey dan Overton, Tina (2003) Descriptive Inorganic Chemistry, Macmillan, hlm. 491, ISBN 0-7167-4620-4.
- ^ Schmidt, Max (1968). "VII. Nebengruppe". Anorganische Chemie II (dalam bahasa Jerman). Wissenschaftsverlag. hlm. 100–109.
- ^ Girolami, Gregory S.; Wilkinson, Geoffrey; Thornton-Pett, Mark; Hursthouse, Michael B. (1983). "Hydrido, alkyl, and ethylene 1,2-bis(dimethylphosphino)ethane complexes of manganese and the crystal structures of MnBr2(dmpe)2, [Mn(AlH4)(dmpe)2]2 and MnMe2(dmpe)2". Journal of the American Chemical Society. 105 (22): 6752–6753. doi:10.1021/ja00360a054.
- ^ languagehat (28 Mei 2005). "MAGNET". languagehat.com (dalam bahasa Inggris). Diakses tanggal 27 Juni 2023.
- ^ Calvert, J. B. (24 Januari 2003). "Chromium and Manganese". Diarsipkan dari versi asli tanggal 31 Desember 2016. Diakses tanggal 27 Juni 2023.
- ^ Chalmin, Emilie; Menu, Michel; Vignaud, Colette (2003). "Analysis of rock art painting and technology of Palaeolithic painters". Measurement Science and Technology. 14 (9): 1590–1597. doi:10.1088/0957-0233/14/9/310.
- ^ Chalmin, E.; Vignaud, C.; Salomon, H.; Farges, F.; Susini, J.; Menu, M. (2006). "Minerals discovered in paleolithic black pigments by transmission electron microscopy and micro-X-ray absorption near-edge structure" (PDF). Applied Physics A. 83 (12): 213–218. Bibcode:2006ApPhA..83..213C. doi:10.1007/s00339-006-3510-7. hdl:2268/67458.
- ^ Sayre, E. V.; Smith, R. W. (1961). "Compositional Categories of Ancient Glass". Science. 133 (3467): 1824–1826. Bibcode:1961Sci...133.1824S. doi:10.1126/science.133.3467.1824. PMID 17818999.
- ^ a b c Mccray, W. Patrick (1998). "Glassmaking in renaissance Italy: The innovation of venetian cristallo". JOM. 50 (5): 14–19. Bibcode:1998JOM....50e..14M. doi:10.1007/s11837-998-0024-0.
- ^ Rancke-Madsen, E. (1975). "The Discovery of an Element". Centaurus. 19 (4): 299–313. Bibcode:1975Cent...19..299R. doi:10.1111/j.1600-0498.1975.tb00329.x.
- ^ Alessio, L.; Campagna, M.; Lucchini, R. (2007). "From lead to manganese through mercury: mythology, science, and lessons for prevention". American Journal of Industrial Medicine. 50 (11): 779–787. doi:10.1002/ajim.20524. PMID 17918211.
- ^ a b c Couper, John (1837). "On the effects of black oxide of manganese when inhaled into the lungs". Br. Ann. Med. Pharm. Vital. Stat. Gen. Sci. 1: 41–42.
- ^ Olsen, Sverre E.; Tangstad, Merete; Lindstad, Tor (2007). "History of omanganese". Production of Manganese Ferroalloys. Tapir Academic Press. hlm. 11–12. ISBN 978-82-519-2191-6.
- ^ a b Preisler, Eberhard (1980). "Moderne Verfahren der Großchemie: Braunstein". Chemie in unserer Zeit (dalam bahasa Jerman). 14 (5): 137–148. doi:10.1002/ciuz.19800140502.
- ^ Bhattacharyya, P. K.; Dasgupta, Somnath; Fukuoka, M.; Roy Supriya (1984). "Geochemistry of braunite and associated phases in metamorphosed non-calcareous manganese ores of India". Contributions to Mineralogy and Petrology. 87 (1): 65–71. Bibcode:1984CoMP...87...65B. doi:10.1007/BF00371403.
- ^ a b c USGS Mineral Commodity Summaries 2009
- ^ Cook, Nigel J.; Ciobanu, Cristiana L.; Pring, Allan; Skinner, William; Shimizu, Masaaki; Danyushevsky, Leonid; Saini-Eidukat, Bernhardt; Melcher, Frank (2009). "Trace and minor elements in sphalerite: A LA-ICPMS study". Geochimica et Cosmochimica Acta (dalam bahasa Inggris). 73 (16): 4761–4791. Bibcode:2009GeCoA..73.4761C. doi:10.1016/j.gca.2009.05.045.
- ^ Wang, X; Schröder, HC; Wiens, M; Schlossmacher, U; Müller, WEG (2009). "Manganese/polymetallic nodules: micro-structural characterization of exolithobiontic- and endolithobiontic microbial biofilms by scanning electron microscopy". Micron. 40 (3): 350–358. doi:10.1016/j.micron.2008.10.005. PMID 19027306.
- ^ United Nations (1978). Manganese Nodules: Dimensions and Perspectives. Marine Geology. Natural Resources Forum Library. 41. Springer. hlm. 343. Bibcode:1981MGeol..41..343C. doi:10.1016/0025-3227(81)90092-X. ISBN 978-90-277-0500-6. OCLC 4515098.
- ^ "Manganese Mining in South Africa – Overview". MBendi Information Services. Diarsipkan dari versi asli tanggal 5 Februari 2016. Diakses tanggal 27 Juni 2023.
- ^ Elliott, R; Coley, K; Mostaghel, S; Barati, M (2018). "Review of Manganese Processing for Production of TRIP/TWIP Steels, Part 1: Current Practice and Processing Fundamentals". JOM. 70 (5): 680–690. Bibcode:2018JOM....70e.680E. doi:10.1007/s11837-018-2769-4.
- ^ Corathers, L. A.; Machamer, J. F. (2006). "Manganese". Industrial Minerals & Rocks: Commodities, Markets, and Uses (edisi ke-7). SME. hlm. 631–636. ISBN 978-0-87335-233-8.
- ^ a b Zhang, Wensheng; Cheng, Chu Yong (2007). "Manganese metallurgy review. Part I: Leaching of ores/secondary materials and recovery of electrolytic/chemical manganese dioxide". Hydrometallurgy. 89 (3–4): 137–159. doi:10.1016/j.hydromet.2007.08.010.
- ^ Chow, Norman; Nacu, Anca; Warkentin, Doug; Aksenov, Igor; Teh, Hoe (2010). "The Recovery of Manganese from low grade resources: bench scale metallurgical test program completed" (PDF). Kemetco Research Inc. Diarsipkan dari versi asli (PDF) tanggal 2 Februari 2012.
- ^ "The CIA secret on the ocean floor". BBC News (dalam bahasa Inggris). 19 Februari 2018. Diakses tanggal 27 Juni 2023.
- ^ "Project Azorian: The CIA's Declassified History of the Glomar Explorer". National Security Archive at George Washington University. 12 Februari 2010. Diakses tanggal 27 Juni 2023.
- ^ Hein, James R. (Januari 2016). Encyclopedia of Marine Geosciences - Manganese Nodules. Springer. hlm. 408–412. Diakses tanggal 27 Juni 2023.
- ^ Hoseinpour, Vahid; Ghaemi, Nasser (1 Desember 2018). "Green synthesis of manganese nanoparticles: Applications and future perspective–A review". Journal of Photochemistry and Photobiology B: Biology. 189: 234–243. doi:10.1016/j.jphotobiol.2018.10.022. PMID 30412855. Diakses tanggal 27 Juni 2023.
- ^ International Seabed Authority. "Polymetallic Nodules" (PDF). isa.org. International Seabed Authority. Diakses tanggal 27 Juni 2023.
- ^ Oebius, Horst U; Becker, Hermann J; Rolinski, Susanne; Jankowski, Jacek A (Januari 2001). "Parametrization and evaluation of marine environmental impacts produced by deep-sea manganese nodule mining". Deep Sea Research Part II: Topical Studies in Oceanography. 48 (17–18): 3453–3467. Bibcode:2001DSRII..48.3453O. doi:10.1016/s0967-0645(01)00052-2. ISSN 0967-0645.
- ^ Thompson, Kirsten F.; Miller, Kathryn A.; Currie, Duncan; Johnston, Paul; Santillo, David (2018). "Seabed Mining and Approaches to Governance of the Deep Seabed". Frontiers in Marine Science. 5. doi:10.3389/fmars.2018.00480
 .
.
- ^ a b Ray, Durbar; Babu, E. V. S. S. K.; Surya Prakash, L. (1 Januari 2017). "Nature of Suspended Particles in Hydrothermal Plume at 3°40'N Carlsberg Ridge:A Comparison with Deep Oceanic Suspended Matter". Current Science. 112 (1): 139. doi:10.18520/cs/v112/i01/139-146
 . ISSN 0011-3891.
. ISSN 0011-3891.
- ^ a b Hernroth, Bodil; Tassidis, Helena; Baden, Susanne P. (Maret 2020). "Immunosuppression of aquatic organisms exposed to elevated levels of manganese: From global to molecular perspective". Developmental & Comparative Immunology. 104: 103536. doi:10.1016/j.dci.2019.103536. ISSN 0145-305X. PMID 31705914.
- ^ a b Sim, Nari; Orians, Kristin J. (Oktober 2019). "Annual variability of dissolved manganese in Northeast Pacific along Line-P: 2010–2013". Marine Chemistry. 216: 103702. doi:10.1016/j.marchem.2019.103702. ISSN 0304-4203.
- ^ Bartlett, Richmond; Ross, Donald (2005). "Chemistry of Redox Processes in Soils". Dalam Tabatabai, M.A.; Sparks, D.L. Chemical Processes in Soils. SSSA Book Series, no. 8. Madison, Wisconsin: Soil Science Society of America. hlm. 461–487. LCCN 2005924447.
- ^ Dixon, Joe B.; White, G. Norman (2002). "Manganese Oxides". Dalam Dixon, J.B.; Schulze, D.G. Soil Mineralogy with Environmental Applications. SSSA Book Series no. 7. Madison, Wisconsin: Soil Science Society of America. hlm. 367–386. LCCN 2002100258.
- ^ Verhoeven, John D. (2007). Steel metallurgy for the non-metallurgist. Materials Park, Ohio: ASM International. hlm. 56–57. ISBN 978-0-87170-858-8.
- ^ Manganese USGS 2006
- ^ Dastur, Y. N.; Leslie, W. C. (1981). "Mechanism of work hardening in Hadfield manganese steel". Metallurgical Transactions A. 12 (5): 749–759. Bibcode:1981MTA....12..749D. doi:10.1007/BF02648339.
- ^ Stansbie, John Henry (2007). Iron and Steel. Read Books. hlm. 351–352. ISBN 978-1-4086-2616-0.
- ^ Brady, George S.; Clauser, Henry R.; Vaccari. John A. (2002). Materials Handbook: an encyclopedia for managers, technical professionals, purchasing and production managers, technicians, and supervisors. New York, NY: McGraw-Hill. hlm. 585–587. ISBN 978-0-07-136076-0.
- ^ Tweedale, Geoffrey (1985). "Sir Robert Abbott Hadfield F.R.S. (1858–1940), and the Discovery of Manganese Steel Geoffrey Tweedale". Notes and Records of the Royal Society of London. 40 (1): 63–74. doi:10.1098/rsnr.1985.0004
 . JSTOR 531536.
. JSTOR 531536.
- ^ "Chemical properties of 2024 aluminum allow". Metal Suppliers Online, LLC. Diakses tanggal 27 Juni 2023.
- ^ a b Kaufman, John Gilbert (2000). "Applications for Aluminium Alloys and Tempers". Introduction to aluminum alloys and tempers. ASM International. hlm. 93–94. ISBN 978-0-87170-689-8.
- ^ a b Dell, R. M. (2000). "Batteries fifty years of materials development". Solid State Ionics. 134 (1–2): 139–158. doi:10.1016/S0167-2738(00)00722-0.
- ^ "WSK1216" (PDF). vishay. Vishay Intertechnology. Diakses tanggal 27 Juni 2023.
- ^ "EPA Comments on the Gasoline Additive MMT". epa.gov. EPA. Diakses tanggal 27 Juni 2023.
- ^ Shorter Oxford English Dictionary (edisi ke-5). Oxford University Press. 2002. ISBN 978-0-19-860457-0.
Tanah berwarna merah kecokelatan yang mengandung besi dan mangan oksida dan lebih gelap dari oker dan sienna, digunakan untuk membuat berbagai pigmen.
- ^ Chen, Daquin; Zhou, Yang; Zhong, Jiasong (2016). "A review on Mn4+ activators in solids for warm white light-emitting diodes". RSC Advances. 6 (89): 86285–86296. Bibcode:2016RSCAd...686285C. doi:10.1039/C6RA19584A.
- ^ Baur, Florian; Jüstel, Thomas (2016). "Dependence of the optical properties of Mn4+ activated A2Ge4O9 (A=K,Rb) on temperature and chemical environment". Journal of Luminescence. 177: 354–360. Bibcode:2016JLum..177..354B. doi:10.1016/j.jlumin.2016.04.046.
- ^ Jansen, T.; Gorobez, J.; Kirm, M.; Brik, M. G.; Vielhauer, S.; Oja, M.; Khaidukov, N. M.; Makhov, V. N.; Jüstel, T. (1 Januari 2018). "Narrow Band Deep Red Photoluminescence of Y2Mg3Ge3O12:Mn4+,Li+ Inverse Garnet for High Power Phosphor Converted LEDs". ECS Journal of Solid State Science and Technology. 7 (1): R3086–R3092. doi:10.1149/2.0121801jss.
- ^ Jansen, Thomas; Baur, Florian; Jüstel, Thomas (2017). "Red emitting K2NbF7:Mn4+ and K2TaF7:Mn4+ for warm-white LED applications". Journal of Luminescence. 192: 644–652. Bibcode:2017JLum..192..644J. doi:10.1016/j.jlumin.2017.07.061.
- ^ Zhou, Zhi; Zhou, Nan; Xia, Mao; Yokoyama, Meiso; Hintzen, H. T. (Bert) (6 Oktober 2016). "Research progress and application prospects of transition metal Mn4+-activated luminescent materials". Journal of Materials Chemistry C. 4 (39): 9143–9161. doi:10.1039/c6tc02496c.
- ^ "TriGain LED phosphor system using red Mn4+-doped complex fluorides" (PDF). GE Global Research. Diakses tanggal 10 December 2022.
- ^ Kuwahara, Raymond T.; Skinner III, Robert B.; Skinner Jr., Robert B. (2001). "Nickel coinage in the United States". Western Journal of Medicine. 175 (2): 112–114. doi:10.1136/ewjm.175.2.112. PMC 1071501
 . PMID 11483555.
. PMID 11483555.
- ^ "Design of the Sacagawea dollar". United States Mint. Diakses tanggal 27 Juni 2023.
- ^ Shepard, Anna Osler (1956). "Manganese and Iron–Manganese Paints". Ceramics for the Archaeologist. Carnegie Institution of Washington. hlm. 40–42. ISBN 978-0-87279-620-1.
- ^ Rice, Derek B.; Massie, Allyssa A.; Jackson, Timothy A. (2017). "Manganese–Oxygen Intermediates in O–O Bond Activation and Hydrogen-Atom Transfer Reactions". Accounts of Chemical Research. 50 (11): 2706–2717. doi:10.1021/acs.accounts.7b00343. PMID 29064667.
- ^ Takeda, A. (2003). "Manganese action in brain function". Brain Research Reviews. 41 (1): 79–87. doi:10.1016/S0165-0173(02)00234-5. PMID 12505649.
- ^ a b Institute of Medicine (US) Panel on Micronutrients (2001). "Manganese". Dietary Reference Intakes for Vitamin A, Vitamin K, Arsenic, Boron, Chromium, Chromium, Iodine, Iron, Manganese, Molybdenum, Nickel, Silicon, Vanadium, and Chromium. National Academy Press. hlm. 394–419. ISBN 978-0-309-07279-3. PMID 25057538.
- ^ Lihat "Manganese". Micronutrient Information Center. Oregon State University Linus Pauling Institute. 23 April 2014.
- ^ "Overview on Dietary Reference Values for the EU population as derived by the EFSA Panel on Dietetic Products, Nutrition and Allergies" (PDF). 2017.
- ^ Tolerable Upper Intake Levels For Vitamins And Minerals (PDF), European Food Safety Authority, 2006
- ^ "Federal Register May 27, 2016 Food Labeling: Revision of the Nutrition and Supplement Facts Labels. FR page 33982" (PDF).
- ^ "Daily Value Reference of the Dietary Supplement Label Database (DSLD)". Dietary Supplement Label Database (DSLD). Diarsipkan dari versi asli tanggal 7 April 2020. Diakses tanggal 27 Juni 2023.
- ^ Silva Avila, Daiana; Luiz Puntel, Robson; Aschner, Michael (2013). "Chapter 7. Manganese in Health and Disease". Dalam Astrid Sigel; Helmut Sigel; Roland K. O. Sigel. Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences. 13. Springer. hlm. 199–227. doi:10.1007/978-94-007-7500-8_7. ISBN 978-94-007-7499-5. PMC 6589086
 . PMID 24470093.
. PMID 24470093.
- ^ Hernroth, Bodil; Krång, Anna-Sara; Baden, Susanne (February 2015). "Bacteriostatic suppression in Norway lobster (Nephrops norvegicus) exposed to manganese or hypoxia under pressure of ocean acidification". Aquatic Toxicology. 159: 217–224. doi:10.1016/j.aquatox.2014.11.025. ISSN 0166-445X. PMID 25553539.
- ^ Umena, Yasufumi; Kawakami, Keisuke; Shen, Jian-Ren; Kamiya, Nobuo (Mei 2011). "Crystal structure of oxygen-evolving photosystem II at a resolution of 1.9 Å" (PDF). Nature. 473 (7345): 55–60. Bibcode:2011Natur.473...55U. doi:10.1038/nature09913. PMID 21499260.
- ^ Dismukes, G. Charles; Willigen, Rogier T. van (2006). "Manganese: The Oxygen-Evolving Complex & Models". Manganese: The Oxygen-Evolving Complex & Models Based in part on the article Manganese: Oxygen-Evolving Complex & Models by Lars-Erik Andréasson & Tore Vänngård which appeared in the Encyclopedia of Inorganic Chemistry, First Edition, First Edition. Encyclopedia of Inorganic Chemistry. doi:10.1002/0470862106.ia128. ISBN 978-0470860786.
- ^ "Safety Data Sheet". Sigma-Aldrich. Diakses tanggal 28 Juni 2023.
- ^ Hasan, Heather (2008). Manganese. The Rosen Publishing Group. hlm. 31. ISBN 978-1-4042-1408-8.
- ^ "Manganese Chemical Background". Metcalf Institute for Marine and Environmental Reporting University of Rhode Island. April 2006. Diarsipkan dari versi asli tanggal 28 Agustus 2006. Diakses tanggal 28 Juni 2023.
- ^ "Risk Assessment Information System Toxicity Summary for Manganese". Laboratorium Nasional Oak Ridge. Diakses tanggal 28 Juni 2023.
- ^ Ong, K. L.; Tan, T. H.; Cheung, W. L. (1997). "Potassium permanganate poisoning – a rare cause of fatal self poisoning". Emergency Medicine Journal. 14 (1): 43–45. doi:10.1136/emj.14.1.43. PMC 1342846
 . PMID 9023625.
. PMID 9023625.
- ^ Young, R.; Critchley, J. A.; Young, K. K.; Freebairn, R. C.; Reynolds, A. P.; Lolin, Y. I. (1996). "Fatal acute hepatorenal failure following potassium permanganate ingestion". Human & Experimental Toxicology. 15 (3): 259–61. doi:10.1177/096032719601500313. PMID 8839216.
- ^ a b "Safety and Health Topics: Manganese Compounds (as Mn)". U.S. Occupational Safety and Health Administration.
- ^ "NIOSH Pocket Guide to Chemical Hazards – Manganese compounds and fume (as Mn)". Centers for Disease Control. Diakses tanggal 28 Juni 2023.
- ^ Yin, Z.; Jiang, H.; Lee, E. S.; Ni, M.; Erikson, K. M.; Milatovic, D.; Bowman, A. B.; Aschner, M. (2010). "Ferroportin is a manganese-responsive protein that decreases manganese cytotoxicity and accumulation" (PDF). Journal of Neurochemistry. 112 (5): 1190–8. doi:10.1111/j.1471-4159.2009.06534.x. PMC 2819584
 . PMID 20002294.
. PMID 20002294.
- ^ a b Bouchard, M. F; Sauvé, S; Barbeau, B; Legrand, M; Bouffard, T; Limoges, E; Bellinger, D. C; Mergler, D (2011). "Intellectual impairment in school-age children exposed to manganese from drinking water". Environmental Health Perspectives. 119 (1): 138–143. doi:10.1289/ehp.1002321. PMC 3018493
 . PMID 20855239.
. PMID 20855239.
- ^ Barceloux, Donald; Barceloux, Donald (1999). "Manganese". Clinical Toxicology. 37 (2): 293–307. doi:10.1081/CLT-100102427. PMID 10382563.
- ^ Devenyi, A. G; Barron, T. F; Mamourian, A. C (1994). "Dystonia, hyperintense basal ganglia, and high whole blood manganese levels in Alagille's syndrome". Gastroenterology. 106 (4): 1068–71. doi:10.1016/0016-5085(94)90769-2. PMID 8143974.
- ^ Agency for Toxic Substances and Disease Registry (2012) 6. Potential for human exposure, dalam Toxicological Profile for Manganese, Atlanta, GA: U.S. Department of Health and Human Services.
- ^ Pourkhabbaz, A; Pourkhabbaz, H (2012). "Investigation of Toxic Metals in the Tobacco of Different Iranian Cigarette Brands and Related Health Issues". Iranian Journal of Basic Medical Sciences. 15 (1): 636–644. PMC 3586865
 . PMID 23493960.
. PMID 23493960.
- ^ Talhout, Reinskje; Schulz, Thomas; Florek, Ewa; Van Benthem, Jan; Wester, Piet; Opperhuizen, Antoon (2011). "Hazardous Compounds in Tobacco Smoke". International Journal of Environmental Research and Public Health. 8 (12): 613–628. doi:10.3390/ijerph8020613
 . PMC 3084482
. PMC 3084482  . PMID 21556207.
. PMID 21556207.
- ^ Bernhard, David; Rossmann, Andrea; Wick, Georg (2005). "Metals in cigarette smoke". IUBMB Life. 57 (12): 805–9. doi:10.1080/15216540500459667
 . PMID 16393783.
. PMID 16393783.
- ^ Baselt, R. (2008) Disposition of Toxic Drugs and Chemicals in Man, edisi ke-8, Biomedical Publications, Foster City, CA, hlm. 883–886, ISBN 0-9626523-7-7.
- ^ Normandin, Louise; Hazell, A. S. (2002). "Manganese neurotoxicity: an update of pathophysiologic mechanisms". Metabolic Brain Disease. 17 (4): 375–87. doi:10.1023/A:1021970120965. PMID 12602514.
- ^ a b Cersosimo, M. G.; Koller, W.C. (2007). "The diagnosis of manganese-induced parkinsonism". NeuroToxicology. 27 (3): 340–346. doi:10.1016/j.neuro.2005.10.006. PMID 16325915.
- ^ Lu, C. S.; Huang, C.C; Chu, N.S.; Calne, D.B. (1994). "Levodopa failure in chronic manganism". Neurology. 44 (9): 1600–1602. doi:10.1212/WNL.44.9.1600. PMID 7936281.
- ^ a b Guilarte TR, Gonzales KK (August 2015). "Manganese-Induced Parkinsonism Is Not Idiopathic Parkinson's Disease: Environmental and Genetic Evidence". Toxicological Sciences (Review). 146 (2): 204–12. doi:10.1093/toxsci/kfv099. PMC 4607750
 . PMID 26220508.
. PMID 26220508.
- ^ a b Kwakye GF, Paoliello MM, Mukhopadhyay S, Bowman AB, Aschner M (Juli 2015). "Manganese-Induced Parkinsonism and Parkinson's Disease: Shared and Distinguishable Features". Int J Environ Res Public Health (Review). 12 (7): 7519–40. doi:10.3390/ijerph120707519
 . PMC 4515672
. PMC 4515672  . PMID 26154659.
. PMID 26154659.
- ^ Peres TV, Schettinger MR, Chen P, Carvalho F, Avila DS, Bowman AB, Aschner M (November 2016). "Manganese-induced neurotoxicity: a review of its behavioral consequences and neuroprotective strategies". BMC Pharmacology & Toxicology (Review). 17 (1): 57. doi:10.1186/s40360-016-0099-0. PMC 5097420
 . PMID 27814772.
. PMID 27814772.
- ^ Lazrishvili, I.; et al. (2016). "Manganese loading induces mouse-killing behaviour in nonaggressive rats". Journal of Biological Physics and Chemistry. 16 (3): 137–141. doi:10.4024/31LA14L.jbpc.16.03.
- ^ "Drinking Water Contaminants". US EPA. Diakses tanggal 28 Juni 2023.
- ^ Prabhakaran, K.; Ghosh, D.; Chapman, G.D.; Gunasekar, P.G. (2008). "Molecular mechanism of manganese exposure-induced dopaminergic toxicity". Brain Research Bulletin. 76 (4): 361–367. doi:10.1016/j.brainresbull.2008.03.004. ISSN 0361-9230. PMID 18502311.
Pranala luar
[sunting | sunting sumber]- (Inggris) National Pollutant Inventory – Lembar Fakta Mangan dan Senyawanya
- (Inggris) Institut Mangan Internasional
- (Inggris) Halaman Topik Mangan NIOSH
- (Inggris) Mangan di The Periodic Table of Videos (Universitas Nottingham)
- (Inggris) Semua tentang Dendrit Mangan
- (Inggris) Terak Tanur Busur Listrik (EAF)
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


