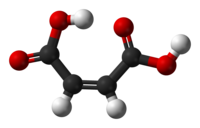
Asam maleat

| |
| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Asam maleat
Asam (Z)-Butenadioat | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C4H4O4 | |
| Massa molar | 116,1 g/mol |
| Penampilan | putih padat |
| Densitas | 1,59 g/cm³, padat |
| Titik lebur | 131-139 °C terurai |
| Titik didih | 135 °C terurai |
| 78 g/100 ml (25 °C) | |
| Keasaman (pKa) | pka1 = 1,83, pka2 = 6,07 |
| Bahaya | |
Klasifikasi UE (DSD) (usang)
|
Berbahaya (Xn) |
| Frasa-R | R22, R36/37/38 |
| Frasa-S | S2, S26, S28, S37 |
| Senyawa terkait | |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Asam maleat atau Asam (Z)-butenadioat atau asam toksilat adalah senyawa organik yang merupakan asam dikarboksilat. Molekul ini terdiri dari gugus etilena yang berikatan dengan dua gugus asam karboksilat. Asam maleat adalah isomer cis dari asam butenadioat, sedangkan asam fumarat merupakan isomer transnya. Isomer cis kurang stabil; perbedaan kalor pembakarannya adalah 22,7 kJ/mol. Sifat-sifat asam maleat sangatlah berbeda dengan asam fumarat. Asam maleat larut dalam air, sedangkan asam fumarat tidak; titik lebur asam maleat adalah (130-139 °C), juga lebih rendah dari titik lebur asam fumara (287 °C). Perbedaan sifat ini dapat dijelaskan oleh ikatan hidrogen intramolekul[1] yang terjadi pada asam maleat.
Asam maleat berbeda dengan asam malat ataupun asam malonat yang keduanya juga merupakan asam dikarboksilat.
Sintesis
Dalam bidang industri, asam maleat diturunkan dari maleat anhidrida dengan hidrolisis. Maleat anhidrida diproduksi dari benzena atau butena melalui proses oksidasi.
Reaksi
- Isomerisasi. Asam maleat dan asam fumarat biasanya tidak akan saling berubah karena rotasi di ikatan ganda karbon tidaklah memfavoritkan pemutaran. Dalam laboratorium, konversi isomer cis menjadi isomer trans dimungkinkan dengan menggunakan cahaya dan bromin dalam jumlah yang kecil.[2] Cahaya mengubah bromin menjadi radikal bromin, yang akan menyerang alkena melalui reaksi adisi radikal menjadi radikal bromo-alkana; memungkinkan terjadi perputaran ikatan tunggal. Radikal bromin berekombinasi dan asam fumarat terbentuk.
- Asam maleat merupakan bahan baku industri untuk produksi asam glioksilat dengan ozonolisis.[3]
- Asam maleat diubah menjadi maleat anhidrida dengan dehidrasi, menjadi asam malat dengan hidrasi, dan menjadi asam suksinat dengan hidrogenasi (etanol / Paladium pada karbon).[4] Ia bereaksi dengan tionil klorida atau fosfor pentaklorida, menghasilkan maleat asil klorida.
- Asam maleat merupakan reaktan pada banyak reaksi Diels-Alder
Maleat
Ion maleat adalah bentuk terionisasi dari asam maleat. Ia merupakan zat yang penting dalam biokimia. Ion maleat berguna dalam biokimia sebagai inhibitor reaksi transaminase. Ester asam maleat juga disebut sebagai maleat, misalnya dimetil maleat.
Referensi
- ^ M. N. G James, G. J. B Williams (1974). "A Refinement of the Crystal Structure of Maleic Acid". Acta Crystallographica. B30 (5): 1249–1275. doi:10.1107/S0567740874004626.
- ^ Light isomerization experiment Diarsipkan 2005-11-27 di Wayback Machine. (from the University of Regensburg, with video)
- ^ "DSM glyoxylic acid production". Diarsipkan dari versi asli tanggal 2005-11-30. Diakses tanggal 2008-10-12.
- ^ Catalytic Hydrogenation of Maleic Acid at Moderate Pressures A Laboratory Demonstration Kwesi Amoa 1948 Journal of Chemical Education • Vol. 84 No. 12 December 2007
Pranala luar
- International Chemical Safety Card 1186
- European Chemicals Bureau Diarsipkan 2011-07-22 di Wayback Machine.
- Titration of Fumaric and Maleic Acid (from the University of Regensburg, about pH, solubility and melting point)
