Timbal(II) nitrat

| |||

| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Lead(II) nitrate
| |||
| Nama lain
Lead nitrate
Plumbous nitrate Lead dinitrate Plumb dulcis | |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChEBI | |||
| ChemSpider | |||
| Nomor EC | |||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| Nomor UN | 1469 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| Pb(NO3)2 | |||
| Massa molar | 331,2g/mol | ||
| Penampilan | Kristal putih tak berwarna | ||
| Densitas | 4,53 g/cm3 (20 °C) | ||
| Titik lebur | 270 °C decomposes | ||
| 37,65 g/100 mL (0 °C) 52 g/100 mL (20 °C) 127 g/100 mL (100 °C) | |||
| Kelarutan dalam asam nitrat dalam etanol dalam metanol |
tak larut 0,04 g/100 mL 1,3 g/100 mL | ||
| Indeks bias (nD) | 1,782[1] | ||
| Struktur | |||
| Kubik pusat muka | |||
| kuboktahedral | |||
| Bahaya | |||
| Lembar data keselamatan | ICSC 1000, MallBaker MSDS | ||
Klasifikasi UE (DSD) (usang)
|
Repr. Cat. 1/3 Beracun (T) Berbahaya (Xn) Berbahaya bagi lingkungan (N) | ||
| Frasa-R | R61, R20/22, R33, R62, R50/53 | ||
| Frasa-S | S53, S45, S60, S61 | ||
| Titik nyala | Tidak terbakar | ||
| Dosis atau konsentrasi letal (LD, LC): | |||
LDLo (terendah tercatat)
|
500 mg/kg (marmot, oral)[2] | ||
| Senyawa terkait | |||
Anion lain
|
Timbal(II) sulfat Timbal(II) klorida Timbal(II) bromida | ||
Kation lainnya
|
Timah(II) nitrat | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Timbal(II) nitrat adalah suatu senyawa anorganik dengan rumus kimia Pb(NO3)2. Senyawa ini umumnya dijumpai sebagai kristal tak berwarna atau serbuk putih dan, tidak seperti kebanyakan garam timbal(II) lainnya, larut dalam air.
Senyawa ini telah dikenal sejak Abad Pertengahan dengan nama plumb dulcis, produksi timbal(II) nitrat baik dari logam timbal maupun timbal oksida dalam asam nitrat merupakan produksi skala kecil, untuk digunakan langsung dalam pembuatan senyawa timbal lainnya. Pada abad ke-19 timbal(II) nitrat mulai diproduksi secara komersial di Eropa dan Amerika Serikat. Menurut catatan sejarah, penggunaan utamanya adalah sebagai bahan baku produksi pigmen untuk cat timbal, tetapi cat sejenis ini sudah digantikan oleh cat yang lebih aman berbahan dasar titanium dioksida. Penggunaan industri lainnya mencakup penstabil panas dalam nilon dan poliester, dan sebagai pelapis kertas fototermografi. Sejak tahun 2000an, timbal(II) nitrat mulai digunakan dalan sianidasi emas.
Timbal(II) nitrat bersifat toksik, suatu oksidator, dan digolongkan sebagai berpotensi karsinogenik pada manusia oleh Badan Internasional Penelitian Kanker (International Agency for Research on Cancer). Akibatnya, timbal(II) nitrat harus ditangani dan disimpan dengan tindakan pencegahan keselamatan yang memadai untuk mencegah terhirup, tertelan, dan terkena kulit. Oleh karena sifat alaminya yang berbahaya, aplikasi terbatas timbal (II) nitrat berada di bawah pengawasan ketat.
Sejarah
[sunting | sunting sumber]Sejak Abad Pertengahan, timbal(II) nitrat telah diproduksi sebagai bahan baku produksi pigmen berwarna dalam cat timbal, seperti krom kuning (timbal(II) kromat), krom jingga (timbal(II) hidroksida kromat) dan senyawa timbal sejenis. Pigmen-pigmen ini digunakan untuk pewarnaan dan pencetakan kaliko dan tekstil lainnya.[3]
Pada tahun 1597, alkimiawan Jerman Andreas Libavius adalah yang pertama menjelaskan senyawa ini, dengan merujuk pada nama abad pertengahan plumb dulcis dan calx plumb dulcis, yang berarti timbal manis, karena rasanya.[4] Meskipun awalnya tidak dipahami selama beberapa abad berikutnya, sifat dekrepitasi timbal(II) nitrat menjadikannya digunakan dalam korek api dan bahan peledak khusus seperti timbal azida.[5]
Proses produksi pernah dan masih mengikuti cara kimia sederhana, melarutkan timbal dalam aqua fortis (asam nitrat), dan secara berkala diambil endapannya. Namun, produksi tetap skala kecil selama berabad-abad, dan produksi komersial timbal(II) nitrat sebagai bahan baku untuk pembuatan senyawa timbal lainnya tidak dilaporkan sampai 1835.[6][7] Pada tahun 1974, A.S. mengkonsumsi senyawa timbal, tidak termasuk pigmen dan aditif bensin, adalah 642 ton.[8]
Struktur
[sunting | sunting sumber]
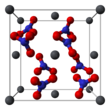
Struktur kristal timbal(II) nitrat padat telah ditentukan menggunakan difraksi neutron.[9][10] Senyawa mengkristal dalam sistem kubik dengan atom timbal dalam sistem kubik pusat muka. Golongan ruangnya adalah Pa3Z=4 (notasi kisi Bravais), yang masing-masing sisi kubus memiliki panjang 784 pikometer.
Noktah hitam menggambarkan atom timbal, noktah putih gugus nitrat 27 pikometer di atas bidang atom timbal. Pada konfigurasi ini, setiap atom timbal [[Ikatan kimia|terikat dengan duabelas atom oksigen (panjang ikatan:281 pikometer). Semua panjang atom N–O juga sama pada 127 pikometer.
Ketertarikan peneliti pada struktur kristal timbal(II) nitrat terutama didasarkan pada kemungkinan rotasi internal bebas gugus nitrat dalam kisi kristal pada kenaikan temperatur, tetapi ini hingga saat ini belum terbukti.[10]
Preparasi dan produksi
[sunting | sunting sumber]Timbal(II) nitrat dapat diperoleh dengan melarutkan logam timbal dalam larutan asam nitrat:[8][11]
Cara yang lebih lazim adalah dengan melarutkan timbal(II) oksida dalam asam nitrat:[8]
Dalam kasus lain, karena pelarutnya adalah asam nitrat pekat (sedangkan timbal(II) nitrat memiliki kelarutan yang sangat rendah) dan larutan yang dihasilkan mengandung ion nitrat, kristal timbal(II) nitrat anhidrat terbentuk secara spontan sebagai hasil dari efek ion sejenis:[11]
Memungkinkan juga untuk mengekstrak nitrat dari bahan organik seperti pupuk atau urin. Ekstraksi nitrat menggunakan metode ini tidak sekuat nitrat berderajat kemurnian industri, tetapi dapat digunakan untuk produksi serbuk mesiu.
Hampir semua timbal(II) nitrat yang tersedia secara komersial diproduksi sesuai dengan bahan skala laboratorium.[12] Dipasok dalam kemasan kantong 25 kg hingga kantong jumbo 1.000&nbps;kg, dan dalam kemasan laboratorium. Hal ini dilakukan baik oleh produsen umum bahan kimia laboratorium maupun produsen timbal dan senyawa timbal. Tidak ada produksi skala besar yang telah dilaporkan.
Dalam perlakuan limbah timbal menggunakan asam nitrat, misalnya, dalam pengolahan limbah timbal-bismut dari pengilangan timbal, larutan tak murni timbal(II) nitrat dibuat sebagai produk sampingan. Larutan ini dilaporkan untuk digunakan dalam proses sianidasi emas.[13]
Reaksi
[sunting | sunting sumber]Selain timbal(II) asetat, timbal(II) nitrat adalah satu-satunya senyawa timbal umum yang dapat larut. Timbal(II) nitrat mudah larut dalam air menghasilkan larutan jernih tak berwarna.[14] Sebagai senyawa ion, pelarutan timbal(II) nitrat melibatkan disosiasi menjadi ion-ion konstituennya.
Timbal(II) nitrat membentuk larutan yang sedikit asam, dengan pH antara 3,0 sampai 4,0 untuk larutan 20% dalam air.[15]
Ketika larutan natrium hidroksida pekat ditambahkan ke dalam larutan timbal(II) nitrat, terbentuk basa nitrat, meskipun sedikit melampaui titik ekivalen. Menuju setengah titik ekivalen, terbentuk senyawa Pb(NO3)2·Pb(OH)2, yang kemudian setelah titik ini akan terbentuk Pb(NO3)2·5Pb(OH)2. Tidak ada pembentukan Pb(OH) sederhana pada pH sekitar 12.[11][16]
Kompleksasi
[sunting | sunting sumber]Timbal(II) nitrat terkait dengan kimia supramolekul yang menakjubkan karena koordinasinya dengan senyawa pendonor elektron nitrogen dan oksigen. Daya tariknya lebih pada aspek akademis, tetapi dengan beberapa aplikasi potensial. Misalnya, penggabungan timbal nitrat dan pentaetilena glikol (EO) dalam larutan asetonitril dan metanol diikuti dengan penguapan lambat menghasilkan bahan kristal baru [Pb(NO3)2(EO5)].[17] Dalam struktur kristal senyawa ini, rantai EO dikelilingi oleh ion timbal dalan suatu bidang ekuatorial yang mirip dengan eter mahkota. Dua ligan nitrat bidentat berada dalam bentuk konfigurasi trans. Bilangan koordinasi total adalah 10, dengan ion timbal dalam struktur geometri molekul antiprisma persegi.
Senyawa kompleks yang dibentuk oleh timbal(II) nitrat, timbal(II) perklorat dan ligan donor N bidentat bitiazola adalah kompleks inti ganda, dengan gugus nitrat menjembatani atom timbal dengan bilangan koordinasi 5 dan 6.[18] Salah satu aspek yang menarik dari kompleks jenis ini adalah adanya celah fisik dalam lingkungan koordinasi; yaitu, ligan tidak berada secara simetris mengelilingi ion logam. Hal ini berpotensi karena pasangan elektron sunyi pada timbal, juga ditemukan dalam kompleks timbal dengan ligan imidazola.[19]
Jenis kimia ini tidak unik hanya untuk garam nitrat; senyawa timbal(II) lainnya seperti timbal(II) bromida juga membentuk kompleks, tetapi senyawa nitratnya sering digunakan karena kelarutannya dan sifat bidentatnya.
Oksidasi dan dekomposisi
[sunting | sunting sumber]Timbal(II) nitrat adalah oksidator. Ini bisa disebabkan karena ion Pb, yang mempunyai potensial reduksi(E°) standar −0,125 V, atau ion nitrat yang pada suasana asam mempunyai E° +0,956 V.[20] Nitrat akan berfungsi pada temperatur tinggi atau dalam suasa asam, sementara timbal(II) berfungsi optimal dalam larutan netral.
Ketika dipanaskan, kristal timbal(II) nitrat terdekomposisi menjadi timbal(II) oksida, oksigen dan nitrogen dioksida.
Oleh karena sifat ini, timbal nitrat sering digunakan dalam piroteknik seperti kembang api.[5]
Aplikasi
[sunting | sunting sumber]Karena sifat timbal(II) nitrat yang berbahaya, ada preferensi untuk menggunakan alternatif dalam aplikasi industri. Sebelumnya, aplikasi utama adalah cat timbal, sekarang sebagian besar telah digantikan dengan titanium dioksida.[21] Aplikasi historis lainnya dari timbal(II) nitrat, seperti dalam korek dan kembang api, telah menurun atau berhenti total. Aplikasi timbal (II) nitrat saat ini mencakup penggunaan sebagai stabilisator panas dalam nilon dan poliester, sebagai pelapis untuk kertas fototermografi, dan rodentisida.[8]
Pada skala laboratorium, timbal(II) nitrat merupakan salah satu dari dua sumber dinitrogen tetroksida yang mudah dan dapat diandalkan. Mengeringkan timbal(II) nitrat dengan hati-hati dan kemudian memanaskannya dalam sebuah bejana baja, dihasilna nitrogen dioksida, yang mengalami dimerisasi menjadi senyawa yang diinginkan.
Untuk memperbaiki proses pelindian (bahasa Inggris: leaching) dalam sianidasi emas, ditambahkan larutan timbal(II) nitrat. Meskipun prosesnya meilbatkan jumlah besar, hanya sedikit timbal(II) nitrat yang diperlukan (10 sampai 100 miligram timbal(II) nitrat per kilogram emas).[22][23] Baik sianidasi itu sendiri, maupun penggunaan senyawa timbal dalam proses, dianggap kontroversial karena sifat toksik kedua senyawa tersebut.
Dalam kimia organik, timbal(II) nitrat telah digunakan sebagai oksidan, misalnya sebagai suatu alternatif dari reaksi Sommelet untuk oksidasi benzil halida menjadi aldehida.[24] Pb(NO''"; juga dijumpai digunakan dalam preparasi isotiosianat dari ditiokarbamat.[25] Karena sifat toksiknya timbal(II) nitrat mulai jarang digunakan, hanya aplikasi-aplikasi terbatas yang masih menggunakannya, seperti peraup (bahasa Inggris: scavenger) bromida selama substitusi SN.[26]
Keselamatan
[sunting | sunting sumber]Timbal(II) nitrat bersifat toksik, dan jika tertelan dapat menyebabkan keracunan timbal akut. Ini berlaku terutama untuk seluruh senyawa timbal yang dapat larut.[27] Seluruh senyawa timbal anorganik diklasifikasikan oleh Badan Internasional Penelitian Kanker (IARC) sebagai berpotensi karsinogen pada manusia (Kategori 2A).[28] Mereka terkait dengan kanker ginjal dan glioma dalam percobaan pada binatang untuk kanker ginjal, kanker otak dan kanker paru-paru dalam manusia, meskipun studi terhadap pekerja yang terpapar timbal sering kali rumit karena bersamaan dengan paparan arsenik.[29] Timbal dikenal sebagai pengganti seng dalam sejumlah enzim, termasuk δ-asam aminolevulinat dehidratase (porfobilinogen sintase) dalam jalur biosintesis heme dan pirimidin-5′-nukleotidase, yang penting bagi metabolisme DNA yang baik dan oleh karenanya menyebabkan kerusakan janin.[30]
Lihat juga
[sunting | sunting sumber]- Pigmen yang mengandung timbal, seperti Timbal putih, Kuning Napoli, dan Timbal merah
- Senyawa bersejarah, seperti Asam muriatat, Vitriol, gula timbal, dan Sal mirabilis
Referensi
[sunting | sunting sumber]- ^ Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. hlm. 475. ISBN 0-07-049439-8.
- ^ "Senyawa timbal (sebagai Pb)". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ^ Partington, James Riddick (1950). A Text-book of Inorganic Chemistry. MacMillan. hlm. 838.
- ^ Libavius, Andreas (1595). Alchemia Andreæ Libavii. Francofurti: Iohannes Saurius.
- ^ a b Barkley, J.B. (October 1978). "Lead nitrate as an oxidizer in blackpowder". Pyrotechnica. Post Falls, Idaho: Pyrotechnica Publications. 4: 16–18.
- ^ "Lead". Encyclopædia Britannica Eleventh Edition. Diakses tanggal 2006-10-11.
- ^ Macgregor, John (1847). Progress of America to year 1846. London: Whittaker & Co. ISBN 0-665-51791-2.
- ^ a b c d Greenwood, Norman N.; Earnshaw, A. (1997). Chemistry of the Elements (edisi ke-2nd). Oxford: Butterworth-Heinemann. hlm. 388, 456. ISBN 0-7506-3365-4.
- ^ Hamilton, W.C. (1957). "A neutron crystallographic study of lead nitrate". Acta Crystallogr. 10 (2): 103–107. doi:10.1107/S0365110X57000304.
- ^ a b Nowotny, H.; G. Heger (1986). "Structure refinement of lead nitrate". Acta Crystallogr. C. 42 (2): 133–35. doi:10.1107/S0108270186097032.
- ^ a b c Othmer, D.F. (1967). Kirk-Othmer Encyclopedia of Chemical Technology. 12 (Iron to Manganese) (edisi ke-second completely revised). New York: John Wiley & Sons. hlm. 272. ISBN 0-471-02040-0.
- ^ Adlam, George Henry Joseph; Price, Leslie Slater (1938). A Higher School Certificate Inorganic Chemistry. London: John Murray.
- ^ "Product catalog; other products". Tilly, Belgium: Sidech. Diarsipkan dari versi asli tanggal 2007-07-01. Diakses tanggal 2008-01-05.
- ^ Ferris, L.M. (1959). "Lead nitrate—Nitric acid—Water system". Journal of Chemicals and Engineering Date. 5 (3): 242–242. doi:10.1021/je60007a002.
- ^ http://www.mallbaker.com/americas/msds/english/L3130_msds_us_Default.pdf[pranala nonaktif permanen]
- ^ Pauley, J. L.; M. K. Testerman (1954). "Basic Salts of Lead Nitrate Formed in Aqueous Media". Journal of the American Chemical Society. 76 (16): 4220–4222. doi:10.1021/ja01645a062.
- ^ Rogers, Robin D.; Andrew H. Bond; Debra M. Roden (1996). "Structural Chemistry of Poly (ethylene glycol). Complexes of Lead(II) Nitrate and Lead(II) Bromide". Inorg. Chem. 35 (24): 6964–6973. doi:10.1021/ic960587b. PMID 11666874.
- ^ Mahjoub, Ali Reza; Ali Morsali (2001). "A Dimeric Mixed-Anions Lead(II) Complex: Synthesis and Structural Characterization of [Pb2(BTZ)4(NO3)(H2O)](ClO4)3 {BTZ = 4,4'-Bithiazole}". Chemistry Letters. 30 (12): 1234. doi:10.1246/cl.2001.1234.
- ^ Shuang-Yi Wan, Jian Fan, Taka-aki Okamura, Hui-Fang Zhu, Xing-Mei Ouyang, Wei-Yin Sun and Norikazu Ueyama (2002). "2D 4.82 Network with threefold parallel interpenetration from nanometre-sized tripodal ligand and lead(II) nitrate". Chem. Commun. (21): 2520–2521. doi:10.1039/b207568g.
- ^ Hill, John W.; Petrucci, Ralph H. (1999). General Chemistry (edisi ke-2nd). Upper Saddle River, New Jersey: Prentice Hall. hlm. 781. ISBN 0-13-010318-7.
- ^ "Historical development of titanium dioxide". Millennium Inorganic Chemicals. Diarsipkan dari versi asli tanggal 2007-10-21. Diakses tanggal 2008-01-04.
- ^ Habashi, Fathi (1998). Recent advances in gold metallurgy. Revisa de la Facultad de Ingeniera, Universidad Central de Venezuela. 13. hlm. 43–54.
- ^ "Auxiliary agents in gold cyanidation". Gold Prospecting and Gold Mining. Diakses tanggal 2008-01-05.
- ^ Schulze, K. E. (1884). "Über α- und β-Methylnaphtalin". Chemische Berichte. 17: 1530. doi:10.1002/cber.188401701384.
- ^ Dains, F. B.; Brewster, R. Q.; Olander, C. P.. "Phenyl isothiocyanate". Org. Synth.; Coll. Vol. 1: 447.
- ^ Rapoport, H.; Jamison, T. (1998). "(S)-N-(9-Phenylfluoren-9-yl)alanine and (S)-Dimethyl-N-(9-phenylfluoren-9-yl)aspartate". Org. Synth.; Coll. Vol. 9: 344.
- ^ "Lead nitrate, Chemical Safety Card 1000". International Labour Organization, International Occupational Safety and Health Information Centre. March 1999. Diakses tanggal 2008-01-19.
- ^ "Inorganic and Organic Lead Compounds" (PDF). IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. International Agency for Research on Cancer. Suppl. 7: 239. 1987. Diakses tanggal 2008-01-19.
- ^ World Health Organization, International Agency for Research on Cancer. (2006). "Inorganic and Organic Lead Compounds" (PDF). IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. International Agency for Research on Cancer. 87. ISBN 92-832-1287-8. Diakses tanggal 2008-01-01.
- ^ Mohammed-Brahim, B.; Buchet, J.P.; Lauwerys, R. (1985). "Erythrocyte pyrimidine 5'-nucleotidase activity in workers exposed to lead, mercury or cadmium". Int Arch Occup Environ Health. 55 (3): 247–52. doi:10.1007/BF00383757. PMID 2987134.
Pranala luar
[sunting | sunting sumber]- Woodbury, William D. (1982). "Lead". Mineral yearbook metals and minerals. Bureau of Mines: 515–42. Diakses tanggal 2008-01-18.
- "Lead". NIOSH Pocket Guide to Chemical Hazards. National Institute for Occupational Safety and Health. September 2005. NIOSH 2005-149. Diakses tanggal 2008-01-19.
- "Lead and Lead Compounds Fact Sheet". National Pollutant Inventory. Australian Government, Department of the Environment and Water Resources. July 2007. Diarsipkan dari versi asli tanggal January 11, 2008. Diakses tanggal 2008-01-19.
- "Lead". A Healthy home environment, Health hazards. US Alliance for healthy homes. Diakses tanggal 2008-01-19.
- "Demonstration movie: Bright Orange Yellow How can you get it". Diakses tanggal 2008-01-19.
- Lembar Data Keselamatan Bahan (MSDS)
- MSDS timbal nitrat, PTCL, Oxford University Diarsipkan 2007-09-16 di Wayback Machine.
- MSDS for lead nitrate, ProSciTechPDF (126 KiB)
- MSDS timbal nitrat, Science Stuff Inc Diarsipkan 2006-03-28 di Wayback Machine.
- MSDS timbal nitrat, Iowa State University Diarsipkan 2006-05-04 di Wayback Machine.
- MSDS timbal nitrat, NIST[pranala nonaktif permanen]
| HNO3 | He | ||||||||||||||||||
| LiNO3 | Be(NO''"; | B(NO''"; | C | N | O | FNO3 | Ne | ||||||||||||
| NaNO3 | Mg(NO''"; | Al(NO''"; | Si | P | S | ClONO2 | Ar | ||||||||||||
| KNO3 | Ca(NO''"; | Sc(NO''"; | Ti(NO''"; | VO(NO''"; | Cr(NO''"; | Mn(NO''"; | Fe(NO''"; | Co(NO''";, Co(NO''"; |
Ni(NO''"; | Cu(NO''"; | Zn(NO''"; | Ga(NO''"; | Ge | As | Se | Br | Kr | ||
| RbNO | Sr(NO''"; | Y | Zr(NO''"; | Nb | Mo | Tc | Ru | Rh | Pd(NO''"; | AgNO | Cd(NO''"; | In | Sn | Sb | Te | I | Xe(NO''"; | ||
| CsNO | Ba(NO''"; | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg, Hg(NO''"; |
Tl(NO''"; | Pb(NO''"; | Bi(NO''"; | Po | At | Rn | |||
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Fl | Uup | Lv | Uus | Uuo | |||
| ↓ | |||||||||||||||||||
| La | Ce(NO''";, Ce(NO''"; |
Pr | Nd | Pm | Sm | Eu | Gd(NO''"; | Tb | Dy | Ho | Er | Tm | Yb | Lu | |||||
| Ac | Th | Pa | UO | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | |||||