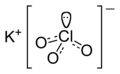
Kalium klorat
| |||

| |||
| Nama | |||
|---|---|---|---|
| Nama lain Kalium klorat(V), Potkrat
| |||
| Penanda | |||
3D model (JSmol)
|
|||
| ChemSpider |
| ||
| ECHA InfoCard | 100.021.173 | ||
| Nomor EC | 223-289-7 | ||
PubChem CID
|
|||
| RTECS number | FO0350000 | ||
| UNII | |||
| Nomor UN | 1485 | ||
| |||
| |||
| Sifat | |||
| KClO3 | |||
| Massa molar | 122.55 g mol−1 | ||
| Penampilan | kristal atau serbuk putih | ||
| Massa jenis | 2.32 g/cm3 | ||
| Titik lebur | 356 °C (673 °F; 629 K) | ||
| Titik didih | 400 °C (752 °F; 673 K) terdekomposisi | ||
| 3.13 g/100 mL (0 °C) 4.46 g/100 mL (10 °C) 8.15 g/100 mL (25 °C) 13.21 g/100 mL (40 °C) 53.51 g/100 mL (100 °C) 183 g/100 g (190 °C) 2930 g/100 g (330 °C)[1] | |||
| Kelarutan | larut dalam gliserol tidak larut dalam aseton dan amonia cair | ||
| Kelarutan dalam gliserol | 1 g/100 g (20 °C) | ||
| −42.8·10−6 cm3/mol | |||
Indeks refraksi (nD)
|
1.40835 | ||
| Struktur | |||
| monoklinik | |||
| Termokimia | |||
Kapasitas kalor (C)
|
100.25 J/mol·K | ||
Entropi molar std (S
|
142.97 J/mol·K | ||
Entalpi pembentukan standar (ΔfH
|
−391.2 kJ/mol[2][3] | ||
Energi bebas Gibbs (ΔfG˚)
|
-289.9 kJ/mol | ||
| Hazards | |||
| Lembar data keselamatan | ICSC 0548 | ||
| Piktogram GHS |    [4] [4]
| ||
| Teks GHS | Berbahaya | ||
| H271, H302, H332, H411 | |||
| P220, P273 | |||
| NFPA 704 | 
0
2
3 OX | ||
| Dosis atau konsentrasi letal (LD, LC): | |||
LD50 (median dose)
|
1870 mg/kg (oral, rat)[5] | ||
| Senyawa terkait | |||
Anion lain
|
Kalium bromat Kalium iodat Kalium nitrat | ||
Kation lain
|
Amonium klorat Natrium klorat Barium klorat | ||
Senyawa terkait
|
Kalium klorida Kalium hipoklorit Kalium klorit Kalium perklorat | ||
Kecuali dinyatakan lain, data di atas berlaku pada temperatur dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Infobox references | |||
Kalium klorat adalah senyawa yang mengandung kalium, klorin dan oksigen, dengan rumus molekul KClO3. Dalam bentuk murni, ia berupa kristal putih. Ini adalah klorat yang paling umum digunakan dalam industri. Garam ini digunakan
- sebagai oksidator,
- untuk menghasilkan oksigen,
- sebagai disinfektan,
- pengaman korek api,
- bahan peledak dan kembang api,
- dalam budidaya, memaksa pemekaran pohon lengkeng, menyebabkan ia menghasilkan buah di iklim yang lebih hangat.[6]
Produksi
[sunting | sunting sumber]Pada skala industri, kalium klorat dibuat melalui proses Liebig: klorin dilewatkan ke kalsium hidroksida panas, kemudian ditambahkan kalium klorida:[7]
- 6 Ca(OH)2 + 6 Cl2 → Ca(ClO3)2 + 5 CaCl2 + 6 H2O
- Ca(ClO3)2 + 2 KCl → 2 KClO3 + CaCl2
Kadang-kadang juga digunakan elektrolisis KCl dalam larutan berair, di mana unsur klorin yang terbentuk di anoda bereaksi dengan KOH secara in situ. Rendahnya kelarutan KClO3 dalam air mengakibatkan garam dengan mudahnya mengisolasi dirinya sendiri dari campuran reaksi dengan membentuk endapan.
Kalium klorat dapat diproduksi dalam jumlah kecil melalui disproporsionasi dalam larutan natrium hipoklorit diikuti oleh reaksi metatesis menggunakan kalium klorida:[8]
- 3 NaOCl(aq) → 2 NaCl(s) + NaClO3(aq)
- KCl(aq) + NaClO3(aq) → NaCl(aq) + KClO3(s)
Kalium klorat juga dapat dibuat dengan melewatkan gas klorin ke dalam larutan kalium hidroksida panas:[9]
- 3 Cl2(g) + 6 KOH(aq) → KClO3(aq) + 5 KCl(aq) + 3 H2O(l)
Penggunaan
[sunting | sunting sumber]
Kalium klorat adalah salah satu bahan utama pada awal senjata api topi perkusi (primer). Aplikasi ini berlanjut pada aplikasi yang tidak tergantikan oleh kalium perklorat.
Propelan berbasis klorat lebih efisien daripada mesiu tradisional dan lebih tahan terhadap air. Namun, mereka dapat menjadi sangat tidak stabil dengan adanya sulfur atau fosforus dan jauh lebih mahal. Propelan klorat harus digunakan hanya pada peralatan yang dirancang khusus; kegagalan mematuhi tindakan pencegahan ini adalah sumber umum kecelakaan. Kalium klorat, sering dalam kombinasi dengan perak fulminat, digunakan dalam trik kembang api jenis baru yang populer.
Aplikasi lain dari kalium klorat adalah sebagai oksidator dalam komposisi asap seperti yang digunakan dalam granat asap. Sejak tahun 2005, kartrij dengan kalium klorat dicampur dengan laktosa dan damar digunakan untuk menghasilkan asap putih yang menandakan terpilihnya paus baru oleh sebuah konklaf kepausan.[10]
Kalium klorat sering digunakan di laboratorium sekolah dan perguruan tinggi untuk menghasilkan gas oksigen. [butuh rujukan] Ini merupakan sumber yang jauh lebih murah daripada tangki oksigen bertekanan atau kriogenik. Kalium klorat mudah terdekomposisi jika dipanaskan dengan adanya katalis, biasanya mangan(IV) dioksida (MnO2). Dengan demikian, untuk menghasilkan oksigen cukup hanya ditempatkan dalam tabung reaksi dan dipanaskan di atas pembakar. Jika tabung reaksi ini dilengkapi dengan sumbat berlubang satu dan selang, oksigen hangat dapat dipisahkan. Reaksinya adalah sebagai berikut:
- 2 KClO3(s) → 3 O2(g) + 2 KCl(s)
Pemanasan tanpa adanya katalis mengubahnya menjadi kalium perklorat:
- 4 KClO3 → 3 KClO4 + KCl
Dengan pemanasan lebih lanjut, kalium perklorat terdekomposisi menjadi kalium klorida dan oksigen:
- KClO4 → KCl + 2 O2
Agar reaksi ini berlangsung aman, diperlukan pereaksi berkemurnian tinggi dan temperatur perlu dikendalikan dengan hati-hati. Leburan kalium klorat merupakan oksidator yang sangat kuat dan bereaksi spontan dengan banyak bahan seperti gula. Ledakan dapat terjadi dari cairan klorat yang dipercikkan pada selang lateks atau pipa PVC generator oksigen, akibat kontak antara klorat dengan hidrokarbon dari gemuk penyegel. Ketakmurnian dalam kalium klorat itu sendiri dapat menimbulkan masalah. Ketika bekerja dengan tumpak baru kalium klorat, disarankan mengambil sejumlah kecil sampel (~1 gram) dan memanaskannya dengan kuat di atas piring kaca terbuka. Munculnya letupan-letupan pada sedikit sampel tersebut menunjukkan bahwa klorat harus dibuang.
Kalium klorat digunakan dalam generator oksigen kimia (disebut juga lilin klorat atau lilin oksigen), yang digunakan sebagai sistem pemasok oksigen pada misalnya, pesawat terbang, stasiun ruang angkasa, kapal selam, dan dianggap bertanggung jawab untuk setidaknya satu kecelakaan pesawat. Penelusuran kebakaran di stasiun ruang angkasa Mir juga mengarah kepada zat ini. Dekomposisi kalium klorat juga digunakan untuk memberikan pasokan oksigen untuk lampu kalsium (bahasa Inggris: limelights).
Kalium klorat digunakan juga sebagai pestisida. Di Finlandia ia dijual dengan nama dagang Fegabit.
Kalium klorat dapat bereaksi dengan asam sulfat menghasilkan larutan asam klorat yang sangat reaktif dan kalium sulfat:
- 2 KClO3 + H2SO4 → 2 HClO3 + K2SO4
Larutan hasil reaksi cukup reaktif yang dapat menyala spontan jika terdapat bahan yang mudah terbakar (gula, kertas, dll.)
Di sekolah-sekolah, kalium klorat cair digunakan dalam demonstrasi kimia dramatis teriakan bayi jeli (screaming jelly babies).
Di laboratorium kimia, senyawa ini digunakan untuk mengoksidasi HCl dan membebaskan sejumlah kecil gas klorin.
Pemberontak di Afghanistan juga menggunakan kalium klorat secara luas sebagai komponen utama dalam produksi alat peledak improvisasi (IED). Ketika telah dilakukan upaya signifikan untuk mengurangi ketersediaan pupuk amonium nitrat di Afghanistan, pembuat IED mulai menggunakan kalium klorat sebagai alternatif yang murah dan efektif. Pada tahun 2013, 60% IED di Afghanistan menggunakan kalium klorat, menjadikannya bahan yang paling jamak digunakan dalam IED.[11] Kalium klorat juga merupakan bahan utama dalam bom mobil yang digunakan dalam bom Bali 2002 yang menewaskan 202 orang.
Keselamatan
[sunting | sunting sumber]Kalium klorat harus ditangani dengan hati-hati. Ia bereaksi hebat, dan dalam beberapa kasus dapat menyala atau meledak spontan, bila dicampur dengan bahan-bahan yang mudah terbakar. Ia membakar dengan hebat jika bercampur dengan hampir setiap bahan yang mudah terbakar, meskipun bahan tersebut normalnya hanya sedikit (agak) mudah terbakar (termasuk debu dan serat biasa). Campuran kalium klorat dan bahan bakar dapat terbakar jika terkena asam sulfat, sehingga harus dijauhkan dari pereaksi ini. Belerang harus dihindarkan dalam komposisi piroteknik yang mengandung kalium klorat, karena campuran ini cenderung mengalami deflagrasi spontan. Sebagian besar sulfur mengandung sekelumit asam bersulfur, yang dapat menyebabkan pengapian spontan - "Bunga belerang" atau "belerang tersublimasi", meskipun secara keseluruhan berkemurnian yang tinggi. Selain itu, campuran kalium klorat dengan setiap senyawa dengan sifat yang dapat menimbulkan pengapian (misalnya. antimon(III) sulfida) yang preparasinya sangat berbahaya, karena sifatnya yang peka guncangan.
Lihat juga
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ Seidell, Atherton; Linke, William F. (1952). Google Books Solubilities of Inorganic and Organic Compounds] Check
|url=value (help). Van Nostrand. Retrieved 2014-05-29. - ^ Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A22. ISBN 0-618-94690-X.
- ^ "potassium chlorate". Retrieved 9 July 2015.
- ^ "Potassium chlorate" Diarsipkan 2012-09-22 di Wayback Machine.. Retrieved 9 July 2015.
- ^ Michael Chambers. "ChemIDplus - 3811-04-9 - VKJKEPKFPUWCAS-UHFFFAOYSA-M - Potassium chlorate - Similar structures search, synonyms, formulas, resource links, and other chemical information". Retrieved 9 July 2015.
- ^ Manochai, P.; Sruamsiri, P.; Wiriya-alongkorn, W.; Naphrom, D.; Hegele, M.; Bangerth, F. (February 12, 2005). "Year around off season flower induction in longan (Dimocarpus longan, Lour.) trees by KClO3 applications: potentials and problems". Scientia Horticulturae. Department of Horticulture, Maejo University, Chiang Mai, Thailand; Department of Horticulture, Chiang Mai University, Chiang Mai, Thailand; Institute of Special Crops and Crop Physiology, University of Hohenheim, 70593 Stuttgart, Germany. 104 (4): 379–390. doi:10.1016/j.scienta.2005.01.004. Diakses tanggal November 28, 2010.
- ^ Реми, Г. Курс неорганической химиию, т. 1/Перевод с немецкого под ред. А. В. Новосёловой. Москва:Мир, 1972.- с. 770//(translated from:) Heinrich Remy. Lehrbuch der anorganischen Chemie. XI Auflage. Band 1. Leipzig:Geest & Portig K.-G., 1960.
- ^ Anne Marie Helmenstine, Ph.D. "Potassium Chlorate Synthesis (Substitute) Formula". About.com Education. Diarsipkan dari versi asli tanggal 2017-02-17. Diakses tanggal 9 July 2015.
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ Daniel J. Wakin and Alan Cowell (March 13, 2013). "New Round of Voting Fails to Name a Pope". The New York Times. Diakses tanggal March 13, 2013.
- ^ "Afghan bomb makers shifting to new explosives for IEDs". USAToday.com. June 25, 2013. Diakses tanggal 2013-06-25.
- "Klorat de kalium. Klorat de sodium", Fiche toxicol. n° 217, Paris:Institut national de recherche et de sécurité, 2000. 4pp.
- Continuous process for the manufacture of potassium chlorate by coupling with a sodium chlorate production plant