Melioidosis
Halaman ini sedang dipersiapkan dan dikembangkan sehingga mungkin terjadi perubahan besar. Anda dapat membantu dalam penyuntingan halaman ini. Halaman ini terakhir disunting oleh Hanamanteo (Kontrib • Log) 906 hari 693 menit lalu. Jika Anda melihat halaman ini tidak disunting dalam beberapa hari, mohon hapus templat ini. |
| Melioidosis | |
|---|---|
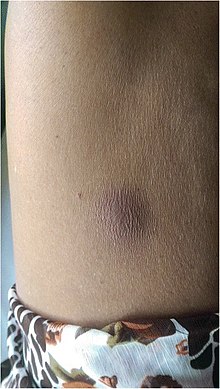 | |
| Bisul melioidosis di perut | |
| Informasi umum | |
| Spesialisasi | Penyakit menular |
| Penyebab | Burkholderia pseudomallei spread by contact to soil or water[1] |
| Faktor risiko | Diabetes mellitus, thalassaemia, alcoholism, chronic kidney disease[1] |
| Aspek klinis | |
| Gejala dan tanda | Tiada, demam, radang paru-paru, beberapa bisul[1] |
| Komplikasi | Encephalomyelitis, septic shock, acute pyelonephritis, septic arthritis, osteomyelitis[1] |
| Awal muncul | 1-21 hari setelah terjangkit[1] |
| Diagnosis | Mengembangkan bakteri di perantara kultur[1] |
| Kondisi serupa | Tuberculosis[2] |
| Tata laksana | |
| Pencegahan | Mencegah dari kontak dengan air yang terkontaminasi, profilaksis antibiotik[1] |
| Perawatan | Ceftazidime, meropenem, co-trimoxazole[1] |
| Distribusi dan frekuensi | |
| Prevalensi | 165,000 orang tiap tahun[1] |
| Kematian | 89,000 orang tiap tahunr[1] |
Melioidosis adalah penyakit infeksi yang disebabkan oleh bakteri Gram-negatif bernama Burkholderia pseudomallei.[1] Kebanyakan orang yang dijangkiti Burkholderia pseudomallei tidak mengalami satupun gejala, tetapi mereka yang mengalami gejala memiliki tanda dan gejala dari gejala ringan seperti demam, perubahan kulit, radang paru-paru, dan bisul, hingga gejala berat seperti radang otak, radang sendi, dan tekanan darah rendah yang berbahaya yang menyebabkan kematian.[1] Sekitar 10% dari orang penderita melioidosis mengalami gejala yang berlangsung lebih dari dua bulan yang disebut melioidosis kronis.[1]
Manusia dijangkiti Burkholderia pseudomallei melalui kontak dengan air yang tercemar. Bakteri ini masuk ke dalam tubuh melalui luka, tarikan napas, atau penelanan. Penularan dari manusia ke manusia atau dari hewan ke manusia sangat jarang terjadi.[1] Infeksi ini masih ada di Asia Tenggara, khususnya di timur laut Thailand dan utara Australia.[1] Di negara-negara maju seperti Eropa dan Amerika Serikat, kasus melioidosis umumnya diimpor dari negara-negara tempat melioidosis lebih sering terjadi.[3] Tanda dan gejala melioidosis menyerupai tuberkulosis dan sering terjadi kesalahan diagnosis.[4][2] Diagnosis biasanya dikonfirmasi oleh pertumbuhan Burkholderia pseudomallei dari darah atau cairan tubuh orang yang dijangkiti lainnya.[1] Mereka yang menderita melioidosis pertama-tama diobati dengan antibiotik intravena "fase intensif" (paling sering seftazidima) diikuti dengan pengobatan kotrimoksazol selama beberapa bulan.[1] Bahkan jika dirawat dengan cermat, sekitar 10% penderita melioidosis meninggal karenanya. Jika tidak ditangani dengan cermat, tingkat kematian bisa melonjak hingga 40%.[1]
Upaya pencegahan melioidosis antara lain memakai alat pelindung diri saat menangani air yang terkontaminasi, membiasakan kebersihan tangan, minum air matang, dan menghindari kontak langsung dengan tanah, air, atau hujan lebat. Antibiotik kotrimoksazol hanya digunakan sebagai pencegahan untuk individu yang berisiko tinggi terkena melioidosis setelah terpapar bakteri. Tiada vaksin untuk melioidosis yang telah disetujui.[1]
Sekitar 165 ribu orang dijangkiti melioidosis tiap tahun dan menewaskan 89 ribu orang. Diabetes adalah faktor risiko utama penyakit melioidosis dengan lebih dari setengah kasus melioidosis terjadi pada penderita diabetes.[1] Peningkatan curah hujan dikaitkan dengan lonjakan jumlah kasus melioidosis di daerah endemi.[2] Melioidosis pertama kali dideskripsikan oleh Alfred Whitmore pada tahun 1912 di wilayah yang saat ini bernama Myanmar.[5]
Tanda dan gejala
Akut




Pajanan terhadap Burkholderia pseudomallei biasanya dapat menyebabkan antibodi diproduksi untuk melawan bakteri itu tanpa gejala apapun. Dari pasien yang menderita infeksi klinis, 85% pasien mengalami gejala akut dari pemerolehan bakteri terkini.[1][6][7] Masa inkubasi rata-rata melioidosis akut adalah 9 hari (kisaran 1–21 hari).[1] Walau begitu, gejala melioidosis dapat muncul dalam 24 jam bagi mereka yang dijangkiti saat hampir tenggelam di air yang terkontaminasi.[7] Mereka yang terkena melioidosis akan memunculkan gejala sepsis (terutama demam) dengan atau tanpa radang paru-paru, atau bisul atau fokus infeksi lainnya. Adanya tanda dan gejala yang tidak spesifik yang menyebabkan melioidosis dijuluki "peniru ulung".[1]
Orang yang menderita diabetes melitus atau pajanan bakteri secara teratur berada pada peningkatan risiko menderita melioidosis. Penyakit ini harus dipertimbangkan pada mereka yang tinggal di daerah endemi yang mengalami demam, radang paru-paru, atau bisul di hati, limpa, prostat, atau kelenjar parotid mereka. Manifestasi klinis penyakit ini dapat membentang dari perubahan kulit yang sederhana hingga masalah organ yang parah.[1] Perubahan kulit dapat berupa bisul atau tukak nonspesifik.[8] Di utara Australia, 60% dari anak-anak yang terjangkit hanya menunjukkan lesi kilit, sedangkan 20% dari anak-anak yang terjangkit menunjukkan radang paru-paru.[3] Organ yang paling sering terkena melioidosis adalah hati, limpa, paru-paru, prostat, dan ginjal. Di antara tanda-tanda klinis yang paling umum adalah adanya bakteri dalam darah (dalam 40% sampai 60% kasus), radang paru-paru (50%), dan syok septik (20%).[1] Orang yang hanya mengalami radang paru-paru pneumonia mungkin mengalami batuk yang menonjol dengan dahak dan sesak napas. Namun, mereka yang mengalami syok septik bersama dengan radang paru-paru mungkin mengalami batuk yang minimal.[2] Hasil sinar-X dada dapat membentang dari infiltrat nodular difus pada mereka yang mengalami syok septik hingga pemadatan paru-paru progresif di lobus atas pada mereka yang hanya mengalami radang paru-paru. Kelebihan cairan di rongga pleura dan pengumpulan nanah di dalam rongga lebih sering terjadi pada melioidosis yang memengaruhi lobus bawah paru-paru.[2] Dalam 10% kasus, orang menderita radang paru-paru sekunder yang disebabkan oleh bakteri lain setelah infeksi primer.[3]
Manifestasi parah lainnya terjadi bergantung pada perjalanan infeksi. Sekitar 1% hingga 5% dari mereka yang terjangkit mengalami radang otak dan penutup otak atau kumpulan nanah di otak, 14% hingga 28% mengalami peradangan bakteri pada ginjal, bisul ginjal atau bisul prostat, 0% sampai 30% mengalami bisul leher atau kelenjar ludah, 10% hingga 33% mengalami bisul hati, limpa, atau paraintestinal, dan 4% sampai 14% mengalami artritis septik dan osteomielitis.[1] Manifestasi yang langka di antaranya penyakit kelenjar getah bening yang menyerupai tuberkulosis,[9] massa mediastinum, pengumpulan cairan di penutup jantung,[3] dilatasi abnormal pembuluh darah karena infeksi,[1] dan radang pankreas.[3] Di Australia, hingga 20% dari pria yang terjangkit mengalami bisul prostat yang ditandai dengan nyeri saat buang air kecil, kesulitan buang air kecil, dan retensi urin yang memerlukan kateterisasi.[1] Pemeriksaan rektum menunjukkan peradangan prostat.[3] Di Thailand, 30% dari anak-anak yang terjangkit mengalami bisul parotid.[1] Ensefalomielitis dapat terjadi pada orang sehat tanpa faktor risiko. Mereka yang menderita ensefalomielitis melioidosis cenderung memiliki pindaian tomografi terkomputasi normal, tetapi sinyal T2 oleh pencitraan resonansi magnetik sehingga meluas ke batak otak dan sumsum tulang belakang. Tanda-tanda klinis yaitu kelemahan anggota gerak neuron motorik atas unilateral, tanda-tanda serebelar, dan kelumpuhan saraf kranial (kelumpuhan saraf VI, VII, dan kelumpuhan bulbar). Beberapa kasus hanya mengalami kelumpuhan kulai.[3] Di utara Australia, semua kasus melioidosis beserta ensefalomielitis mengalami peningkatan sel darah putih dalam cairan serebrospinal (CSF), sebagian besar sel mononuklir dengan protein CSF yang meningkat.[9]
Kronis
Melioidosis kronis biasanya ditandai dengan gejala yang berlangsung lebih dari dua bulan dan terjadi pada sekitar 10% pesakit.[1] Penyajian klinis yaitu demam, penurunan berat badan, dan batuk berkelanjutan dengan atau tanpa dahak berdarah, yang mungkin menyerupai tuberkulosis. Selain itu, bisul di beberapa bagian tumbuh yang berlangsung lama juga dapat timbul.[2] Tuberkulosis harus diwaspadai jika kelenjar getah bening membesar di akar paru-paru. Melioidosis kronis dapat muncul dengan kavitasi radang paru-paru menyerupai tuberkulosis paru kronis.[10] Tidak seperti tuberkulosis, radang paru-paru yang disebabkan oleh melioidosis jarang menyebabkan jaringan parut dan pengapuran paru-paru, tidak seperti tuberkulosis.[9]
Laten
Dalam infeksi laten, orang yang imunokompeten dapat menghilangkan infeksi tanpa menunjukkan gejala apa pun, tetapi kurang dari 5% dari semua kasus melioidosis memiliki aktivasi setelah periode laten.[1] Pesakit melioidosis laten dapat saja bebas gejala selama beberapa dasawarsa.[11] Awalnya, periode terlama antara dugaan paparan dan presentasi klinis diperkirakan selama 62 tahun di tahanan perang Perang Dunia II di Burma-Thailand-Malaysia.[11] Genotipe isolat bakteri selanjutnya dari veteran Perang Vietnam menunjukkan bahwa isolat tersebut mungkin tidak berasal dari Asia Tenggara, melainkan Amerika Selatan.[12] Laporan ini membalikkan laporan lain yang menempatkan periode laten terpanjang untuk melioidosis yaitu 29 tahun.[13] Potensi inkubasi yang berkepanjangan diakui oleh prajurit Amerika Serikat yang terlibat dalam Perang Vietnam, sehingga melioidosis disebut sebagai "bom waktu Vietnam".[2][14] Di Australia, periode laten terpanjang yang tercatat adalah 24 tahun.[3] Berbagai komorbiditas seperti diabetes, gagal ginjal, dan alkoholisme dapat menjadi predisposisi reaktivasi melioidosis.[2]
Penyebab
Bakteri
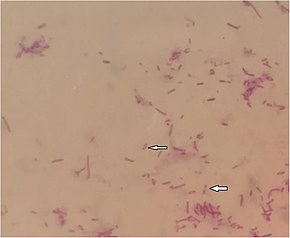
Melioidosis disebabkan oleh bakteri Gram-negatif, motil, saprofit bernama Burkholderia pseudomallei. Bakteri ini juga dapat menjadi patogen intraseluler fakultatif oportunistik.[1] Bakteri ini juga aerobik dan positif berdasarkan uji oksidase. Sebuah vakuola di tengah bakteri membuatnya menyerupai “peniti” saat diwarnai dengan Gram.[2] Bakteri ini mengeluarkan bau tanah yang kuat setelah 24 hingga 48 jam pertumbuhan dalam kultur. Burkholderia pseudomallei menghasilkan kapsul polisakarida glikokaliks yang membuatnya resisten terhadap banyak jenis antibiotik.[15] Bakteri ini umumnya resisten terhadap gentamisin dan kolistin, tetapi peka terhadap asam klavulanat (co-amoxiclav). Burkholderia pseudomallei adalah patogen level keselamatan biologi 3, yang memerlukan penanganan laboratorium khusus.[2] Pada hewan, makhluk hidup serupa lainnya bernama Burkholderia mallei adalah agen penyebab penyakit glanders.[1] Burkholderia pseudomallei dapat dibedakan dari Burkholderia thailandensis yang berkerabat dekat tetapi kurang patogen lewat kemampuannya mengasimilasi arabinose.[9] Burkholderia pseudomallei sangat mudah beradaptasi dengan berbagai lingkungan inang mulai dari spora jamur mikoriza hingga ameba.[2] Kemampuan beradaptasinya dapat memberikan keuntungan bertahan hidup dalam tubuh manusia.[1]
Genom Burkholderia pseudomallei terdiri dari dua replikon, yaitu kromosom 1 mengodekan fungsi urus rumah bakteri seperti sintesis, mobilitas, dan metabolisme dinding sel serta kromosom 2 mengodekan fungsi yang memungkinkan bakteri beradaptasi dengan berbagai lingkungan. Transfer gen horizontal di antara bakteri telah menghasilkan genom yang sangat bervariasi pada Burkholderia pseudomallei. Australia diperkirakan sebagai reservoir awal bagi Burkholderia pseudomallei karena variabilitas genetik yang tinggi dari bakteri yang ditemukan di wilayah ini. Bakteri yang diisolasi dari Afrika serta Amerika Tengah dan Selatan tampaknya memiliki nenek moyang sama yang hidup pada abad ke-17 hingga ke-19.[1] Burkholderia mallei adalah klon dari Burkholderia pseudomallei yang telah kehilangan sebagian besar genomnya karena beradaptasi untuk hidup secara eksklusif pada mamalia.[3]
Penularan
Burkholderia pseudomallei biasanya ditemukan di tanah dan air permukaan serta paling banyak ditemukan di kedalaman tanah 10 cm hingga 90 cm.[1] Bakteri ini juga ditemukan di tanah, kolam, sungai, lubuk, genangan air, dan sawah.[2] Bakteri ini dapat bertahan hidup dalam lingkungan yang miskin nutrisi seperti air suling, tanah gurun, dan tanah yang kekurangan nutrisi selama lebih dari 16 tahun. Bakteri ini juga dapat bertahan dalam larutan antiseptik dan deterjen, lingkungan asam (pH 4,5 selama 70 hari), dan lingkungan pada suhu berkisar antara 24°C hingga 32°C. Bakteri ini tidak bertahan hidup dengan adanya sinar ultraviolet.[1]
Bakteri dapat memasuki tubuh lewat luka, hirupan, dan menelan air yang tercemar.[1] Penularan dari orang ke orang sangat jarang terjadi.[2] Melioidosis adalah penyakit yang diakui terhadap hewan semisal kucing, anjing, kambing, domba, dan kuda. Sapi, kerbau, dan buaya dianggap relatif resisten terhadap melioidosis meskipun terus-menerus terpapar air dan tanah yang mengandung bakteri ini. Burung juga resisten terhadap melioidosis.[9][15] Penularan dari hewan ke manusia jarang terjadi.[1][2]
Klorinasi pasokan air yang tidak memadai dikaitkan dengan wabah Burkholderia pseudomallei di Australia Utara dan Barat. Bakteri ini juga ditemukan dalam pasokan air yang tidak diklorinasi di pedesaan Thailand. Cairan pengairan yang terkontaminasi dengan Burkholderia pseudomallei dikaitkan dengan infeksi luka nosokomial di rumah sakit.[1] Berdasarkan pengurutan keseluruhan genom bakteri ini, manusia mungkin berperan dalam memindahkan Burkholderia pseudomallei dari satu tempat ke tempat lain.[16]
Patogenesis
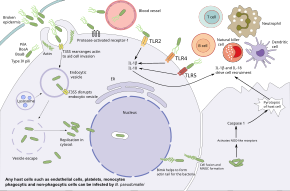
Burkholderia pseudomallei memiliki kemampuan untuk menjangkiti pelbagai jenis sel dan menghindari respons imun manusia. Bakteri pertama-tama masuk ke dalam celah di kulit atau selaput lendir dan bereplikasi di sel epitel. Dari sana, bakteri ini menggunakan motilitas flagela untuk menyebar dan menjangkiti pelbagai jenis sel. Dalam aliran darah, bakteri ini dapat menjangkiti baik fagosit dan nonfagosit. Burkholderia pseudomallei menggunakan flagela untuk bergerak mendekati sel inang, kemudian menempel pada sel menggunakan pelbagai protein adhesi termasuk protein pilus tipe IV PilA dan protein adhesi BoaA dan BoaB. Selain itu, adhesi bakteri sebagian tergantung pada keberadaan reseptor-1 yang diaktifkan protease protein inang yang ada pada permukaan sel endotel, keping darah, dan monosit. Setelah terikat, bakteri ini memasuki sel inang melalui endositosis dan berakhir di dalam vesikel endositik. Saat vesikel menjadi asam, Burkholderia pseudomallei menggunakan sistem sekresi tipe 3 (T3SS) untuk menyuntikkan protein efektor ke dalam sel inang, sehingga mengganggu vesikel dan membiarkan bakteri keluar ke sitoplasma inang. Dalam sitoplasma inang, bakteri menghindari dari dibunuh oleh autofagi inang menggunakan pelbagai protein efektor T3SS. Bakteri ini bereplikasi di sitoplasma inang.[1][9]
Di dalam sel inang, Burkholderia pseudomallei bergerak dengan menginduksi polimerisasi aktin inang di belakangnya, sehingga mendorong bakteri ini ke depan.[1] Motilitas yang dimediasi aktin ini dicapai dengan autotransporter BimA yang berinteraksi dengan aktin di ujung ekor bakteri. Didorong oleh aktin, bakteri ini mendorong membran inang, sehingga menciptakan tonjolan yang meluas ke sel tetangga. Tonjolan ini menyebabkan sel-sel tetangga menyatu yang mengarah kepada pembentukan sel raksasa berinti banyak (MNGC). Ketika MNGC lisis, sel-sel tetangga membentuk plak (daerah bening pusat dengan cincin sel yang menyatu) yang menyediakan perlindungan bagi bakteri untuk replikasi lebih lanjut atau infeksi laten. Proses yang sama pada neuron yang terjangkit ini dapat memungkinkan bakteri melakukan perjalanan melalui akar saraf di sumsum tulang belakang dan otak yang menyebabkan peradangan otak dan sumsum tulang belakang. Selain menyebar dari sel ke sel, bakteri juga dapat menyebar melalui aliran darah sehingga menyebabkan sepsis. Bakteri ini dapat bertahan hidup dalam sel penyaji antigen dan sel dendritik. Dengan demikian, sel-sel ini bertindak sebagai kendaraan yang mengangkut bakteri ke dalam sistem limfatik, sehingga menyebabkan penyebaran bakteri secara luas dalam tubuh manusia.[1][9]
Manakala Burkholderia pseudomallei dapat bertahan hidup dalam sel fagosit, sel-sel fagosit ini dapat membunuh Burkholderia pseudomallei melalui beberapa mekanisme. Makrofag yang diaktifkan oleh interferon gamma menaikkan daya bunuh terhadap Burkholderiapseudomallei melalui produksi sintase oksida nitrat yang dapat diinduksi. Pengasaman endosom dan degradasi bakteri juga mungkin, tetapi kapsul bakteri dan LPS membuat Burkholderia pseudomallei resisten terhadap degradasi lisosom. Setelah Burkholderia pseudomallei lolos ke sitosol inang, bakteri ini dapat dikenali oleh reseptor pengenal pola seperti reseptor mirip NOD, sehingga memicu pembentukan inflamasom dan aktivasi kaspase 1 yang menginduksi kematian sel inang oleh piroptosis dan aktivasi lebih lanjut dari sel inang. sistem kekebalan tubuh. Beberapa pertahanan inang sistemik juga berkontribusi kepada respons imun. Burkholderia pseudomallei memicu sistem komplemen dan kaskade penggumpalan darah, namun kapsul bakteri yang tebal mencegah aksi kompleks serangan membran komplemen.[1][9]
Unsur tambahan dari sistem imun diaktifkan oleh reseptor mirip tol inang seperti TLR2, TLR4, dan TLR5 yang mengenali bagian-bagian bakteri ini yang terlindung dari kerusakan seperti LPS dan flagela. Aktivasi ini menghasilkan produksi sitokin seperti interleukin 1 beta (IL-1β) dan interleukin-18 (IL-18). IL-18 meningkatkan produksi IFN melalui sel pembunuh alami, sedangkan IL-1β mengurangi produksi IFN. Molekul imun ini mendorong pendayagunaan sel imun lain seperti neutrofil, sel dendritik, sel B, dan sel T ke tempat infeksi. Sel T tampaknya sangat penting untuk mengendalikan Burkholderia pseudomallei; jumlah sel T meningkat pada orang yang bertahan hidup dan jumlah sel T yang rendah dikaitkan dengan risiko kematian yang tinggi akibat melioidosis. Meskipun demikian, infeksi HIV bukan merupakan faktor risiko melioidosis. Meskipun makrofag menunjukkan respons sitokin yang dideregulasi pada individu dengan infeksi HIV, internalisasi bakteri dan pembunuhan intraseluler masih efektif. Orang yang terinfeksi Burkholderia pseudomallei mengembangkan antibodi terhadap bakteri, dan orang yang tinggal di daerah endemik cenderung memiliki antibodi dalam darah mereka yang mengenali Burkholderia pseudomallei, tetapi efektivitas antibodi ini dalam mencegah melioidosis tidak jelas.[1][9]
B. pseudomallei can remain latent in the human body from 19 to 29 years until it is reactivated during immunosuppression or stress response. The site of bacteria during latent infection and the mechanism by which they avoid immune recognition for years are both unclear. Amongst the mechanisms suggested are residing in the nucleus of the cell to prevent being digested, entering a stage of slower growth, antibiotic resistance, and genetic adaption to the host environment. Granulomas (containing neutrophils, macrophages, lymphocytes, and multinucleated giant cells) formed at the infection site in melioidosis have been associated with latent infection in humans.[1]
Diagnosis



Bacterial culture is the definitive diagnosis of melioidosis. B. pseudomallei is never part of human flora. Therefore, any growth of the bacteria is diagnostic of melioidosis. Blood cultures are the most common samples for diagnosis, as bacteria can be detected in the blood in 50 to 60% of melioidosis cases. Other samples, such as throat, rectal swabs, pus from abscesses, and sputum, can also be used for culture. When bacteria do not grow from people strongly suspected of having melioidosis, repeated cultures should be taken, as subsequent cultures can become positive.[1] B. pseudomallei can be grown on sheep blood agar, MacConkey agar, Ashdown's medium (containing gentamicin),[1] or Ashdown's broth (containing colistin).[3] Agar plates for melioidosis should be incubated at 37 °C (98.6 °F) in air [2] and inspected daily for four days. On the agar plates, B. pseudomallei forms creamy, nonhaemolytic, colonies after 2 days of incubation. After 4 days of incubation, colonies appear dry and wrinkled.[1] Colonies of B. pseudomallei that are grown on Francis medium (a modification of Ashdown medium with gentamicin concentration increased to 8 mg/l) are yellow. For laboratories located outside endemic areas, Burkholderia cepacia selective agar or Pseudomonas selective agar can be used if Ashdown's medium is not available.[2] It is important not misinterpret the bacterial growth as Pseudomonas or Bacillus spp. Other biochemical screening tools can also be used for detecting B. pseudomallei, including the API 20NE or 20E biochemical kit combined with Gram stain, oxidase test, typical growth characteristics, and resistance to certain antibiotics of the bacteria.[3] Molecular methods such as 16S rDNA probes and polymerase chain reaction can also be used to detect B. pseudomallei in culture, but they are only available in research and reference laboratories.[1]
General blood tests in people with melioidosis show low white blood cell counts (indicates infection), raised liver enzymes, increased bilirubin levels (indicates liver dysfunction), and raised urea and creatinine levels (indicates kidney dysfunction). Low blood glucose and acidosis predicts a poorer prognosis in those with melioidosis. However, other tests such as C-reactive protein and procalcitonin levels are not reliable in predicting the severity of melioidosis infection.[15]
By microscopy, B. pseudomallei is seen as Gram-negative and rod-shaped, with a bipolar staining similar in appearance to a safety pin. Bacteria can sometimes be seen directly in clinical samples from infected people, but identification by light microscopy is neither specific nor sensitive. Immunofluorescence microscopy is highly specific for detecting bacteria directly from clinical specimens, but has less than 50% sensitivity.[1][3] A lateral flow immunoassay has been developed but not extensively evaluated.[1][3] An increasing number of laboratories use Matrix-assisted laser desorption/ionization mass spectrometry to identify the bacteria accurately.[9]
Serological tests such as indirect haemagglutination have been used to detect the presence of antibodies against B. pseudomallei. Different groups of people, though, have widely different levels of antibodies, so interpretation of these tests depends on location. In Australia, less than 5% of people have B. pseudomallei antibodies, so the presence of even relatively low amounts of antibody is unusual and could suggest melioidosis. In Thailand, many people have antibodies against B. pseudomallei, so only a relatively high amount of antibody in the blood suggests melioidosis.[1][3] Thailand also uses direct immunofluorescent antibody test (IFAT) and latex agglutination. In IFAT, both B. pseudomallei antigen and B. thailandensis can be used to quantify the amount of antibodies produced against the bacteria. Therefore, the results have to be interpreted with caution as a false-positive reaction could be found if someone is previously exposed to nonpathogenic B. thailandensis.[2] Latex agglutination is useful in screening for suspected B. pseudomallei colonies.[1] Commercial ELISA kits for melioidosis are no longer available in the market due to low sensitivity to human antibodies detection.[9]
Various imaging modalities can also help with the diagnosis of melioidosis. In acute melioidosis with the spreading of the bacteria through the bloodstream, the chest X-ray shows multifocal nodular lesions. It may also show merging nodules or cavitations. For those with acute melioidosis without the spread to the bloodstream, chest X-ray shows upper-lobe consolidation or cavitations. In chronic melioidosis, the slow progression of upper-lobe consolidation of the lungs resembles tuberculosis. For abscesses located in other parts of the body apart from the lungs, especially in the liver and spleen, CT scan has higher sensitivity when compared with an ultrasound scan. In liver and splenic abscesses, an ultrasound scan shows "target-like" lesions, while CT scan shows "honeycomb sign" in liver abscesses. For melioidosis involving the brain, MRI has higher sensitivity than a CT scan in diagnosing the lesion. MRI shows ring-enhancing lesions for brain melioidosis.[9]
Referensi
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw ax ay az ba bb Wiersinga WJ, Virk HS, Torres AG, Currie BJ, Peacock SJ, Dance DA, Limmathurotsakul D (February 2018). "Melioidosis". Nature Reviews. Disease Primers. 4 (17107): 17107. doi:10.1038/nrdp.2017.107. PMC 6456913
 . PMID 29388572.
. PMID 29388572.
- ^ a b c d e f g h i j k l m n o p q Foong YC, Tan M, Bradbury RS (30 October 2014). "Melioidosis: a review". Rural and Remote Health. 14 (4): 2763. PMID 25359677.
- ^ a b c d e f g h i j k l m n Currie BJ (February 2015). "Melioidosis: evolving concepts in epidemiology, pathogenesis, and treatment". Seminars in Respiratory and Critical Care Medicine. 36 (1): 111–25. doi:10.1055/s-0034-1398389
 . PMID 25643275.
. PMID 25643275.
- ^ Brightman, Christopher; Locum (2020). "Melioidosis: the Vietnamese time bomb". Trends in Urology & Men's Health (dalam bahasa Inggris). 11 (3): 30–32. doi:10.1002/tre.753
 . ISSN 2044-3749.
. ISSN 2044-3749.
- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamaWhitmore 1912 - ^ Currie BJ, Ward L, Cheng AC (2010). "The epidemiology and clinical spectrum of melioidosis: 540 cases from the 20 year Darwin prospective study". PLOS Negl Trop Dis. 4 (11): e900. doi:10.1371/journal.pntd.0000900. PMC 2994918
 . PMID 21152057.
. PMID 21152057.
- ^ a b Bennett JE, Raphael D, Martin JB, Currie BJ (2015). "223". Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases (edisi ke-Eighth). Elsevier. hlm. 2541–2549. ISBN 978-1-4557-4801-3.
- ^ Fertitta L, Monsel G, Torresi J, Caumes E (February 2019). "Cutaneous melioidosis: a review of the literature". International Journal of Dermatology. 58 (2): 221–227. doi:10.1111/ijd.14167. hdl:11343/284394
 . PMID 30132827.
. PMID 30132827.
- ^ a b c d e f g h i j k l Gassiep I, Armstrong M, Norton R (March 2020). "Human Melioidosis". Clinical Microbiology Reviews. 33 (2). doi:10.1128/CMR.00006-19. PMC 7067580
 . PMID 32161067.
. PMID 32161067.
- ^ Brightman, Christopher; Locum (2020). "Melioidosis: the Vietnamese time bomb". Trends in Urology & Men's Health (dalam bahasa Inggris). 11 (3): 30–32. doi:10.1002/tre.753
 . ISSN 2044-3749.
. ISSN 2044-3749.
- ^ a b Ngauy V, Lemeshev Y, Sadkowski L, Crawford G (February 2005). "Cutaneous melioidosis in a man who was taken as a prisoner of war by the Japanese during World War II". Journal of Clinical Microbiology. 43 (2): 970–2. doi:10.1128/JCM.43.2.970-972.2005. PMC 548040
 . PMID 15695721.
. PMID 15695721.
- ^ Gee JE, Gulvik CA, Elrod MG, Batra D, Rowe LA, Sheth M, Hoffmaster AR (July 2017). "Phylogeography of Burkholderia pseudomallei Isolates, Western Hemisphere". Emerging Infectious Diseases. 23 (7): 1133–1138. doi:10.3201/eid2307.161978. PMC 5512505
 . PMID 28628442.
. PMID 28628442.
- ^ Chodimella U, Hoppes WL, Whalen S, Ognibene AJ, Rutecki GW (May 1997). "Septicemia and suppuration in a Vietnam veteran". Hospital Practice. 32 (5): 219–21. doi:10.1080/21548331.1997.11443493. PMID 9153149.
- ^ Brightman, Christopher; Locum (2020). "Melioidosis: the Vietnamese time bomb". Trends in Urology & Men's Health (dalam bahasa Inggris). 11 (3): 30–32. doi:10.1002/tre.753
 . ISSN 2044-3749.
. ISSN 2044-3749.
- ^ a b c Cheng AC, Currie BJ (April 2005). "Melioidosis: epidemiology, pathophysiology, and management". Clinical Microbiology Reviews. 18 (2): 383–416. doi:10.1128/CMR.18.2.383-416.2005. PMC 1082802
 . PMID 15831829.
. PMID 15831829.
- ^ Baker A, Pearson T, Price EP, Dale J, Keim P, Hornstra H, et al. (March 2011). "Molecular phylogeny of Burkholderia pseudomallei from a remote region of Papua New Guinea". PLOS ONE. 6 (3): e18343. Bibcode:2011PLoSO...618343B. doi:10.1371/journal.pone.0018343
 . PMC 3069084
. PMC 3069084  . PMID 21483841.
. PMID 21483841. 
Pranala luar
| Klasifikasi | |
|---|---|
| Sumber luar |
- Resource Center for melioidosis
- Templat:CDCDiseaseInfo
- Burkholderia pseudomallei genomes and related information at PATRIC, a Bioinformatics Resource Center funded by NIAID
- Monograph on Melioidosis (ISBN 978-0-444-53479-8); Elsevier Press, 2012, https://www.researchgate.net/publication/354857974_Monograph_Melioidosis-a-century-of-observation-and-research_ISBN_978-0-444-53479-8
