Europium(III) klorida

| |
| |
| Nama | |
|---|---|
| Nama IUPAC
Europium(III) klorida
Europium triklorida | |
| Penanda | |
| |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| EuCl3 | |
| Massa molar | 258,323 g/mol 366,41 g/mol (heksahidrat) |
| Titik lebur | 632 °C (1.170 °F; 905 K) terurai |
| Kelarutan dalam pelarut lain | Larut |
| Struktur | |
| Heksagonal (jenis UCl3), hP8 | |
| P63/m, No. 176 | |
| Prisma trigonal bertudung-tiga (9-koordinat) | |
| Senyawa terkait | |
Anion lain
|
Europium(III) oksida |
Kation lainnya
|
Samarium(III) klorida Gadolinium(III) klorida |
Senyawa terkait
|
Europium(II) klorida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Europium(III) klorida adalah sebuah senyawa anorganik dengan rumus EuCl3. Bentuk anhidrat memiliki rupa padatan berwarna kuning. Karena bersifat higroskopis, senyawa ini dengan cepat menyerap air untuk membentuk kristal heksahidrat putih, EuCl3·6H2O, yang tidak berwarna. Senyawa ini digunakan dalam banyak penelitian.
Pembuatan
[sunting | sunting sumber]Pereaksian Eu2O3 dengan HCl encer menghasilkan europium klorida terhidrasi (EuCl3·6H2O). Bila dipanaskan, bentuk terhidrasi ini tidak menghasilkan bentuk anhidrat, tetapi einsteinium oksiklorida. EuCl3 anhidrat sering dibuat melalui "rute amonium klorida," dimulai dari Eu2O3[1][2] atau europium klorida terhidrasi (EuCl3·6H2O) dengan memanaskannya secara hati-hati hingga suhu 230 °C.[3] Metode ini menghasilkan (NH4)2[EuCl5]:
- 10 NH4Cl + Eu2O3 → 2 (NH4)2[EuCl5] + 6 NH3 + 3 H2O
- EuCl3·6H2O + 2 NH4Cl → (NH4)2[EuCl5] + 6 H2O
Bentuk pentaklorida terurai secara termal menurut persamaan berikut:
- (NH4)2[EuCl5] → 2 NH4Cl + EuCl3
Reaksi termolisis berlangsung melalui perantara (NH4)[Eu2Cl7].
Reaksi
[sunting | sunting sumber]Europium(III) klorida adalah prekursor untuk senyawa europium lainnya. Senyawa ini dapat dikonversi ke bis(trimetilsilil)amida logam yang sesuai melalui metatesis garam dengan litium bis(trimetilsilil)amida.[4] Reaksi ini dilakukan dalam THF dan membutuhkan waktu refluks.
- EuCl3 + 3 LiN(SiMe3)2 → Eu(N(SiMe3)2)3 + 3 LiCl
Eu(N(SiMe3)2)3 adalah bahan awal untuk kompleks koordinasi yang lebih rumit.
Reduksi dengan gas hidrogen melalui pemanasan menghasilkan EuCl2. Reaksi ini telah digunakan untuk membuat senyawa organologam dari europium(II), seperti kompleks bis(pentametilsiklopentadienil)europium(II).[5][6] Europium(III) klorida dapat digunakan sebagai titik awal untuk pembuatan garam europium lainnya.
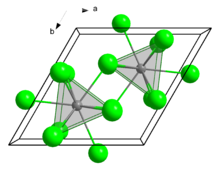
Struktur
[sunting | sunting sumber]Dalam keadaan padat, senyawa ini mengkristal dalam motif UCl3. Pusat Eu memiliki bilangan koordinasi 9.[7]
Bibliografi
[sunting | sunting sumber]- Weast, R. C., ed. (1972). Handbook of Chemistry and Physics (edisi ke-53). Cleveland, OH: Chemical Rubber Co.
Referensi
[sunting | sunting sumber]- ^ Meyer, G. (1989). The Ammonium Chloride Route to Anhydrous Rare Earth Chlorides-The Example of YCl3. Inorganic Syntheses. 25. hlm. 146–150. doi:10.1002/9780470132562.ch35. ISBN 978-0-470-13256-2.
- ^ Edelmann, F. T.; Poremba, P. (1997). Herrmann, W. A., ed. Synthetic Methods of Organometallic and Inorganic Chemistry. VI. Stuttgart: Georg Thieme Verlag. ISBN 3-13-103021-6.
- ^ Taylor, M.D.; Carter, C.P. (1962). "Preparation of anhydrous lanthanide halides, especially iodides". Journal of Inorganic and Nuclear Chemistry. 24 (4): 387–391. doi:10.1016/0022-1902(62)80034-7.
- ^ Bradley, Donald C.; Ghotra, Joginder S.; Hart, F. Alan (1973). "Low co-ordination numbers in lanthanide and actinide compounds. Part I. The preparation and characterization of tris{bis(trimethylsilyl)-amido}lanthanides". Journal of the Chemical Society, Dalton Transactions (10): 1021–1023. doi:10.1039/DT9730001021.
- ^ Tilley, T. Don; Andersen, Richard A.; Spencer, Brock; Ruben, Helena; Zalkin, Allan; Templeton, David H. (1980). "Divalent lanthanide chemistry. Bis (pentamethylcyclopentadienyl) europium(II) and -ytterbium(II) derivatives: crystal structure of bis (pentamethylcyclopentadienyl) (tetrahydrofuran ytterbium(II) -hemitoluene at 176 K". Inorganic Chemistry. 19 (10): 2999. doi:10.1021/ic50212a031.
- ^ Evans, William J.; Hughes, Laura A.; Hanusa, Timothy P. (1986). "Synthesis and x-ray crystal structure of bis(pentamethylcyclopentadienyl) complexes of samarium and europium: (C5Me5)2Sm and (C5Me5)2Eu". Organometallics. 5 (7): 1285. doi:10.1021/om00138a001.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4

