Boron trioksida
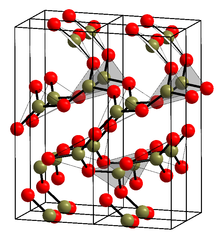
![Crystal structure of B2O3[1]](http://upload.wikimedia.org/wikipedia/commons/thumb/d/d9/B2O3powder.JPG/220px-B2O3powder.JPG)
| |
| |
| Nama | |
|---|---|
| Nama lain
boron oxide, diboron trioxide, boron sesquioxide, boric oxide, boria
Boric acid anhydride | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| B2O3 | |
| Massa molar | 69.6182 g/mol |
| Penampilan | putih, padat seperti kaca |
| Densitas | 2.460 g/cm3, liquid; 2.55 g/cm3, trigonal; |
| Titik lebur | 450 °C (842 °F; 723 K) (trigonal) 510 °C (tetrahedral) |
| Titik didih | 1.860 °C (3.380 °F; 2.130 K) ,[2] sublimates at 1500 °C[3] |
| 1.1 g/100mL (10 °C) 3.3 g/100mL (20 °C) 15.7 100 g/100mL (100 °C) | |
| Kelarutan | dapat larut sebagian dalam metanol |
| Keasaman (pKa) | ~ 4 |
| -39.0·10−6 cm3/mol | |
| Termokimia | |
| Kapasitas kalor (C) | 66.9 J/mol K |
| Entropi molar standar (S |
80.8 J/mol K |
| Entalpi pembentukan standar (ΔfH |
-1254 kJ/mol |
| Energi bebas Gibbs (ΔfG) | -832 kJ/mol |
| Bahaya | |
| Bahaya utama | Iritan[4] |
Klasifikasi UE (DSD) (usang)
|
Repr. Cat. 2 |
| Titik nyala | Tidak mudah terbakar |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
3163 mg/kg (lewat mulut, tikus)[5] |
| Batas imbas kesehatan AS (NIOSH): | |
PEL (yang diperbolehkan)
|
TWA 15 mg/m3[4] |
REL (yang direkomendasikan)
|
TWA 10 mg/m3[4] |
IDLH (langsung berbahaya)
|
2000 mg/m3[4] |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Boron trioksida (atau diboron trioksida) adalah senyawa anorganik berbentuk padat seperti kaca dan berwarna putih dengan rumus B2O3. Senyawa ini dapat dikristalkan melalui proses anil yang panjang.
Pembuatan
[sunting | sunting sumber]Boron trioksida dapat dihasilkan dari reaksi boraks dengan asam sulfat. Pada suhu di atas 750 °C, lapisan boron oksida yang meleleh terpisah dari natrium sulfat. Boron trioksida lalu didekantasi, didinginkan dan dihasilkan dengan tingkat kemurnian 96–97%.[3]
Metode lain adalah dengan memanaskan asam borat di atas suhu ~300 °C. Asam borat awalnya akan berdekomposisi menjadi uap (H2O(g)) dan asam metaborat (HBO2) pada suhu sekitar 170 °C, dan jika dipanaskan hingga di atas suhu 300 °C akan menghasilkan uap dan boron trioksida.
- H3BO3 → HBO2 + H2O
- 2 HBO2 → B2O3 + H2O
Referensi
[sunting | sunting sumber]- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamaa1 - ^ High temperature corrosion and materials chemistry: proceedings of the Per Kofstad Memorial Symposium. Proceedings of the Electrochemical Society. The Electrochemical Society. 2000. hlm. 496. ISBN 1-56677-261-3.
- ^ a b Patnaik, P. (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. hlm. 119. ISBN 0-07-049439-8. Diakses tanggal 2009-06-06.
- ^ a b c d "NIOSH Pocket Guide to Chemical Hazards #0060". National Institute for Occupational Safety and Health (NIOSH).
- ^ "Boron oxide". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
